
–ü—Ä–æ–±–ª–µ–º—ã –≠–≤–æ–ª—é—Ü–∏–∏ |
–ü–∞–ª–µ–æ–Ω—Ç–æ–ª. –∂—É—Ä–Ω. 2006. ‚Ññ1. –°. 1-11.
–ü–∞–ª–µ–æ–Ω—Ç–æ–ª. –∂—É—Ä–Ω. 2006. ‚Ññ1. –°. 1-11.
–£–î–ö 576.6:579.881
–ù–∞—à –æ–±–∑–æ—Ä "–ë–∞–∫—Ç–µ—Ä–∏—è –≤–æ–ª—å–±–∞—Ö–∏—è - –ø–æ–≤–µ–ª–∏—Ç–µ–ª—å –º—É—Ö"
1–ü–∞–ª–µ–æ–Ω—Ç–æ–ª–æ–≥–∏—á–µ—Å–∫–∏–π –ò–Ω—Å—Ç–∏—Ç—É—Ç –Ý–ê–ù
2–ò–Ω—Å—Ç–∏—Ç—É—Ç –æ–±—â–µ–π –≥–µ–Ω–µ—Ç–∏–∫–∏ –∏–º. –ù.–ò.–í–∞–≤–∏–ª–æ–≤–∞ –Ý–ê–ù
–ü–æ—Å—Ç—É–ø–∏–ª–∞ –≤ —Ä–µ–¥–∞–∫—Ü–∏—é 22.03.2005 –≥.
–ü—Ä–∏–æ–±—Ä–µ—Ç–µ–Ω–∏–µ —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–Ω—Ç–æ–≤ — –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–π, –¥–∞–≤—à–∏—Ö –Ω–∞—á–∞–ª–æ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º, –±—ã–ª–æ –æ–¥–Ω–∏–º –∏–∑ –∫–ª—é—á–µ–≤—ã—Ö —Å–æ–±—ã—Ç–∏–π –Ω–∞ –ø—É—Ç–∏ —Å—Ç–∞–Ω–æ–≤–ª–µ–Ω–∏—è —ç–≤–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–æ–π –∫–ª–µ—Ç–∫–∏. –î–ª—è —Ä–µ–∫–æ–Ω—Å—Ç—Ä—É–∫—Ü–∏–∏ —ç—Ç–æ–≥–æ –ø—Ä–æ—Ü–µ—Å—Å–∞ –±–æ–ª—å—à–æ–µ –∑–Ω–∞—á–µ–Ω–∏–µ –º–æ–∂–µ—Ç –∏–º–µ—Ç—å –∞–Ω–∞–ª–∏–∑ –≤–∑–∞–∏–º–æ–æ—Ç–Ω–æ—à–µ–Ω–∏–π, —Å–∫–ª–∞–¥—ã–≤–∞–≤—à–∏—Ö—Å—è –≤ –±–æ–ª–µ–µ –ø–æ–∑–¥–Ω–µ–µ –≤—Ä–µ–º—è —É —ç–≤–∫–∞—Ä–∏–æ—Ç —Å –¥—Ä—É–≥–∏–º–∏ –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏—è–º–∏. –í –∫–∞—á–µ—Å—Ç–≤–µ –º–æ–¥–µ–ª—å–Ω–æ–≥–æ –æ–±—ä–µ–∫—Ç–∞ —Ä–∞—Å—Å–º–∞—Ç—Ä–∏–≤–∞–µ—Ç—Å—è –±–∞–∫—Ç–µ—Ä–∏—è Wolbachia pipientis, –∂–∏–≤—É—â–∞—è –≤ –∫–ª–µ—Ç–∫–∞—Ö –º–Ω–æ–≥–∏—Ö –Ω–∞–∑–µ–º–Ω—ã—Ö –±–µ—Å–ø–æ–∑–æ–≤–æ–Ω–æ—á–Ω—ã—Ö –∏ –æ—Ç–ª–∏—á–∞—é—â–∞—è—Å—è —á—Ä–µ–∑–≤—ã—á–∞–π–Ω—ã–º —Ä–∞–∑–Ω–æ–æ–±—Ä–∞–∑–∏–µ–º —ç—Ñ—Ñ–µ–∫—Ç–æ–≤, –æ–∫–∞–∑—ã–≤–∞–µ–º—ã—Ö –µ—é –Ω–∞ —Å–≤–æ–∏—Ö —Ö–æ–∑—è–µ–≤. –ù–µ—Å–º–æ—Ç—Ä—è –Ω–∞ –∑–Ω–∞—á–∏—Ç–µ–ª—å–Ω–æ–µ —Å—Ö–æ–¥—Å—Ç–≤–æ –≤–æ–ª—å–±–∞—Ö–∏–∏ –∏ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π –ø–æ —Ä—è–¥—É —Å—É—â–µ—Å—Ç–≤–µ–Ω–Ω—ã—Ö –ø—Ä–∏–∑–Ω–∞–∫–æ–≤ (–±–∞–∑–æ–≤—ã–π –º–µ—Ç–∞–±–æ–ª–∏–∑–º, –æ—Ä–≥–∞–Ω–∏–∑–∞—Ü–∏—è –º–µ–º–±—Ä–∞–Ω–Ω–æ–≥–æ —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–∞ –º–∞–ª—ã—Ö –º–æ–ª–µ–∫—É–ª, —Å—Ç—Ä–æ–µ–Ω–∏–µ –æ–±–æ–ª–æ—á–∫–∏ –∏ –¥—Ä.), –∏—Ö –≤–∑–∞–∏–º–æ–æ—Ç–Ω–æ—à–µ–Ω–∏—è —Å –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º–æ–π –≤–æ –º–Ω–æ–≥–æ–º —è–≤–ª—è—é—Ç—Å—è –¥–∏–∞–º–µ—Ç—Ä–∞–ª—å–Ω–æ –ø—Ä–æ—Ç–∏–≤–æ–ø–æ–ª–æ–∂–Ω—ã–º–∏. –ú–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏ –∏–º–ø–æ—Ä—Ç–∏—Ä—É—é—Ç –±–æ–ª—å—à—É—é —á–∞—Å—Ç—å –Ω–µ–æ–±—Ö–æ–¥–∏–º—ã—Ö –∏–º –±–µ–ª–∫–æ–≤ –∏–∑ –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã –∏ –Ω–∞—Ö–æ–¥—è—Ç—Å—è –ø–æ–¥ –∫–æ–Ω—Ç—Ä–æ–ª–µ–º –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º–∞—Ç–∏—á–µ—Å–∫–∏—Ö —Ä–µ–≥—É–ª—è—Ç–æ—Ä–Ω—ã—Ö —Å–∏—Å—Ç–µ–º. –í–æ–ª—å–±–∞—Ö–∏—è, –Ω–∞–ø—Ä–æ—Ç–∏–≤, —ç–∫—Å–ø–æ—Ä—Ç–∏—Ä—É–µ—Ç –≤ —Ü–∏—Ç–æ–ø–ª–∞–∑–º—É —Ö–æ–∑—è–∏–Ω–∞ —Å–≤–æ–∏ –±–µ–ª–∫–∏, —Ä–µ–≥—É–ª–∏—Ä—É—é—â–∏–µ –µ–≥–æ –∂–∏–∑–Ω–µ–¥–µ—è—Ç–µ–ª—å–Ω–æ—Å—Ç—å, —á—Ç–æ –ø—Ä–∏–≤–æ–¥–∏—Ç –∫ –¥—Ä–∞–º–∞—Ç–∏—á–µ—Å–∫–∏–º –∏–∑–º–µ–Ω–µ–Ω–∏—è–º –æ–Ω—Ç–æ–≥–µ–Ω–µ–∑–∞ –∏ —Ä–µ–ø—Ä–æ–¥—É–∫—Ü–∏–∏ —Ö–æ–∑—è–∏–Ω–∞. –í–æ–∑–º–æ–∂–Ω–æ, –Ω–∞–±–ª—é–¥–∞–µ–º—ã–µ —Ä–∞–∑–ª–∏—á–∏—è –æ–±—ä—è—Å–Ω—è—é—Ç—Å—è –ø—Ä–µ–∂–¥–µ –≤—Å–µ–≥–æ —Ç–µ–º, —á—Ç–æ –±–æ–ª—å—à–∏–Ω—Å—Ç–≤–æ –≥–µ–Ω–æ–≤ –ø—Ä–æ—Ç–æ–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π –±—ã–ª–∏ –ø–µ—Ä–µ–Ω–µ—Å–µ–Ω—ã –≤ —Ü–µ–Ω—Ç—Ä–∞–ª—å–Ω—ã–π (—è–¥–µ—Ä–Ω—ã–π) –≥–µ–Ω–æ–º –Ω–∞ —Ä–∞–Ω–Ω–∏—Ö —ç—Ç–∞–ø–∞—Ö —Å—Ç–∞–Ω–æ–≤–ª–µ–Ω–∏—è —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–∑–∞, —Ç–æ–≥–¥–∞ –∫–∞–∫ –≥–µ–Ω—ã –≤–æ–ª—å–±–∞—Ö–∏–∏ –≤ —è–¥–µ—Ä–Ω—ã–π –≥–µ–Ω–æ–º —Ö–æ–∑—è–∏–Ω–∞, –ø–æ-–≤–∏–¥–∏–º–æ–º—É, –ø—Ä–∞–∫—Ç–∏—á–µ—Å–∫–∏ –Ω–µ –ø–µ—Ä–µ–Ω–æ—Å–∏–ª–∏—Å—å. –≠—Ç–æ —Å–æ–æ—Ç–≤–µ—Ç—Å—Ç–≤—É–µ—Ç –≤—ã—Å–∫–∞–∑–∞–Ω–Ω–æ–π —Ä–∞–Ω–µ–µ –≥–∏–ø–æ—Ç–µ–∑–µ –æ —Ç–æ–º, —á—Ç–æ –≤ —ç–≤–æ–ª—é—Ü–∏–∏ –ø—Ä–æ—Ç–æ—ç–≤–∫–∞—Ä–∏–æ—Ç –±—ã–ª –ø–µ—Ä–∏–æ–¥ –∞–∫—Ç–∏–≤–∏–∑–∞—Ü–∏–∏ –ª–∞—Ç–µ—Ä–∞–ª—å–Ω–æ–≥–æ –ø–µ—Ä–µ–Ω–æ—Å–∞; —Ç–æ–≥–¥–∞ –∏ –ø—Ä–æ–∏–∑–æ—à–ª–æ –ø—Ä–∏–æ–±—Ä–µ—Ç–µ–Ω–∏–µ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π. –í–ø–æ—Å–ª–µ–¥—Å—Ç–≤–∏–∏ —É —ç–≤–∫–∞—Ä–∏–æ—Ç —Ä–∞–∑–≤–∏–ª–∏—Å—å –º–µ—Ö–∞–Ω–∏–∑–º—ã –∑–∞—â–∏—Ç—ã –æ—Ç –ª–∞—Ç–µ—Ä–∞–ª—å–Ω–æ–≥–æ –ø–µ—Ä–µ–Ω–æ—Å–∞, –æ—Å–æ–±–µ–Ω–Ω–æ —Å–∏–ª—å–Ω–æ –≤—ã—Ä–∞–∂–µ–Ω–Ω—ã–µ —É –º–Ω–æ–≥–æ–∫–ª–µ—Ç–æ—á–Ω—ã—Ö –∂–∏–≤–æ—Ç–Ω—ã—Ö, –≤ —Ä–µ–∑—É–ª—å—Ç–∞—Ç–µ —á–µ–≥–æ –≥–µ–Ω—ã –Ω–æ–≤–æ–ø—Ä–∏–æ–±—Ä–µ—Ç–µ–Ω–Ω—ã—Ö —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–Ω—Ç–æ–≤ —É–∂–µ –Ω–µ –º–æ–≥—É—Ç –ø–µ—Ä–µ–Ω–æ—Å–∏—Ç—å—Å—è –≤ —Ü–µ–Ω—Ç—Ä–∞–ª—å–Ω—ã–π –≥–µ–Ω–æ–º, –∞ —Å–∞–º–∏ —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–Ω—Ç—ã —Å–æ—Ö—Ä–∞–Ω—è—é—Ç —Å–ø–æ—Å–æ–±–Ω–æ—Å—Ç—å –∫ —ç–≥–æ–∏—Å—Ç–∏—á–µ—Å–∫–æ–π —ç–≤–æ–ª—é—Ü–∏–∏.
–ü–æ—è–≤–ª–µ–Ω–∏–µ —ç–≤–∫–∞—Ä–∏–æ—Ç –±—ã–ª–æ –æ–¥–Ω–∏–º –∏–∑ –≤–∞–∂–Ω–µ–π—à–∏—Ö —Å–æ–±—ã—Ç–∏–π –≤ –∏—Å—Ç–æ—Ä–∏–∏ –∂–∏–∑–Ω–∏ –Ω–∞ –ó–µ–º–ª–µ, –∫–æ—Ç–æ—Ä–æ–µ —Å—É—â–µ—Å—Ç–≤–µ–Ω–Ω–æ –∏–∑–º–µ–Ω–∏–ª–æ —Å—Ç—Ä—É–∫—Ç—É—Ä—É –±–∏–æ—Å—Ñ–µ—Ä—ã –∏ –±–∏–æ–≥–µ–æ—Ö–∏–º–∏—á–µ—Å–∫–∏—Ö —Ü–∏–∫–ª–æ–≤ –∏ –æ—Ç–∫—Ä—ã–ª–æ –Ω–æ–≤—ã–µ –≤–æ–∑–º–æ–∂–Ω–æ—Å—Ç–∏ –¥–ª—è –ø—Ä–æ–≥—Ä–µ—Å—Å–∏–≤–Ω–æ–π —ç–≤–æ–ª—é—Ü–∏–∏ –∂–∏–≤—ã—Ö –æ—Ä–≥–∞–Ω–∏–∑–º–æ–≤ (Schopf, 1983; Martin, Russell, 2003). –°—á–∏—Ç–∞–µ—Ç—Å—è, —á—Ç–æ –±–æ–ª—å—à—É—é —á–∞—Å—Ç—å —Å–≤–æ–µ–≥–æ —Å—É—â–µ—Å—Ç–≤–æ–≤–∞–Ω–∏—è (–¥–æ 1 –º–ª—Ä–¥. –ª–µ—Ç –Ω–∞–∑–∞–¥) –±–∏–æ—Å—Ñ–µ—Ä–∞ –±—ã–ª–∞ –ø—Ä–µ–∏–º—É—â–µ—Å—Ç–≤–µ–Ω–Ω–æ –ø—Ä–æ–∫–∞—Ä–∏–æ—Ç–Ω–æ–π (–ó–∞–≤–∞—Ä–∑–∏–Ω, 2001). –û–¥–Ω–∞–∫–æ –≤ –ø–æ—Å–ª–µ–¥–Ω–µ–µ –≤—Ä–µ–º—è –ø–æ—è–≤–∏–ª–∏—Å—å –¥–∞–Ω–Ω—ã–µ, —Å–≤–∏–¥–µ—Ç–µ–ª—å—Å—Ç–≤—É—é—â–∏–µ –æ —Ç–æ–º, —á—Ç–æ —ç–≤–∫–∞—Ä–∏–æ—Ç—ã, –ø–æ-–≤–∏–¥–∏–º–æ–º—É, –ø–æ—è–≤–∏–ª–∏—Å—å –∏ –Ω–∞—á–∞–ª–∏ –∏–≥—Ä–∞—Ç—å —Å—É—â–µ—Å—Ç–≤–µ–Ω–Ω—É—é —Ä–æ–ª—å –≤ —Å—Ç—Ä—É–∫—Ç—É—Ä–µ —Å–æ–æ–±—â–µ—Å—Ç–≤ –∑–Ω–∞—á–∏—Ç–µ–ª—å–Ω–æ —Ä–∞–Ω—å—à–µ, —á—Ç–æ –ø–æ–∑–≤–æ–ª—è–µ—Ç –≥–æ–≤–æ—Ä–∏—Ç—å –æ —Å—É—â–µ—Å—Ç–≤–æ–≤–∞–Ω–∏–∏ «–ø–µ—Ä–µ—Ö–æ–¥–Ω–æ–π» (–ø—Ä–æ–∫–∞—Ä–∏–æ—Ç–Ω–æ — —ç–≤–∫–∞—Ä–∏–æ—Ç–Ω–æ–π) –±–∏–æ—Å—Ñ–µ—Ä—ã –≤ –ø–µ—Ä–∏–æ–¥ –æ—Ç 2 –¥–æ 1 –º–ª—Ä–¥. –ª–µ—Ç –Ω–∞–∑–∞–¥ (–Ý–æ–∑–∞–Ω–æ–≤, 2003). –û–± –æ—á–µ–Ω—å —Ä–∞–Ω–Ω–µ–º –ø–æ—è–≤–ª–µ–Ω–∏–∏ –ø–µ—Ä–≤—ã—Ö —ç–≤–∫–∞—Ä–∏–æ—Ç —Å–≤–∏–¥–µ—Ç–µ–ª—å—Å—Ç–≤—É—é—Ç, –≤ —á–∞—Å—Ç–Ω–æ—Å—Ç–∏, –æ—Å—Ç–∞—Ç–∫–∏ —Å—Ç–µ—Ä–æ–ª–æ–≤, –æ–±–Ω–∞—Ä—É–∂–µ–Ω–Ω—ã–µ –≤ –æ—Ç–ª–æ–∂–µ–Ω–∏—è—Ö –≤–æ–∑—Ä–∞—Å—Ç–æ–º 2.7 –º–ª—Ä–¥ –ª–µ—Ç (Brocks et al., 1999), –∞ —Ç–∞–∫–∂–µ «—ç–≤–∫–∞—Ä–∏–æ—Ç–æ–ø–æ–¥–æ–±–Ω—ã–µ» –º–∏–∫—Ä–æ—Ñ–æ—Å—Å–∏–ª–∏–∏, –æ–ø–∏—Å–∞–Ω–Ω—ã–µ –∏–∑ –æ—Ç–ª–æ–∂–µ–Ω–∏–π –≤–æ–∑—Ä–∞—Å—Ç–æ–º 2.9 — 3.0 –º–ª—Ä–¥. –ª–µ—Ç (–¢–∏–º–æ—Ñ–µ–µ–≤, 1982).
–ü—Ä–∏–æ–±—Ä–µ—Ç–µ–Ω–∏–µ –±–∞–∫—Ç–µ—Ä–∏–∞–ª—å–Ω—ã—Ö —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–Ω—Ç–æ–≤, –¥–∞–≤—à–∏—Ö –Ω–∞—á–∞–ª–æ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º, —è–≤–∏–ª–æ—Å—å –æ–¥–Ω–∏–º –∏–∑ –≥–ª–∞–≤–Ω—ã—Ö —Å–æ–±—ã—Ç–∏–π –Ω–∞ –ø—É—Ç–∏ —Å—Ç–∞–Ω–æ–≤–ª–µ–Ω–∏—è —ç–≤–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–æ–π –∫–ª–µ—Ç–∫–∏. –ù–µ–∫–æ—Ç–æ—Ä—ã–µ –∞–≤—Ç–æ—Ä—ã –ø–æ–ª–∞–≥–∞—é—Ç, —á—Ç–æ –∏–º–µ–Ω–Ω–æ –ø—Ä–∏–æ–±—Ä–µ—Ç–µ–Ω–∏–µ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π (–∞ –Ω–µ —è–¥—Ä–∞) –±—ã–ª–æ –∫–ª—é—á–µ–≤—ã–º –º–æ–º–µ–Ω—Ç–æ–º –≤ —Å—Ç–∞–Ω–æ–≤–ª–µ–Ω–∏–∏ —ç–≤–∫–∞—Ä–∏–æ—Ç (Vellai et al., 1998; Vellai, Vida, 1999). –°–æ–≤–º–µ—Å—Ç–Ω–æ–µ —Å—É—â–µ—Å—Ç–≤–æ–≤–∞–Ω–∏–µ –≤ –ø—Ä–µ–¥–µ–ª–∞—Ö –æ–¥–Ω–æ–π –∫–ª–µ—Ç–∫–∏ –¥–≤—É—Ö —Ä–∞–∑–Ω—ã—Ö –≥–µ–Ω–æ–º–æ–≤ —Ç—Ä–µ–±–æ–≤–∞–ª–æ —Ä–∞–∑–≤–∏—Ç–∏—è —ç—Ñ—Ñ–µ–∫—Ç–∏–≤–Ω–æ–π —Å–∏—Å—Ç–µ–º—ã –∏—Ö –∫–æ–º–ø–ª–µ–∫—Å–Ω–æ–π —Ä–µ–≥—É–ª—è—Ü–∏–∏ –∏ –∫–æ–æ—Ä–¥–∏–Ω–∞—Ü–∏–∏. –ü–æ—ç—Ç–æ–º—É –ø—Ä–∏–æ–±—Ä–µ—Ç–µ–Ω–∏–µ –≤–Ω—É—Ç—Ä–∏–∫–ª–µ—Ç–æ—á–Ω—ã—Ö —Å–∏–º–±–∏–æ–Ω—Ç–æ–≤ –º–æ–≥–ª–æ —Å—Ç–∞—Ç—å –≤–∞–∂–Ω—ã–º —Å—Ç–∏–º—É–ª–æ–º –≤ —Ä–∞–∑–≤–∏—Ç–∏–∏ —è–¥—Ä–∞ –∏ –≥–µ–Ω–Ω–æ-—Ä–µ–≥—É–ª—è—Ç–æ—Ä–Ω—ã—Ö —Å–∏—Å—Ç–µ–º (–ú–∞—Ä–∫–æ–≤, 2005). –ê–Ω–∞–ª–∏–∑ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã—Ö –≥–µ–Ω–æ–º–æ–≤ –ø–æ–∫–∞–∑–∞–ª –º–æ–Ω–æ—Ñ–∏–ª–µ—Ç–∏—á–µ—Å–∫–æ–µ –ø—Ä–æ–∏—Å—Ö–æ–∂–¥–µ–Ω–∏–µ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π –≤—Å–µ—Ö —Å–æ–≤—Ä–µ–º–µ–Ω–Ω—ã—Ö —ç–≤–∫–∞—Ä–∏–æ—Ç (Dyall, Johnson, 2000; –õ–∏—Ç–æ—à–µ–Ω–∫–æ, 2002; Boussau et al., 2004). –ë–µ–∑–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã–µ –ø—Ä–æ—Å—Ç–µ–π—à–∏–µ, –ø–æ –≤—Å–µ–π –≤–∏–¥–∏–º–æ—Å—Ç–∏, –ø—Ä–æ–∏—Å—Ö–æ–¥—è—Ç –æ—Ç –ø—Ä–µ–¥–∫–æ–≤, –∏–º–µ–≤—à–∏—Ö –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏, –ø–æ—Å–∫–æ–ª—å–∫—É –≤ –∏—Ö —è–¥–µ—Ä–Ω–æ–π –î–ù–ö –æ–±–Ω–∞—Ä—É–∂–µ–Ω—ã –≥–µ–Ω—ã –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω–æ–≥–æ –ø—Ä–æ–∏—Å—Ö–æ–∂–¥–µ–Ω–∏—è. –ò–Ω—Ç–µ—Ä–µ—Å–µ–Ω —Ñ–∞–∫—Ç –æ–±–Ω–∞—Ä—É–∂–µ–Ω–∏—è —É —ç–≤–∫–∞—Ä–∏–æ—Ç —è–¥–µ—Ä–Ω—ã—Ö –≥–µ–Ω–æ–≤, –∫–æ–¥–∏—Ä—É—é—â–∏—Ö —Ü–∏—Ç–æ–ø–ª–∞–∑–º–∞—Ç–∏—á–µ—Å–∫–∏–µ –±–µ–ª–∫–∏, –Ω–æ –ø–æ –ø–æ—Å–ª–µ–¥–æ–≤–∞—Ç–µ–ª—å–Ω–æ—Å—Ç—è–º –Ω—É–∫–ª–µ–æ—Ç–∏–¥–æ–≤ –±–ª–∏–∑–∫–∏—Ö –∫ –≥–µ–Ω–∞–º –ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–π (–ø—Ä–µ–¥–∫–æ–≤ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π). –≠—Ç–æ –≥–æ–≤–æ—Ä–∏—Ç –æ —Ç–æ–º, —á—Ç–æ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã–π —Å–∏–º–±–∏–æ–Ω—Ç –º–æ–≥ —Å—ã–≥—Ä–∞—Ç—å –±–æ–ª–µ–µ –∑–Ω–∞—á–∏—Ç–µ–ª—å–Ω—É—é —Ä–æ–ª—å –≤ —Ñ–æ—Ä–º–∏—Ä–æ–≤–∞–Ω–∏–∏ –≥–µ–Ω–µ—Ç–∏—á–µ—Å–∫–æ–π –∏ –±–∏–æ—Ö–∏–º–∏—á–µ—Å–∫–æ–π —Å—Ç—Ä—É–∫—Ç—É—Ä—ã —ç–≤–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–æ–π –∫–ª–µ—Ç–∫–∏, —á–µ–º —Ä–∞–Ω–µ–µ –ø—Ä–µ–¥–ø–æ–ª–∞–≥–∞–ª–æ—Å—å. –ú–Ω–æ–≥–∏–µ –∏–∑–Ω–∞—á–∞–ª—å–Ω–æ «–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã–µ» –≥–µ–Ω—ã –±—ã–ª–∏ –∞–¥–∞–ø—Ç–∏—Ä–æ–≤–∞–Ω—ã –¥–ª—è –≤—ã–ø–æ–ª–Ω–µ–Ω–∏—è —è–¥–µ—Ä–Ω–æ-—Ü–∏—Ç–æ–ø–ª–∞–∑–º–∞—Ç–∏—á–µ—Å–∫–∏—Ö —Ñ—É–Ω–∫—Ü–∏–π (Roger, 1999; Gabaldon, Huynen, 2003).
–ü—Ä–µ–¥–∫–æ–º –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π –±—ã–ª–∏ –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–∏ (–∫ –∫–æ—Ç–æ—Ä—ã–º –æ—Ç–Ω–æ—Å—è—Ç—Å—è, –≤ —á–∞—Å—Ç–Ω–æ—Å—Ç–∏, –Ω–µ–∫–æ—Ç–æ—Ä—ã–µ –ø—É—Ä–ø—É—Ä–Ω—ã–µ –±–∞–∫—Ç–µ—Ä–∏–∏, –æ—Å—É—â–µ—Å—Ç–≤–ª—è—é—â–∏–µ –±–µ—Å–∫–∏—Å–ª–æ—Ä–æ–¥–Ω—ã–π —Ñ–æ—Ç–æ—Å–∏–Ω—Ç–µ–∑). –í–æ–ø—Ä–æ—Å –æ —Ç–æ–º, –∫ –∫–∞–∫–æ–π –∏–∑ –≥—Ä—É–ø–ø –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–π –ø—Ä–∏–Ω–∞–¥–ª–µ–∂–∞–ª –ø—Ä–µ–¥–æ–∫ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π, –æ—Å—Ç–∞–µ—Ç—Å—è –¥–∏—Å–∫—É—Å—Å–∏–æ–Ω–Ω—ã–º. –ù–µ–∫–æ—Ç–æ—Ä—ã–µ –∞–≤—Ç–æ—Ä—ã —Å–±–ª–∏–∂–∞—é—Ç –ø—Ä–µ–¥–∫–∞ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π —Å —Ä–∏–∫–∫–µ—Ç—Å–∏–µ–≤—ã–º–∏ (Andersson et al., 1998; Emelyanov, 2003). –ù–µ–¥–∞–≤–Ω–æ –±—ã–ª–æ –ø–æ–∫–∞–∑–∞–Ω–æ, —á—Ç–æ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã–π –≥–µ–Ω–æ–º –¥—Ä–æ–∂–∂–µ–π –Ω–∞–∏–±–æ–ª–µ–µ –±–ª–∏–∑–æ–∫ –∫ –≥–µ–Ω–æ–º—É –ø—É—Ä–ø—É—Ä–Ω–æ–π –Ω–µ—Å–µ—Ä–Ω–æ–π –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–∏ Rhodospirillum rubrum (Esser et al., 2004). –≠–ª–µ–∫—Ç—Ä–æ–Ω–Ω–æ-—Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–Ω–∞—è —Ü–µ–ø—å, –∏–∑–Ω–∞—á–∞–ª—å–Ω–æ —Å—Ñ–æ—Ä–º–∏—Ä–æ–≤–∞–≤—à–∞—è—Å—è —É —ç—Ç–∏—Ö –±–∞–∫—Ç–µ—Ä–∏–π –∫–∞–∫ —á–∞—Å—Ç—å —Ñ–æ—Ç–æ—Å–∏–Ω—Ç–µ—Ç–∏—á–µ—Å–∫–æ–≥–æ –∞–ø–ø–∞—Ä–∞—Ç–∞, –≤–ø–æ—Å–ª–µ–¥—Å—Ç–≤–∏–∏ –±—ã–ª–∞ –∞–¥–∞–ø—Ç–∏—Ä–æ–≤–∞–Ω–∞ –¥–ª—è –∫–∏—Å–ª–æ—Ä–æ–¥–Ω–æ–≥–æ –¥—ã—Ö–∞–Ω–∏—è. –ì–ª–∞–≤–Ω—ã–º —Å—Ç–∏–º—É–ª–æ–º –æ–±—ä–µ–¥–∏–Ω–µ–Ω–∏—è –∞–Ω–∞—ç—Ä–æ–±–Ω–æ–≥–æ –ø—Ä–µ–¥–∫–∞ –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã —Å «–ø—Ä–æ—Ç–æ–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–µ–π» –±—ã–ª–∞ –ø–æ—Ç—Ä–µ–±–Ω–æ—Å—Ç—å –ø–µ—Ä–≤–æ–≥–æ –∑–∞—â–∏—Ç–∏—Ç—å—Å—è –æ—Ç —Ç–æ–∫—Å–∏—á–µ—Å–∫–æ–≥–æ –¥–µ–π—Å—Ç–≤–∏—è –∫–∏—Å–ª–æ—Ä–æ–¥–∞ (Gupta, 1998; Kurland, Andersson, 2000; Dolan et al., 2002).
–í—Å–∫–æ—Ä–µ –ø–æ—Å–ª–µ –ø–µ—Ä–µ—Ö–æ–¥–∞ –ø—Ä–µ–¥–∫–æ–≤ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π –∫ —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–∑—É –∑–Ω–∞—á–∏—Ç–µ–ª—å–Ω–∞—è —á–∞—Å—Ç—å –∏—Ö –≥–µ–Ω–æ–≤ –±—ã–ª–∞ –ø–µ—Ä–µ–Ω–µ—Å–µ–Ω–∞ –≤ —è–¥—Ä–æ, –≥–¥–µ –æ–Ω–∏ –ø–æ–ø–∞–ª–∏ –ø–æ–¥ –∫–æ–Ω—Ç—Ä–æ–ª—å —è–¥–µ—Ä–Ω–æ-—Ü–∏—Ç–æ–ø–ª–∞–∑–º–∞—Ç–∏—á–µ—Å–∫–∏—Ö —Ä–µ–≥—É–ª—è—Ç–æ—Ä–Ω—ã—Ö —Å–∏—Å—Ç–µ–º. –ì–µ–Ω—ã –ø–µ—Ä–µ–Ω–æ—Å–∏–ª–∏—Å—å —Ü–µ–ª—ã–º–∏ –∫—Ä—É–ø–Ω—ã–º–∏ –±–ª–æ–∫–∞–º–∏ (Martin, 2003). –ü–∞—Ä–∞–ª–ª–µ–ª—å–Ω–æ —Å —ç—Ç–∏–º –º–Ω–æ–≥–∏–µ –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–∞–ª—å–Ω—ã–µ –±–µ–ª–∫–∏ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π –±—ã–ª–∏ –∑–∞–º–µ–Ω–µ–Ω—ã –∏–ª–∏ –¥–æ–ø–æ–ª–Ω–µ–Ω—ã –Ω–æ–≤—ã–º–∏ —ç–≤–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–∏–º–∏ –±–µ–ª–∫–∞–º–∏, –≥–µ–Ω—ã –∫–æ—Ç–æ—Ä—ã—Ö —Å—Ñ–æ—Ä–º–∏—Ä–æ–≤–∞–ª–∏—Å—å –≤ —è–¥–µ—Ä–Ω–æ–º –≥–µ–Ω–æ–º–µ –∏ –Ω–∏–∫–æ–≥–¥–∞ –Ω–µ –≤—Ö–æ–¥–∏–ª–∏ –≤ —Å–æ—Å—Ç–∞–≤ –≥–µ–Ω–æ–º–æ–≤ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π –∏–ª–∏ –∏—Ö –ø—Ä–µ–¥–∫–æ–≤ (Karlberg, 2004).
–Ý–µ–∫–æ–Ω—Å—Ç—Ä—É–∫—Ü–∏—è —Ä–∞–∑–≤–∏—Ç–∏—è —Å–∏–º–±–∏–æ—Ç–∏—á–µ—Å–∫–∏—Ö –æ—Ç–Ω–æ—à–µ–Ω–∏–π –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π —Å –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º–æ–π –∏–º–µ–µ—Ç –∫–ª—é—á–µ–≤–æ–µ –∑–Ω–∞—á–µ–Ω–∏–µ –¥–ª—è –ø–æ–Ω–∏–º–∞–Ω–∏—è –≤—Å–µ–≥–æ –ø—Ä–æ—Ü–µ—Å—Å–∞ —Å—Ç–∞–Ω–æ–≤–ª–µ–Ω–∏—è —ç–≤–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–æ–π –∫–ª–µ—Ç–∫–∏. –û–¥–Ω–∏–º –∏–∑ –≤–æ–∑–º–æ–∂–Ω—ã—Ö –ø–æ–¥—Ö–æ–¥–æ–≤ –∫ –ø–æ—Å—Ç—Ä–æ–µ–Ω–∏—é —Ç–∞–∫–æ–π —Ä–µ–∫–æ–Ω—Å—Ç—Ä—É–∫—Ü–∏–∏ —è–≤–ª—è–µ—Ç—Å—è –∏–∑—É—á–µ–Ω–∏–µ –≤–∑–∞–∏–º–æ–æ—Ç–Ω–æ—à–µ–Ω–∏–π, —Å–∫–ª–∞–¥—ã–≤–∞–≤—à–∏—Ö—Å—è –≤ –±–æ–ª–µ–µ –ø–æ–∑–¥–Ω–µ–µ –≤—Ä–µ–º—è —É —ç–≤–∫–∞—Ä–∏–æ—Ç —Å –ø—Ä–æ–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–∏–º–∏ –≤–Ω—É—Ç—Ä–∏–∫–ª–µ—Ç–æ—á–Ω—ã–º–∏ —Å–∏–º–±–∏–æ–Ω—Ç–∞–º–∏. –û—Å–æ–±—ã–π –∏–Ω—Ç–µ—Ä–µ—Å –ø—Ä–µ–¥—Å—Ç–∞–≤–ª—è—é—Ç —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–Ω—Ç—ã, –æ—Ç–Ω–æ—Å—è—â–∏–µ—Å—è –∫ –≥—Ä—É–ø–ø–µ –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–π.
–í –¥–∞–Ω–Ω–æ–π —Å—Ç–∞—Ç—å–µ –≤ –∫–∞—á–µ—Å—Ç–≤–µ «–º–æ–¥–µ–ª—å–Ω–æ–≥–æ –æ–±—ä–µ–∫—Ç–∞» —Ä–∞—Å—Å–º–∞—Ç—Ä–∏–≤–∞–µ—Ç—Å—è –æ–¥–Ω–∞ –∏–∑ –∏–Ω—Ç–µ—Ä–µ—Å–Ω–µ–π—à–∏—Ö —ç–Ω–¥–æ—Å–∏–º–±–∏–æ—Ç–∏—á–µ—Å–∫–∏—Ö –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–π — Wolbachia pipientis, –æ—Ç–ª–∏—á–∞—é—â–∞—è—Å—è –Ω–µ–æ–±—ã—á–∞–π–Ω—ã–º —Ä–∞–∑–Ω–æ–æ–±—Ä–∞–∑–Ω–∏–µ–º —ç—Ñ—Ñ–µ–∫—Ç–æ–≤, –æ–∫–∞–∑—ã–≤–∞–µ–º—ã—Ö –µ—é –Ω–∞ —Ä–∞–∑–ª–∏—á–Ω—ã—Ö —Ö–æ–∑—è–µ–≤. –í —Å—Ç–∞—Ç—å–µ —Å—Ä–∞–≤–Ω–∏–≤–∞—é—Ç—Å—è —Å–∏—Å—Ç–µ–º—ã –≤–∑–∞–∏–º–æ–¥–µ–π—Å—Ç–≤–∏—è –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã —Å –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º–∏ –∏ —Å –≤–æ–ª—å–±–∞—Ö–∏—è–º–∏. –í—ã—è—Å–Ω–µ–Ω–∏–µ –≤–æ–∑–º–æ–∂–Ω—ã—Ö –ø—Ä–∏—á–∏–Ω –≤—ã—è–≤–ª–µ–Ω–Ω—ã—Ö —Å—Ö–æ–¥—Å—Ç–≤ –∏ —Ä–∞–∑–ª–∏—á–∏–π –ø–æ–∑–≤–æ–ª—è–µ—Ç –≤—ã–¥–µ–ª–∏—Ç—å –Ω–µ–∫–æ—Ç–æ—Ä—ã–µ –∫–ª—é—á–µ–≤—ã–µ —Ñ–∞–∫—Ç–æ—Ä—ã, –æ–ø—Ä–µ–¥–µ–ª–∏–≤—à–∏–µ —Å–ø–µ—Ü–∏—Ñ–∏–∫—É –≤–∑–∞–∏–º–æ–æ—Ç–Ω–æ—à–µ–Ω–∏–π –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã —Å –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º–∏ –Ω–∞ —Ä–∞–Ω–Ω–∏—Ö —ç—Ç–∞–ø–∞—Ö —Å—Ç–∞–Ω–æ–≤–ª–µ–Ω–∏—è —ç–≤–∫–∞—Ä–∏–æ—Ç. –ö—Ä–æ–º–µ —Ç–æ–≥–æ, –≤–æ–ª—å–±–∞—Ö–∏—è –ø—Ä–µ–¥—Å—Ç–∞–≤–ª—è–µ—Ç –±–æ–ª—å—à–æ–π —Ç–µ–æ—Ä–µ—Ç–∏—á–µ—Å–∫–∏–π –∏–Ω—Ç–µ—Ä–µ—Å –∏ —Å–∞–º–∞ –ø–æ —Å–µ–±–µ, –∫–∞–∫ –ø—Ä–∏–º–µ—Ä –≤ –≤—ã—Å—à–µ–π —Å—Ç–µ–ø–µ–Ω–∏ –Ω–µ–æ–±—ã—á–Ω–æ–≥–æ —Ñ–∞–∫—Ç–æ—Ä–∞, —Å–ø–æ—Å–æ–±–Ω–æ–≥–æ –æ–∫–∞–∑—ã–≤–∞—Ç—å —Å—É—â–µ—Å—Ç–≤–µ–Ω–Ω–æ–µ –≤–ª–∏—è–Ω–∏–µ –Ω–∞ —ç–≤–æ–ª—é—Ü–∏—é –º–Ω–æ–≥–æ–∫–ª–µ—Ç–æ—á–Ω—ã—Ö —ç–≤–∫–∞—Ä–∏–æ—Ç.
–ë–∞–∫—Ç–µ—Ä–∏—è Wolbachia –∂–∏–≤–µ—Ç –≤ –∫–ª–µ—Ç–∫–∞—Ö –æ–≥—Ä–æ–º–Ω–æ–≥–æ –º–Ω–æ–∂–µ—Å—Ç–≤–∞ –Ω–∞–∑–µ–º–Ω—ã—Ö –±–µ—Å–ø–æ–∑–≤–æ–Ω–æ—á–Ω—ã—Ö. –í–æ–ª—å–±–∞—Ö–∏–µ–π –∑–∞—Ä–∞–∂–µ–Ω—ã –º–Ω–æ–≥–∏–µ –Ω–∞—Å–µ–∫–æ–º—ã–µ: –¥–≤—É–∫—Ä—ã–ª—ã–µ, –±–∞–±–æ—á–∫–∏, –∂—É–∫–∏, –±–ª–æ—Ö–∏, –≤—à–∏, –ø—Ä—è–º–æ–∫—Ä—ã–ª—ã–µ, —Ç–µ—Ä–º–∏—Ç—ã, –∫–ª–æ–ø—ã, —Å—Ç—Ä–µ–∫–æ–∑—ã, –ø–µ—Ä–µ–ø–æ–Ω—á–∞—Ç–æ–∫—Ä—ã–ª—ã–µ, –Ω–æ–≥–æ—Ö–≤–æ—Å—Ç–∫–∏ –∏ –¥—Ä. –ü–æ —Ä–∞–∑–Ω—ã–º –æ—Ü–µ–Ω–∫–∞–º, –∏–∑ –æ–±—â–µ–≥–æ —á–∏—Å–ª–∞ –≤–∏–¥–æ–≤ –Ω–∞—Å–µ–∫–æ–º—ã—Ö –æ—Ç 20 –¥–æ 75% –∑–∞—Ä–∞–∂–µ–Ω—ã –≤–æ–ª—å–±–∞—Ö–∏–µ–π. –í–æ–ª—å–±–∞—Ö–∏—è –Ω–∞–π–¥–µ–Ω–∞ —Ç–∞–∫–∂–µ —É –º–Ω–æ–≥–∏—Ö –ø–∞—É–∫–æ–≤, –∫–ª–µ—â–µ–π, —Ä–∞–∫–æ–æ–±—Ä–∞–∑–Ω—ã—Ö (–Ω–∞–∑–µ–º–Ω—ã—Ö, –ª–∏—Ç–æ—Ä–∞–ª—å–Ω—ã—Ö –∏ –ø—Ä–µ—Å–Ω–æ–≤–æ–¥–Ω—ã—Ö –∏–∑–æ–ø–æ–¥ –∏ –ª–∏—Ç–æ—Ä–∞–ª—å–Ω—ã—Ö –∞–º—Ñ–∏–ø–æ–¥) –∏ –Ω–µ–º–∞—Ç–æ–¥ — —Ñ–∏–ª—è—Ä–∏–π. –ü–æ –º–µ—Ä–µ –∏–∑—É—á–µ–Ω–∏—è –∫—Ä—É–≥ –∏–∑–≤–µ—Å—Ç–Ω—ã—Ö —Ö–æ–∑—è–µ–≤ –≤–æ–ª—å–±–∞—Ö–∏–∏ –ø–æ—Å—Ç–æ—è–Ω–Ω–æ —Ä–∞—Å—Ç–µ—Ç. –Ø—Å–Ω–æ, —á—Ç–æ –∑–∞—Ä–∞–∂–µ–Ω–Ω–æ—Å—Ç—å –≤–æ–ª—å–±–∞—Ö–∏–µ–π —É –Ω–∞–∑–µ–º–Ω—ã—Ö –±–µ—Å–ø–æ–∑–≤–æ–Ω–æ—á–Ω—ã—Ö — —è–≤–ª–µ–Ω–∏–µ –ø–æ–≤—Å–µ–º–µ—Å—Ç–Ω–æ–µ –∏ –º–∞—Å—Å–æ–≤–æ–µ (Stouthamer et al., 1999).
–° —Ä–∞–∑–Ω—ã–º–∏ —Ö–æ–∑—è–µ–≤–∞–º–∏ –æ—Ç–Ω–æ—à–µ–Ω–∏—è –≤–æ–ª—å–±–∞—Ö–∏–∏ —Å–∫–ª–∞–¥—ã–≤–∞—é—Ç—Å—è –ø–æ-—Ä–∞–∑–Ω–æ–º—É. –û–Ω–∞ –º–æ–∂–µ—Ç –±—ã—Ç—å –∫–∞–∫ –ø–∞—Ä–∞–∑–∏—Ç–æ–º, —Ç–∞–∫ –∏ –∫–æ–º–º–µ–Ω—Å–∞–ª–æ–º –∏–ª–∏ —Å–∏–º–±–∏–æ–Ω—Ç–æ–º. –í–æ–ª—å–±–∞—Ö–∏—è –Ω–∞—É—á–∏–ª–∞—Å—å —Ç–æ–Ω–∫–æ —Ä–µ–≥—É–ª–∏—Ä–æ–≤–∞—Ç—å —Ä–∞–∑–º–Ω–æ–∂–µ–Ω–∏–µ –∏ —Ä–∞–∑–≤–∏—Ç–∏–µ —Å–≤–æ–∏—Ö —Ö–æ–∑—è–µ–≤. –ü–æ—ç—Ç–æ–º—É –µ–µ –Ω–∞–∑—ã–≤–∞—é—Ç «–º–∏–∫—Ä–æ–±–æ–º — –º–∞–Ω–∏–ø—É–ª—è—Ç–æ—Ä–æ–º» (Stouthamer et al., 1999). –®–∏—Ä–æ–∫–∞—è —Ä–∞—Å–ø—Ä–æ—Å—Ç—Ä–∞–Ω–µ–Ω–Ω–æ—Å—Ç—å –≤–æ–ª—å–±–∞—Ö–∏–∏ –∏ –µ–µ –±–æ–ª—å—à–æ–µ —Ç–µ–æ—Ä–µ—Ç–∏—á–µ—Å–∫–æ–µ –∏ –ø—Ä–∞–∫—Ç–∏—á–µ—Å–∫–æ–µ –∑–Ω–∞—á–µ–Ω–∏–µ –æ–±—É—Å–ª–∞–≤–ª–∏–≤–∞—é—Ç –ø–æ–≤—ã—à–µ–Ω–Ω—ã–π –∏–Ω—Ç–µ—Ä–µ—Å –∏—Å—Å–ª–µ–¥–æ–≤–∞—Ç–µ–ª–µ–π –∫ —ç—Ç–æ–π –±–∞–∫—Ç–µ—Ä–∏–∏.
–û –≤—Ä–µ–º–µ–Ω–∏ –ø—Ä–æ–∏—Å—Ö–æ–∂–¥–µ–Ω–∏—è –≤–æ–ª—å–±–∞—Ö–∏–∏ –º–æ–∂–Ω–æ —Å—É–¥–∏—Ç—å —Ç–æ–ª—å–∫–æ –ø–æ –º–æ–ª–µ–∫—É–ª—è—Ä–Ω–æ-–≥–µ–Ω–µ—Ç–∏—á–µ—Å–∫–∏–º –¥–∞–Ω–Ω—ã–º, –ø–æ—Å–∫–æ–ª—å–∫—É –≤ –ø–∞–ª–µ–æ–Ω—Ç–æ–ª–æ–≥–∏—á–µ—Å–∫–æ–π –ª–µ—Ç–æ–ø–∏—Å–∏ —Å–ª–µ–¥—ã –µ–µ –ø—Ä–∏—Å—É—Ç—Å—Ç–≤–∏—è –ø–æ–∫–∞ –Ω–µ –æ–±–Ω–∞—Ä—É–∂–µ–Ω—ã. –ü–æ-–≤–∏–¥–∏–º–æ–º—É, –¥–≤–µ –æ—Å–Ω–æ–≤–Ω—ã–µ –≥—Ä—É–ø–ø—ã —à—Ç–∞–º–º–æ–≤ –≤–æ–ª—å–±–∞—Ö–∏–∏ (A+B –∏ C+D, –∂–∏–≤—É—â–∏–µ –≤ —á–ª–µ–Ω–∏—Å—Ç–æ–Ω–æ–≥–∏—Ö –∏ –Ω–µ–º–∞—Ç–æ–¥–∞—Ö —Å–æ–æ—Ç–≤–µ—Ç—Å—Ç–≤–µ–Ω–Ω–æ) —Ä–∞–∑–æ—à–ª–∏—Å—å –æ–∫–æ–ª–æ 100 –º–ª–Ω. –ª–µ—Ç –Ω–∞–∑–∞–¥ (–≤ —Å–µ—Ä–µ–¥–∏–Ω–µ –º–µ–ª–∞), –∞ –ª–∏–Ω–∏–∏ A –∏ B — 58-67 –º–ª–Ω. –ª–µ—Ç –Ω–∞–∑–∞–¥ (–ø—Ä–∏–º–µ—Ä–Ω–æ –Ω–∞ —Ä—É–±–µ–∂–µ –º–µ–ª–∞ –∏ –ø–∞–ª–µ–æ–≥–µ–Ω–∞) (Werren et al., 1995b; Bandi et al., 1998). –ü–æ-–≤–∏–¥–∏–º–æ–º—É, –≤–æ–ª—å–±–∞—Ö–∏—è –ø—Ä–æ–∏–∑–æ—à–ª–∞ –Ω–µ –æ—Ç —Å–≤–æ–±–æ–¥–Ω–æ–∂–∏–≤—É—â–∏—Ö –ø—Ä–µ–¥–∫–æ–≤, –∞ –æ—Ç –¥—Ä—É–≥–∏—Ö –≤–Ω—É—Ç—Ä–∏–∫–ª–µ—Ç–æ—á–Ω—ã—Ö –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–π –±–æ–ª–µ–µ 100 –º–ª–Ω. –ª–µ—Ç –Ω–∞–∑–∞–¥ (—Å–∫–æ—Ä–µ–µ –≤—Å–µ–≥–æ, –≤ —Ä–∞–Ω–Ω–µ–º –º–µ–ª—É) (Stouthamer et al., 1999). –í–µ—Ä–æ—è—Ç–Ω–æ, –Ω–∞—á–∞–ª—å–Ω—ã–µ —ç—Ç–∞–ø—ã —ç–≤–æ–ª—é—Ü–∏–∏ –≤–æ–ª—å–±–∞—Ö–∏–∏ –±—ã–ª–∏ —Å–≤—è–∑–∞–Ω—ã —Å —ç–∫—Å–ø–∞–Ω—Å–∏–µ–π –ø–æ–∫—Ä—ã—Ç–æ—Å–µ–º–µ–Ω–Ω—ã—Ö —Ä–∞—Å—Ç–µ–Ω–∏–π –∏ –Ω–∞—Å–µ–∫–æ–º—ã—Ö –≤ –Ω–∞—á–∞–ª–µ — —Å–µ—Ä–µ–¥–∏–Ω–µ –º–µ–ª–∞.
–í–æ–∑–¥–µ–π—Å—Ç–≤–∏–µ –≤–æ–ª—å–±–∞—Ö–∏–∏ –Ω–∞ —Ö–æ–∑—è–µ–≤
–Ý–∞–∑–Ω–æ–æ–±—Ä–∞–∑–Ω—ã–µ –º–∞–Ω–∏–ø—É–ª—è—Ü–∏–∏, –ø—Ä–æ–∏–∑–≤–æ–¥–∏–º—ã–µ –≤–æ–ª—å–±–∞—Ö–∏–µ–π –Ω–∞–¥ —Å–≤–æ–∏–º–∏ —Ö–æ–∑—è–µ–≤–∞–º–∏, –ø—Ä–µ—Å–ª–µ–¥—É—é—Ç –æ–¥–Ω—É –æ–±—â—É—é —Ü–µ–ª—å — –º–∞–∫—Å–∏–º–∞–ª—å–Ω–æ–µ —Ä–∞—Å–ø—Ä–æ—Å—Ç—Ä–∞–Ω–µ–Ω–∏–µ –±–∞–∫—Ç–µ—Ä–∏–∏ –≤ –∑–∞—Ä–∞–∂–µ–Ω–Ω–æ–π –ø–æ–ø—É–ª—è—Ü–∏–∏. –í–æ–ª—å–±–∞—Ö–∏—è, –ø–æ–¥–æ–±–Ω–æ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º, –º–æ–∂–µ—Ç –∂–∏—Ç—å —Ç–æ–ª—å–∫–æ –≤–Ω—É—Ç—Ä–∏ –∫–ª–µ—Ç–æ–∫ –¥—Ä—É–≥–æ–≥–æ (—ç–≤–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–æ–≥–æ) –æ—Ä–≥–∞–Ω–∏–∑–º–∞. –û–Ω–∞ –Ω–µ —Ä–∞—Å—Ç–µ—Ç –Ω–∞ –∏—Å–∫—É—Å—Å—Ç–≤–µ–Ω–Ω—ã—Ö —Å—Ä–µ–¥–∞—Ö, –∏ –¥–∞–∂–µ –≤ –∫—É–ª—å—Ç—É—Ä–∞—Ö –∫–ª–µ—Ç–æ–∫ (–Ω–∞—Å–µ–∫–æ–º—ã—Ö –∏ –º–ª–µ–∫–æ–ø–∏—Ç–∞—é—â–∏—Ö) –≤—ã—Ä–∞—Å—Ç–∏—Ç—å –µ–µ —É–¥–∞–ª–æ—Å—å –ª–∏—à—å –Ω–µ–¥–∞–≤–Ω–æ (Noda et al., 2002). –ü–µ—Ä–µ–¥–∞–µ—Ç—Å—è –≤–æ–ª—å–±–∞—Ö–∏—è (–∫–∞–∫ –∏ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏) –≤ –æ—Å–Ω–æ–≤–Ω–æ–º –≤–µ—Ä—Ç–∏–∫–∞–ª—å–Ω–æ, –ø–æ –º–∞—Ç–µ—Ä–∏–Ω—Å–∫–æ–π –ª–∏–Ω–∏–∏, –ø—Ä–æ–Ω–∏–∫–∞—è –≤ —Ü–∏—Ç–æ–ø–ª–∞–∑–º—É —è–π—Ü–µ–∫–ª–µ—Ç–æ–∫ –∏, —Ç–∞–∫–∏–º –æ–±—Ä–∞–∑–æ–º, –∑–∞—Ä–∞–∂–∞—è –ø–æ—Ç–æ–º—Å—Ç–≤–æ. –ì–æ—Ä–∏–∑–æ–Ω—Ç–∞–ª—å–Ω–∞—è –ø–µ—Ä–µ–¥–∞—á–∞ —Ç–æ–∂–µ –ø—Ä–æ–∏—Å—Ö–æ–¥–∏—Ç, –Ω–æ —Å—Ä–∞–≤–Ω–∏—Ç–µ–ª—å–Ω–æ —Ä–µ–¥–∫–æ (Werren et al., 1995a; Heath et al., 1999; Van Meer et al., 1999). –û–Ω–∞ –∑–∞—Ç—Ä—É–¥–Ω–µ–Ω–∞ –Ω–µ—Å–ø–æ—Å–æ–±–Ω–æ—Å—Ç—å—é –≤–æ–ª—å–±–∞—Ö–∏–∏ –∂–∏—Ç—å –≤–Ω–µ –∫–ª–µ—Ç–æ–∫ —Ö–æ–∑—è–∏–Ω–∞. –≠—Ç–∏ –æ—Å–æ–±–µ–Ω–Ω–æ—Å—Ç–∏ –æ–ø—Ä–µ–¥–µ–ª—è—é—Ç –∫—Ä—É–≥ –æ—Å–Ω–æ–≤–Ω—ã—Ö –∑–∞–¥–∞—á, —Å—Ç–æ—è—â–∏—Ö –ø–µ—Ä–µ–¥ –ø–∞—Ä–∞–∑–∏—Ç–æ–º. –ß—Ç–æ–±—ã –æ–±–µ—Å–ø–µ—á–∏—Ç—å —Å–æ–±—Å—Ç–≤–µ–Ω–Ω–æ–µ —Ä–∞—Å–ø—Ä–æ—Å—Ç—Ä–∞–Ω–µ–Ω–∏–µ, –≤–æ–ª—å–±–∞—Ö–∏—è «–∑–∞–∏–Ω—Ç–µ—Ä–µ—Å–æ–≤–∞–Ω–∞» –≤ —Ç–æ–º, —á—Ç–æ–±—ã: 1) –ø—Ä–∏—á–∏–Ω—è—Ç—å –∫–∞–∫ –º–æ–∂–Ω–æ –º–µ–Ω—å—à–µ –≤—Ä–µ–¥–∞ –∑–∞—Ä–∞–∂–µ–Ω–Ω–æ–π —Å–∞–º–∫–µ –∏–ª–∏ –¥–∞–∂–µ –ø–æ–≤—ã—à–∞—Ç—å –µ–µ –∂–∏–∑–Ω–µ—Å–ø–æ—Å–æ–±–Ω–æ—Å—Ç—å; 2) –ø–æ–≤—ã—à–∞—Ç—å –ø–ª–æ–¥–æ–≤–∏—Ç–æ—Å—Ç—å –∑–∞—Ä–∞–∂–µ–Ω–Ω—ã—Ö —Å–∞–º–æ–∫; 3) —Å–Ω–∏–∂–∞—Ç—å –ø–ª–æ–¥–æ–≤–∏—Ç–æ—Å—Ç—å –Ω–µ–∑–∞—Ä–∞–∂–µ–Ω–Ω—ã—Ö —Å–∞–º–æ–∫ (–¥–ª—è —ç—Ç–æ–≥–æ –≤ –∫–∞—á–µ—Å—Ç–≤–µ «–æ—Ä—É–¥–∏—è» –∏—Å–ø–æ–ª—å–∑—É—é—Ç—Å—è –∑–∞—Ä–∞–∂–µ–Ω–Ω—ã–µ —Å–∞–º—Ü—ã, —Å–º. –Ω–∏–∂–µ); 4) —Å–¥–≤–∏–≥–∞—Ç—å —Å–æ–æ—Ç–Ω–æ—à–µ–Ω–∏–µ –ø–æ–ª–æ–≤ –≤ –ø–æ–ø—É–ª—è—Ü–∏–∏ —Ö–æ–∑—è–µ–≤ –≤ —Å—Ç–æ—Ä–æ–Ω—É –ø—Ä–µ–æ–±–ª–∞–¥–∞–Ω–∏—è —Å–∞–º–æ–∫. –î–µ–ª–æ –≤ —Ç–æ–º, —á—Ç–æ –≤–æ–ª—å–±–∞—Ö–∏—è –Ω–µ –º–æ–∂–µ—Ç –ø–µ—Ä–µ–¥–∞–≤–∞—Ç—å—Å—è —Å–æ —Å–ø–µ—Ä–º–∞—Ç–æ–∑–æ–∏–¥–∞–º–∏ (Bressac, Rousset, 1993). –ë–∞–∫—Ç–µ—Ä–∏–∏, –ø–æ–ø–∞–≤—à–∏–µ –≤ –æ—Ä–≥–∞–Ω–∏–∑–º —Å–∞–º—Ü–∞, –Ω–µ –∏–º–µ—é—Ç —à–∞–Ω—Å–æ–≤ –ø–µ—Ä–µ–¥–∞—Ç—å —Å–≤–æ–µ –ø–æ—Ç–æ–º—Å—Ç–≤–æ —Å–ª–µ–¥—É—é—â–µ–º—É –ø–æ–∫–æ–ª–µ–Ω–∏—é —Ö–æ–∑—è–µ–≤. –ü–æ—ç—Ç–æ–º—É —Å–∞–º—Ü—ã —è–≤–ª—è—é—Ç—Å—è –¥–ª—è –≤–æ–ª—å–±–∞—Ö–∏–∏ —Å–≤–æ–µ–≥–æ —Ä–æ–¥–∞ «–Ω–µ–Ω—É–∂–Ω—ã–º –±–∞–ª–ª–∞—Å—Ç–æ–º».
–í–ª–∏—è–Ω–∏–µ, –æ–∫–∞–∑—ã–≤–∞–µ–º–æ–µ –≤–æ–ª—å–±–∞—Ö–∏–µ–π –Ω–∞ —Ö–æ–∑—è–∏–Ω–∞, –æ–ø—Ä–µ–¥–µ–ª—è–µ—Ç—Å—è –≤ –ø–µ—Ä–≤—É—é –æ—á–µ—Ä–µ–¥—å —à—Ç–∞–º–º–æ–º –±–∞–∫—Ç–µ—Ä–∏–∏ –∏ –ª–∏—à—å –≤–æ –≤—Ç–æ—Ä—É—é — –±–∏–æ–ª–æ–≥–∏–µ–π —Ö–æ–∑—è–∏–Ω–∞. –ö—Ä–∞—Ç–∫–æ —Ä–∞—Å—Å–º–æ—Ç—Ä–∏–º –æ—Å–Ω–æ–≤–Ω—ã–µ —Ç–∏–ø—ã —ç—Ñ—Ñ–µ–∫—Ç–æ–≤, –ø—Ä–æ–∏–∑–æ–¥–∏–º—ã—Ö –≤–æ–ª—å–±–∞—Ö–∏–µ–π.
–¶–∏—Ç–æ–ø–ª–∞–∑–º–∞—Ç–∏—á–µ—Å–∫–∞—è –Ω–µ—Å–æ–≤–º–µ—Å—Ç–∏–º–æ—Å—Ç—å (–¶–ù) — –Ω–∞–∏–±–æ–ª–µ–µ —à–∏—Ä–æ–∫–æ —Ä–∞—Å–ø—Ä–æ—Å—Ç—Ä–∞–Ω–µ–Ω–Ω—ã–π –∏, –ø–æ-–≤–∏–¥–∏–º–æ–º—É, —ç–≤–æ–ª—é—Ü–∏–æ–Ω–Ω–æ —Å–∞–º—ã–π –¥—Ä–µ–≤–Ω–∏–π —ç—Ñ—Ñ–µ–∫—Ç –≤–æ–ª—å–±–∞—Ö–∏–∏. –¶–ù –ø—Ä–æ—è–≤–ª—è–µ—Ç—Å—è –≤ —Ç–æ–º, —á—Ç–æ –∫–æ–≥–¥–∞ –∑–∞—Ä–∞–∂–µ–Ω–Ω—ã–π —Å–∞–º–µ—Ü –æ–ø–ª–æ–¥–æ—Ç–≤–æ—Ä—è–µ—Ç –Ω–µ–∑–∞—Ä–∞–∂–µ–Ω–Ω—É—é —Å–∞–º–∫—É, –æ—Ç—Ü–æ–≤—Å–∫–∏–µ —Ö—Ä–æ–º–æ—Å–æ–º—ã –≤ –æ–ø–ª–æ–¥–æ—Ç–≤–æ—Ä–µ–Ω–Ω–æ–º —è–π—Ü–µ –≤–µ–¥—É—Ç —Å–µ–±—è –Ω–µ–Ω–æ—Ä–º–∞–ª—å–Ω–æ –∏ –≤ –∫–æ–Ω—Ü–µ –∫–æ–Ω—Ü–æ–≤ —Ä–∞–∑—Ä—É—à–∞—é—Ç—Å—è (Richardson et al., 1987; Callaini et al., 1997). –í —Ä–µ–∑—É–ª—å—Ç–∞—Ç–µ —è–π—Ü–æ –æ—Å—Ç–∞–µ—Ç—Å—è —Ñ–∞–∫—Ç–∏—á–µ—Å–∫–∏ –≥–∞–ø–ª–æ–∏–¥–Ω—ã–º, –∏ —ç–º–±—Ä–∏–æ–Ω –≤—Å–∫–æ—Ä–µ –ø–æ–≥–∏–±–∞–µ—Ç. –ú–æ–ª–µ–∫—É–ª—è—Ä–Ω—ã–π –º–µ—Ö–∞–Ω–∏–∑–º –¶–ù –¥–æ –∫–æ–Ω—Ü–∞ –Ω–µ –≤—ã—è—Å–Ω–µ–Ω. –°–æ–≥–ª–∞—Å–Ω–æ –Ω–∞–∏–±–æ–ª–µ–µ –∞—Ä–≥—É–º–µ–Ω—Ç–∏—Ä–æ–≤–∞–Ω–Ω–æ–π –≥–∏–ø–æ—Ç–µ–∑–µ, –≤–æ–ª—å–±–∞—Ö–∏–∏, –∂–∏–≤—É—â–∏–µ –≤ –≥–æ–Ω–∞–¥–∞—Ö —Å–∞–º—Ü–∞, –∫–∞–∫–∏–º-—Ç–æ –æ–±—Ä–∞–∑–æ–º –º–æ–¥–∏—Ñ–∏—Ü–∏—Ä—É—é—Ç («–º–µ—Ç—è—Ç») —Ö—Ä–æ–º–æ—Å–æ–º—ã —Å–ø–µ—Ä–º–∞—Ç–æ–∑–æ–∏–¥–æ–≤. –≠—Ç–∞ –º–µ—Ç–∫–∞ –∏ —è–≤–ª—è–µ—Ç—Å—è –ø—Ä–∏—á–∏–Ω–æ–π —Ä–∞–∑—Ä—É—à–µ–Ω–∏—è —Ö—Ä–æ–º–æ—Å–æ–º –ø–æ—Å–ª–µ –æ–ø–ª–æ–¥–æ—Ç–≤–æ—Ä–µ–Ω–∏—è. –û–¥–Ω–∞–∫–æ –µ—Å–ª–∏ —Å–∞–º–∫–∞ –∑–∞—Ä–∞–∂–µ–Ω–∞ —Ç–µ–º –∂–µ —Å–∞–º—ã–º —à—Ç–∞–º–º–æ–º –≤–æ–ª—å–±–∞—Ö–∏–∏, –æ—Ç—Ü–æ–≤—Å–∫–∏–µ —Ö—Ä–æ–º–æ—Å–æ–º—ã –Ω–µ —Ä–∞–∑—Ä—É—à–∞—é—Ç—Å—è, –∏ –∏–∑ —è–π—Ü–∞ —Ä–∞–∑–≤–∏–≤–∞–µ—Ç—Å—è –Ω–æ—Ä–º–∞–ª—å–Ω–∞—è –æ—Å–æ–±—å (–µ—Å—Ç–µ—Å—Ç–≤–µ–Ω–Ω–æ, –∑–∞—Ä–∞–∂–µ–Ω–Ω–∞—è). –ü–æ –≤—Å–µ–π –≤–µ—Ä–æ—è—Ç–Ω–æ—Å—Ç–∏, –ø—Ä–∏—Å—É—Ç—Å—Ç–≤—É—é—â–∏–µ –≤ —è–π—Ü–µ–∫–ª–µ—Ç–∫–µ –±–∞–∫—Ç–µ—Ä–∏–∏ –∫–∞–∫–∏–º-—Ç–æ –æ–±—Ä–∞–∑–æ–º —Ä–∞—Å–ø–æ–∑–Ω–∞—é—Ç –º–µ—Ç–∫—É –∏ —Å–ø–∞—Å–∞—é—Ç —Ö—Ä–æ–º–æ—Å–æ–º—ã –æ—Ç —Ä–∞–∑—Ä—É—à–µ–Ω–∏—è. –≠—Ç–æ —Ä–∞—Å–ø–æ–∑–Ω–∞–≤–∞–Ω–∏–µ –∏ «—Å–ø–∞—Å–µ–Ω–∏–µ» –≤ –±–æ–ª—å—à–∏–Ω—Å—Ç–≤–µ —Å–ª—É—á–∞–µ–≤ —è–≤–ª—è–µ—Ç—Å—è —à—Ç–∞–º–º–æ—Å–ø–µ—Ü–∏—Ñ–∏—á–Ω—ã–º: –≤–æ–ª—å–±–∞—Ö–∏–∏ —Å–ø–∞—Å–∞—é—Ç —Ç–æ–ª—å–∫–æ —Ö—Ä–æ–º–æ—Å–æ–º—ã, –ø–æ–º–µ—á–µ–Ω–Ω—ã–µ —Ç–µ–º –∂–µ —Å–∞–º—ã–º —à—Ç–∞–º–º–æ–º (Werren, 1997).
–ü–∞—Ä—Ç–µ–Ω–æ–≥–µ–Ω–µ–∑. –£ —Ä—è–¥–∞ –ø–µ—Ä–µ–ø–æ–Ω—á–∞—Ç–æ–∫—Ä—ã–ª—ã—Ö, —Ç—Ä–∏–ø—Å–æ–≤, –Ω–æ–≥–æ—Ö–≤–æ—Å—Ç–æ–∫ –∏ –∫–ª–µ—â–µ–π –≤–æ–ª—å–±–∞—Ö–∏—è –≤—ã–∑—ã–≤–∞–µ—Ç –ø–µ—Ä–µ—Ö–æ–¥ –∫ –ø–∞—Ä—Ç–µ–Ω–æ–≥–µ–Ω–µ–∑—É. –£ –ø–µ—Ä–µ–ø–æ–Ω—á–∞—Ç–æ–∫—Ä—ã–ª—ã—Ö –≤ –Ω–æ—Ä–º–µ –∏–∑ –Ω–µ–æ–ø–ª–æ–¥–æ—Ç–≤–æ—Ä–µ–Ω–Ω—ã—Ö —è–∏—Ü —Ä–∞–∑–≤–∏–≤–∞—é—Ç—Å—è —Å–∞–º—Ü—ã, –∏–∑ –æ–ø–ª–æ–¥–æ—Ç–≤–æ—Ä–µ–Ω–Ω—ã—Ö — —Å–∞–º–∫–∏. –í–æ–ª—å–±–∞—Ö–∏—è –≤–º–µ—à–∏–≤–∞–µ—Ç—Å—è –≤ –ø—Ä–æ—Ü–µ—Å—Å –æ–Ω—Ç–æ–≥–µ–Ω–µ–∑–∞, –Ω–∞—Ä—É—à–∞—è –Ω–æ—Ä–º–∞–ª—å–Ω—ã–π —Ö–æ–¥ —Ä–∞–∑–≤–∏—Ç–∏—è –Ω–∞—Å–µ–∫–æ–º–æ–≥–æ. –ö–æ–≥–¥–∞ –Ω–µ–æ–ø–ª–æ–¥–æ—Ç–≤–æ—Ä–µ–Ω–Ω–æ–µ —è–π—Ü–æ (–∏–∑ –∫–æ—Ç–æ—Ä–æ–≥–æ –≤ –Ω–æ—Ä–º–µ –¥–æ–ª–∂–µ–Ω —Ä–∞–∑–≤–∏—Ç—å—Å—è —Å–∞–º–µ—Ü) –≤—Å—Ç—É–ø–∞–µ—Ç –≤ –ø–µ—Ä–≤—ã–π –º–∏—Ç–æ–∑, –≤–æ–ª—å–±–∞—Ö–∏—è –æ—Å—Ç–∞–Ω–∞–≤–ª–∏–≤–∞–µ—Ç –ø—Ä–æ—Ü–µ—Å—Å –≤ –∞–Ω–∞—Ñ–∞–∑–µ, –∫–æ–≥–¥–∞ —Ö—Ä–æ–º–æ—Å–æ–º—ã —É–∂–µ —É–¥–≤–æ–∏–ª–∏—Å—å, –∞ –¥–æ—á–µ—Ä–Ω–∏–µ —è–¥—Ä–∞ –µ—â–µ –Ω–µ —Ä–∞–∑–¥–µ–ª–∏–ª–∏—Å—å. –í —Ä–µ–∑—É–ª—å—Ç–∞—Ç–µ —è–π—Ü–æ —Å—Ç–∞–Ω–æ–≤–∏—Ç—Å—è –¥–∏–ø–ª–æ–∏–¥–Ω—ã–º, –∏ –∏–∑ –Ω–µ–≥–æ —Ä–∞–∑–≤–∏–≤–∞–µ—Ç—Å—è —Å–∞–º–∫–∞ (Stouthamer, Kazmer, 1994).
–§–µ–º–∏–Ω–∏–∑–∞—Ü–∏—è. –í–æ–ª—å–±–∞—Ö–∏—è –ø—Ä–µ–≤—Ä–∞—â–∞–µ—Ç –≥–µ–Ω–µ—Ç–∏—á–µ—Å–∫–∏—Ö —Å–∞–º—Ü–æ–≤ –≤ —Å–∞–º–æ–∫ —É —Ä–∞–≤–Ω–æ–Ω–æ–≥–∏—Ö —Ä–∞–∫–æ–æ–±—Ä–∞–∑–Ω—ã—Ö (–∏–∑–æ–ø–æ–¥). –ú–µ—Ö–∞–Ω–∏–∑–º —è–≤–ª–µ–Ω–∏—è –∏–∑—É—á–µ–Ω —É –º–æ–∫—Ä–∏—Ü Armadillidium vulgare. –û–∫–∞–∑–∞–ª–æ—Å—å, —á—Ç–æ –≤–æ–ª—å–±–∞—Ö–∏—è –≤–æ–∑–¥–µ–π—Å—Ç–≤—É–µ—Ç –Ω–∞ —Å–∏—Å—Ç–µ–º—É –≤—ã—Ä–∞–±–æ—Ç–∫–∏ –∞–Ω–¥—Ä–æ–≥–µ–Ω–Ω–æ–≥–æ –≥–æ—Ä–º–æ–Ω–∞. –ü—Ä–∏ –æ—Ç—Å—É—Ç—Å—Ç–≤–∏–∏ —ç—Ç–æ–≥–æ –≥–æ—Ä–º–æ–Ω–∞ –∏–∑ —ç–º–±—Ä–∏–æ–Ω–∞ —Ä–∞–∑–≤–∏–≤–∞–µ—Ç—Å—è —Å–∞–º–∫–∞, –ø—Ä–∏ –µ–≥–æ –Ω–∞–ª–∏—á–∏–∏ — —Å–∞–º–µ—Ü. –£ –∑–∞—Ä–æ–¥—ã—à–µ–π –º–æ–∫—Ä–∏—Ü –º—É–∂—Å–∫–æ–≥–æ –ø–æ–ª–∞ –≤–æ–ª—å–±–∞—Ö–∏—è –ø–æ–¥–∞–≤–ª—è–µ—Ç —Ä–∞–∑–≤–∏—Ç–∏–µ –∞–Ω–¥—Ä–æ–≥–µ–Ω–Ω–æ–π –∂–µ–ª–µ–∑—ã, –≤—ã—Ä–∞–±–∞—Ç—ã–≤–∞—é—â–µ–π –¥–∞–Ω–Ω—ã–π –≥–æ—Ä–º–æ–Ω (LeGrand et al., 1987). –ï—Å–ª–∏ –∏—Å–∫—É—Å—Å—Ç–≤–µ–Ω–Ω–æ –∑–∞—Ä–∞–∑–∏—Ç—å –≤–æ–ª—å–±–∞—Ö–∏–µ–π –≤–∑—Ä–æ—Å–ª–æ–≥–æ —Å–∞–º—Ü–∞ –º–æ–∫—Ä–∏—Ü—ã, —É –∫–æ—Ç–æ—Ä–æ–≥–æ —É–∂–µ –∏–º–µ–µ—Ç—Å—è –∞–Ω–¥—Ä–æ–≥–µ–Ω–Ω–∞—è –∂–µ–ª–µ–∑–∞, –ø—Ä–æ–∏—Å—Ö–æ–¥–∏—Ç —á–∞—Å—Ç–∏—á–Ω–∞—è —Ñ–µ–º–∏–Ω–∏–∑–∞—Ü–∏—è, —Ö–æ—Ç—è –¥–µ—è—Ç–µ–ª—å–Ω–æ—Å—Ç—å –∞–Ω–¥—Ä–æ–≥–µ–Ω–Ω–æ–π –∂–µ–ª–µ–∑—ã –ø—Ä–∏ —ç—Ç–æ–º –ø—Ä–æ–¥–æ–ª–∂–∞–µ—Ç—Å—è. –ü—Ä–∏ —á–∞—Å—Ç–∏—á–Ω–æ–π —Ñ–µ–º–∏–Ω–∏–∑–∞—Ü–∏–∏ –ø–æ—è–≤–ª—é—Ç—Å—è –∏–Ω—Ç–µ—Ä—Å–µ–∫—Å—ã — –æ—Å–æ–±–∏ —Å —Ä–∞–∑–ª–∏—á–Ω—ã–º–∏ —Å–æ—á–µ—Ç–∞–Ω–∏—è–º–∏ –º—É–∂—Å–∫–∏—Ö –∏ –∂–µ–Ω—Å–∫–∏—Ö –ø—Ä–∏–∑–Ω–∞–∫–æ–≤. –£ –∏–∑–æ–ø–æ–¥ —Å–∞–º–∫–∏ –≥–µ—Ç–µ—Ä–æ–≥–∞–º–µ—Ç–Ω—ã (—Ç.–µ. –∏–º–µ—é—Ç –¥–≤–µ —Ä–∞–∑–Ω—ã–µ –ø–æ–ª–æ–≤—ã–µ —Ö—Ä–æ–º–æ—Å–æ–º—ã WZ, —É —Å–∞–º—Ü–æ–≤ ZZ). –ï—Å–ª–∏ –≤—ã–ª–µ—á–∏—Ç—å «–Ω–µ–æ—Å–∞–º–∫—É» (—Ç.–µ. –∑–∞—Ä–∞–∂–µ–Ω–Ω—É—é –º–æ–∫—Ä–∏—Ü—É —Å —Ö—Ä–æ–º–æ—Å–æ–º–∞–º–∏ ZZ — –≥–µ–Ω–µ—Ç–∏—á–µ—Å–∫–æ–≥–æ —Å–∞–º—Ü–∞), —Ç–æ, –µ—Å–ª–∏ «—Å–∞–º–∫–∞» –º–æ–ª–æ–¥–∞—è, –æ–Ω–∞ —á–∞—Å—Ç–∏—á–Ω–æ –∏–ª–∏ –ø–æ–ª–Ω–æ—Å—Ç—å—é –ø—Ä–µ–≤—Ä–∞—â–∞–µ—Ç—Å—è –≤ —Å–∞–º—Ü–∞, –∞ –µ—Å–ª–∏ —Å—Ç–∞—Ä–∞—è — –æ—Å—Ç–∞–µ—Ç—Å—è —Å–∞–º–∫–æ–π, –Ω–æ –ø—Ä–æ–∏–∑–≤–æ–¥–∏—Ç –Ω–∞ —Å–≤–µ—Ç –∏—Å–∫–ª—é—á–∏—Ç–µ–ª—å–Ω–æ –æ–¥–Ω–∏—Ö —Å–∞–º—Ü–æ–≤ (—Ç–∞–∫ –∫–∞–∫ —É –Ω–µ–µ –Ω–µ—Ç «–∂–µ–Ω—Å–∫–æ–π» —Ö—Ä–æ–º–æ—Å–æ–º—ã W).
–ì–∏–±–µ–ª—å —Å–∞–º—Ü–æ–≤ (–∞–Ω–¥—Ä–æ—Ü–∏–¥). –í–æ–ª—å–±–∞—Ö–∏—è –≤—ã–∑—ã–≤–∞–µ—Ç –≥–∏–±–µ–ª—å —ç–º–±—Ä–∏–æ–Ω–æ–≤ –º—É–∂—Å–∫–æ–≥–æ –ø–æ–ª–∞ —É –±–æ–∂—å–∏—Ö –∫–æ—Ä–æ–≤–æ–∫ Adalia bipunctata (Hurst et al., 1999, –ó–∞—Ö–∞—Ä–æ–≤ –∏ –¥—Ä., 2000), –±–∞–±–æ—á–µ–∫ —Ä–æ–¥–æ–≤ Acraea (Jiggins et al., 1998) –∏ Ostrinia, –º—É—Ö Drosophila bifasciata (Hurst et al., 2000) –∏ D. innubila (Dyer, Jaenike, 2004) –∏, –≤–æ–∑–º–æ–∂–Ω–æ, —É –Ω–µ–∫–æ—Ç–æ—Ä—ã—Ö –º—É—Ä–∞–≤—å–µ–≤ (Van Borm et al., 2001). –ì–∏–±–µ–ª—å —Å–∞–º—Ü–æ–≤ –≤—ã–∑—ã–≤–∞–µ—Ç—Å—è —Ü–µ–ª—ã–º —Ä—è–¥–æ–º –¥—Ä—É–≥–∏—Ö –±–∞–∫—Ç–µ—Ä–∏–π (—Ä–∏–∫–∫–µ—Ç—Å–∏—è–º–∏, —ç—Ä–ª–∏—Ö–∏—è–º–∏, —Å–ø–∏—Ä–æ–ø–ª–∞–∑–º–∞–º–∏), –∞ —Ç–∞–∫–∂–µ –ø–∞—Ä–∞–∑–∏—Ç–∏—á–µ—Å–∫–∏–º–∏ –ø—Ä–æ—Å—Ç–µ–π—à–∏–º–∏. –ù–µ –∏—Å–∫–ª—é—á–µ–Ω–æ, —á—Ç–æ –∏–Ω–æ–≥–¥–∞ —á–∞—Å—Ç–∏—á–Ω–∞—è –≥–∏–±–µ–ª—å —Å–∞–º—Ü–æ–≤ –º–æ–∂–µ—Ç –±—ã—Ç—å –≤—ã–≥–æ–¥–Ω–∞ —Å–∞–º–∏–º –Ω–∞—Å–µ–∫–æ–º—ã–º (–ó–∞—Ö–∞—Ä–æ–≤, 1999). –í —Ç–∞–∫–æ–º —Å–ª—É—á–∞–µ –¥–∞–Ω–Ω—ã–π —ç—Ñ—Ñ–µ–∫—Ç –º–æ–∂–µ—Ç –±—ã—Ç—å –≥–µ–Ω–µ—Ç–∏—á–µ—Å–∫–∏ –∑–∞–∫—Ä–µ–ø–ª–µ–Ω —Å–æ —Å—Ç–æ—Ä–æ–Ω—ã —Ö–æ–∑—è–∏–Ω–∞. –•–æ–∑—è–∏–Ω –∫–∞–∫ –±—ã «–ø–µ—Ä–µ–ø–æ—Ä—É—á–∞–µ—Ç» —Ä–µ–≥—É–ª—è—Ü–∏—é —Å–æ–æ—Ç–Ω–æ—à–µ–Ω–∏—è –ø–æ–ª–æ–≤ –≤ —Å–æ–±—Å—Ç–≤–µ–Ω–Ω–æ–π –ø–æ–ø—É–ª—è—Ü–∏–∏ –±–∞–∫—Ç–µ—Ä–∏—è–º-—Å–∏–º–±–∏–æ–Ω—Ç–∞–º. –í–æ–∑–º–æ–∂–Ω–æ, –Ω–∞—Å–µ–∫–æ–º—ã–µ —Ä–µ–∞–≥–∏—Ä—É—é—Ç –≥–∏–±–µ–ª—å—é —Å–∞–º—Ü–æ–≤ –Ω–∞ –∫–∞–∫–∏–µ-—Ç–æ —Ñ–∞–∫—Ç–æ—Ä—ã, –æ–±—â–∏–µ –¥–ª—è –≤–æ–ª—å–±–∞—Ö–∏–∏ –∏ –¥—Ä—É–≥–∏—Ö «—Å–∞–º—Ü–µ—É–±–∏–π—Ü». –í–∞–∂–Ω–æ –æ—Ç–º–µ—Ç–∏—Ç—å, —á—Ç–æ —Å—Ä–µ–¥–∏ –Ω–∞—Å–µ–∫–æ–º—ã—Ö, —É –∫–æ—Ç–æ—Ä—ã—Ö –≤–æ–ª—å–±–∞—Ö–∏—è –≤—ã–∑—ã–≤–∞–µ—Ç –∞–Ω–¥—Ä–æ—Ü–∏–¥, –µ—Å—Ç—å –≤–∏–¥—ã –∫–∞–∫ —Å –≥–µ—Ç–µ—Ä–æ–≥–∞–º–µ—Ç–Ω—ã–º–∏ —Å–∞–º–∫–∞–º–∏ (—Å–∞–º–∫–∏ WZ, —Å–∞–º—Ü—ã ZZ —É –±–∞–±–æ—á–µ–∫), —Ç–∞–∫ –∏ —Å–∞–º—Ü–∞–º–∏ (—Å–∞–º–∫–∏ XX, —Å–∞–º—Ü—ã XY —É –¥—Ä–æ–∑–æ—Ñ–∏–ª –∏ –±–æ–∂—å–∏—Ö –∫–æ—Ä–æ–≤–æ–∫), –∞ —Ç–∞–∫–∂–µ –≥–∞–ø–ª–æ–¥–∏–ø–ª–æ–∏–¥—ã (—Å–∞–º–∫–∏ –•–•, —Å–∞–º—Ü—ã –•0 —É –º—É—Ä–∞–≤—å–µ–≤). –°–ª–µ–¥–æ–≤–∞—Ç–µ–ª—å–Ω–æ, «—Ä–∞—Å–ø–æ–∑–Ω–∞–≤–∞–Ω–∏–µ» —Å–∞–º—Ü–æ–≤ –±–∞–∫—Ç–µ—Ä–∏—è–º–∏ –ø—Ä–æ–∏—Å—Ö–æ–¥–∏—Ç –Ω–µ –ø–æ –Ω–∞–±–æ—Ä—É –ø–æ–ª–æ–≤—ã—Ö —Ö—Ä–æ–º–æ—Å–æ–º, –∞ –∫–∞–∫-—Ç–æ –∏–Ω–∞—á–µ.
–ü–æ–≤—ã—à–µ–Ω–∏–µ –ø–ª–æ–¥–æ–≤–∏—Ç–æ—Å—Ç–∏ –∏ –∂–∏–∑–Ω–µ—Å–ø–æ—Å–æ–±–Ω–æ—Å—Ç–∏. –£ –Ω–µ–∫–æ—Ç–æ—Ä—ã—Ö –Ω–∞—Å–µ–∫–æ–º—ã—Ö –ø–æ—Å–ª–µ –∏–∑–ª–µ—á–µ–Ω–∏—è –æ—Ç –≤–æ–ª—å–±–∞—Ö–∏–∏ –æ—Ç–º–µ—á–∞–µ—Ç—Å—è —Å–Ω–∏–∂–µ–Ω–∏–µ –ø—Ä–æ–¥–æ–ª–∂–∏—Ç–µ–ª—å–Ω–æ—Å—Ç–∏ –∂–∏–∑–Ω–∏, –∞ —Ç–∞–∫–∂–µ –∏–Ω—Ç–µ–≥—Ä–∞–ª—å–Ω–æ–≥–æ –ø–∞—Ä–∞–º–µ—Ç—Ä–∞ «–æ–±—â–µ–π –ø—Ä–∏—Å–ø–æ—Å–æ–±–ª–µ–Ω–Ω–æ—Å—Ç–∏», —É—á–∏—Ç—ã–≤–∞—é—â–µ–≥–æ —Ç–∞–∫–∏–µ –ø–æ–∫–∞–∑–∞—Ç–µ–ª–∏, –∫–∞–∫ –ø–ª–æ–¥–æ–≤–∏—Ç–æ—Å—Ç—å, –∫–æ–Ω–∫—É—Ä–µ–Ω—Ç–æ—Å–ø–æ—Å–æ–±–Ω–æ—Å—Ç—å –ª–∏—á–∏–Ω–æ–∫ –∏ –¥—Ä. –£ –æ—Å—ã Trichogramma bourarachae –µ–¥–∏–Ω—Å—Ç–≤–µ–Ω–Ω—ã–π —ç—Ñ—Ñ–µ–∫—Ç, –ø—Ä–æ–∏–∑–≤–æ–¥–∏–º—ã–π –≤–æ–ª—å–±–∞—Ö–∏–µ–π, — –¥–≤—É–∫—Ä–∞—Ç–Ω–æ–µ —É–≤–µ–ª–∏—á–µ–Ω–∏–µ –ø–ª–æ–¥–æ–≤–∏—Ç–æ—Å—Ç–∏ —Å–∞–º–æ–∫ (Girin, Bouletreau, 1995). –£ –¥—Ä—É–≥–∏—Ö –º—É—Ö –∏ –æ—Å —ç—Ç–æ—Ç —ç—Ñ—Ñ–µ–∫—Ç —Å–æ—á–µ—Ç–∞–µ—Ç—Å—è —Å –¶–ù. –ò–Ω–æ–≥–¥–∞ –≤–æ–ª—å–±–∞—Ö–∏—è –ø–æ–≤—ã—à–∞–µ—Ç –ø–ª–æ–¥–æ–≤–∏—Ç–æ—Å—Ç—å —Å–∞–º—Ü–æ–≤ (Hariri et al., 1998). –£ –æ—Å—ã Asobara tabida, –≤—Å–µ –æ—Å–æ–±–∏ –∫–æ—Ç–æ—Ä–æ–π –∑–∞—Ä–∞–∂–µ–Ω—ã —Å—Ä–∞–∑—É —Ç—Ä–µ–º—è —à—Ç–∞–º–º–∞–º–∏ –≤–æ–ª—å–±–∞—Ö–∏–∏, –æ–¥–∏–Ω –∏–∑ —ç—Ç–∏—Ö —à—Ç–∞–º–º–æ–≤ –∞–±—Å–æ–ª—é—Ç–Ω–æ –Ω–µ–æ–±—Ö–æ–¥–∏–º –¥–ª—è –Ω–æ—Ä–º–∞–ª—å–Ω–æ–≥–æ –æ–æ–≥–µ–Ω–µ–∑–∞, –∞ –¥–≤–∞ –¥—Ä—É–≥–∏—Ö –≤—ã–∑—ã–≤–∞—é—Ç –¶–ù.
–î–ª—è –Ω–µ–º–∞—Ç–æ–¥-—Ñ–∏–ª—è—Ä–∏–π –≤–æ–ª—å–±–∞—Ö–∏—è, –ø–æ-–≤–∏–¥–∏–º–æ–º—É, —è–≤–ª—è–µ—Ç—Å—è –ø–æ–ª–µ–∑–Ω—ã–º —Å–∏–º–±–∏–æ–Ω—Ç–æ–º. –£ –Ω–µ–º–∞—Ç–æ–¥, «–≤—ã–ª–µ—á–µ–Ω–Ω—ã—Ö» –æ—Ç –≤–æ–ª—å–±–∞—Ö–∏–∏ –ø—Ä–∏ –ø–æ–º–æ—â–∏ —Ç–µ—Ç—Ä–∞—Ü–∏–∫–ª–∏–Ω–∞, –Ω–∞–±–ª—é–¥–∞–µ—Ç—Å—è –∑–Ω–∞—á–∏—Ç–µ–ª—å–Ω—ã–π —Ä–æ—Å—Ç —Å–º–µ—Ä—Ç–Ω–æ—Å—Ç–∏ –∏ —Å–Ω–∏–∂–µ–Ω–∏–µ –ø–ª–æ–¥–æ–≤–∏—Ç–æ—Å—Ç–∏. –ü—Ä–∞–≤–¥–∞, —ç—Ç–∏ —ç—Ñ—Ñ–µ–∫—Ç—ã –º–æ–≥—É—Ç –æ–±—ä—è—Å–Ω—è—Ç—å—Å—è –Ω–µ —Ç–æ–ª—å–∫–æ –Ω–µ–æ–±—Ö–æ–¥–∏–º–æ—Å—Ç—å—é –≤–æ–ª—å–±–∞—Ö–∏–∏ –¥–ª—è –Ω–æ—Ä–º–∞–ª—å–Ω–æ–π –∂–∏–∑–Ω–µ–¥–µ—è—Ç–µ–ª—å–Ω–æ—Å—Ç–∏ –Ω–µ–º–∞—Ç–æ–¥, –Ω–æ –∏ —Ç–æ–∫—Å–∏—á–µ—Å–∫–∏–º –¥–µ–π—Å—Ç–≤–∏–µ–º –º–µ—Ç–∞–±–æ–ª–∏—Ç–æ–≤, –æ—Å–≤–æ–±–æ–∂–¥–∞—é—â–∏—Ö—Å—è –ø—Ä–∏ –≥–∏–±–µ–ª–∏ –≤–Ω—É—Ç—Ä–∏–∫–ª–µ—Ç–æ—á–Ω—ã—Ö –±–∞–∫—Ç–µ—Ä–∏–π. –ù–∞–¥–µ–∂–¥—ã —Ä–∞–∑—Ä–∞–±–æ—Ç–∞—Ç—å —ç—Ñ—Ñ–µ–∫—Ç–∏–≤–Ω—É—é –º–µ—Ç–æ–¥–∏–∫—É –ª–µ—á–µ–Ω–∏—è —Ñ–∏–ª—è—Ä–∏–∞—Ç–æ–∑–æ–≤, –æ—Å–Ω–æ–≤–∞–Ω–Ω—É—é –Ω–∞ —É–Ω–∏—á—Ç–æ–∂–µ–Ω–∏–∏ –∞–Ω—Ç–∏–±–∏–æ—Ç–∏–∫–∞–º–∏ —Å–∏–º–±–∏–æ–Ω—Ç–æ–≤ –ø–∞—Ç–æ–≥–µ–Ω–Ω–æ–≥–æ —á–µ—Ä–≤—è, –ø–æ–∫–∞ –Ω–µ –æ–ø—Ä–∞–≤–¥–∞–ª–∏—Å—å, —Ç–∞–∫ –∫–∞–∫ –ø–æ–≥–æ–ª–æ–≤–Ω–æ–π –≥–∏–±–µ–ª–∏ –Ω–µ–º–∞—Ç–æ–¥ –ø—Ä–∏ —ç—Ç–æ–º –Ω–µ –ø—Ä–æ–∏—Å—Ö–æ–¥–∏—Ç (Chirgwin et al., 2003), –æ–¥–Ω–∞–∫–æ –Ω–µ–∫–æ—Ç–æ—Ä—ã–µ —É—Å–ø–µ—Ö–∏ –¥–æ—Å—Ç–∏–≥–Ω—É—Ç—ã (–ú–∞–ª—å—Ü–µ–≤–∞, 2004).
–ü–æ-–≤–∏–¥–∏–º–æ–º—É, —Ä–∞–∑–Ω–æ–æ–±—Ä–∞–∑–Ω—ã–µ —ç—Ñ—Ñ–µ–∫—Ç—ã –≤–æ–ª—å–±–∞—Ö–∏–∏ –±–∞–∑–∏—Ä—É—é—Ç—Å—è –Ω–∞ –µ–¥–∏–Ω–æ–π –º–æ–ª–µ–∫—É–ª—è—Ä–Ω–æ-–≥–µ–Ω–µ—Ç–∏—á–µ—Å–∫–æ–π –æ—Å–Ω–æ–≤–µ –∏ –º–æ–≥—É—Ç —Å—Ä–∞–≤–Ω–∏—Ç–µ–ª—å–Ω–æ –ª–µ–≥–∫–æ –ø–µ—Ä–µ—Ö–æ–¥–∏—Ç—å –æ–¥–∏–Ω –≤ –¥—Ä—É–≥–æ–π. –°—É—â–µ—Å—Ç–≤—É–µ—Ç —Ç–∞–∫–∂–µ –≤–æ–∑–º–æ–∂–Ω–æ—Å—Ç—å —Ñ–∞–≥–æ–≤–æ–≥–æ –ø–µ—Ä–µ–Ω–æ—Å–∞ (—Ç—Ä–∞–Ω—Å–¥—É–∫—Ü–∏–∏) –≥–µ–Ω–æ–≤, –æ—Ç–≤–µ—Ç—Å—Ç–≤–µ–Ω–Ω—ã—Ö –∑–∞ —Ç–µ –∏–ª–∏ –∏–Ω—ã–µ —ç—Ñ—Ñ–µ–∫—Ç—ã, –æ—Ç –æ–¥–Ω–∏—Ö —à—Ç–∞–º–º–æ–≤ –≤–æ–ª—å–±–∞—Ö–∏–∏ –∫ –¥—Ä—É–≥–∏–º. –í–æ–ª—å–±–∞—Ö–∏—è –æ—Ç–ª–∏—á–∞–µ—Ç—Å—è –æ—Ç –¥—Ä—É–≥–∏—Ö –≤–Ω—É—Ç—Ä–∏–∫–ª–µ—Ç–æ—á–Ω—ã—Ö –±–∞–∫—Ç–µ—Ä–∏–π –≤—ã—Å–æ–∫–æ–π –∑–∞—Ä–∞–∂–µ–Ω–Ω–æ—Å—Ç—å—é —Ñ–∞–≥–∞–º–∏, –∫–æ—Ç–æ—Ä—ã–µ —Å—Ä–∞–≤–Ω–∏—Ç–µ–ª—å–Ω–æ —á–∞—Å—Ç–æ –æ—Å—É—â–µ—Å—Ç–≤–ª—è—é—Ç –≥–æ—Ä–∏–∑–æ–Ω—Ç–∞–ª—å–Ω—ã–µ –ø–µ—Ä–µ—Ö–æ–¥—ã –º–µ–∂–¥—É —à—Ç–∞–º–º–∞–º–∏ –±–∞–∫—Ç–µ—Ä–∏–∏ (Bordenstein, Wernegreen, 2004; Gavotte et al., 2004).
–ú–æ–±–∏–ª—å–Ω—ã–µ –≥–µ–Ω–µ—Ç–∏—á–µ—Å–∫–∏–µ —ç–ª–µ–º–µ–Ω—Ç—ã –∏ —ç–≤–æ–ª—é—Ü–∏—è –≤–æ–ª—å–±–∞—Ö–∏–∏. –ì–µ–Ω–æ–º –≤–æ–ª—å–±–∞—Ö–∏–∏ –Ω–µ–≤–µ–ª–∏–∫ –ø–æ —Ä–∞–∑–º–µ—Ä—É –∏ —Å–∏–ª—å–Ω–æ —É–ø—Ä–æ—â–µ–Ω, —á—Ç–æ —Ö–∞—Ä–∞–∫—Ç–µ—Ä–Ω–æ –∫–∞–∫ –¥–ª—è –±–∞–∫—Ç–µ—Ä–∏–π — –≤–Ω—É—Ç—Ä–∏–∫–ª–µ—Ç–æ—á–Ω—ã—Ö –ø–∞—Ä–∞–∑–∏—Ç–æ–≤, —Ç–∞–∫ –∏ –¥–ª—è –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π (Schneider, Ebert, 2004). –ü—Ä–∏ —ç—Ç–æ–º, –æ–¥–Ω–∞–∫–æ, —É –≤–æ–ª—å–±–∞—Ö–∏–∏ –æ–±–Ω–∞—Ä—É–∂–µ–Ω–æ –Ω–µ–æ–±—ã—á–∞–π–Ω–æ –±–æ–ª—å—à–æ–µ –∫–æ–ª–∏—á–µ—Å—Ç–≤–æ –ø–æ–≤—Ç–æ—Ä—è—é—â–∏—Ö—Å—è –ø–æ—Å–ª–µ–¥–æ–≤–∞—Ç–µ–ª—å–Ω–æ—Å—Ç–µ–π –∏ –º–æ–±–∏–ª—å–Ω—ã—Ö –≥–µ–Ω–µ—Ç–∏—á–µ—Å–∫–∏—Ö —ç–ª–µ–º–µ–Ω—Ç–æ–≤ (–ú–ì–≠). –≠—Ç–æ —É–Ω–∏–∫–∞–ª—å–Ω–∞—è –æ—Å–æ–±–µ–Ω–Ω–æ—Å—Ç—å –≤–æ–ª—å–±–∞—Ö–∏–∏, –æ—Ç–ª–∏—á–∞—é—â–∞—è –µ–µ –Ω–µ —Ç–æ–ª—å–∫–æ –æ—Ç –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π, –Ω–æ –∏ –æ—Ç –≤—Å–µ—Ö –æ—Å—Ç–∞–ª—å–Ω—ã—Ö –≤–Ω—É—Ç—Ä–∏–∫–ª–µ—Ç–æ—á–Ω—ã—Ö –±–∞–∫—Ç–µ—Ä–∏–π. –ì–µ–Ω–æ–º –≤–æ–ª—å–±–∞—Ö–∏–∏ –Ω–µ—Å–µ—Ç —Å–ª–µ–¥—ã –º–Ω–æ–≥–æ—á–∏—Å–ª–µ–Ω–Ω—ã—Ö –∏ —á–∞—Å—Ç—ã—Ö —Ä–µ–æ—Ä–≥–∞–Ω–∏–∑–∞—Ü–∏–π, —Å–≤—è–∑–∞–Ω–Ω—ã—Ö —Å –ø–µ—Ä–µ–º–µ—â–µ–Ω–∏—è–º–∏ –ú–ì–≠. –°—É–¥—è –ø–æ –≤—Å–µ–º—É, –º–æ–±–∏–ª—å–Ω—ã–µ —ç–ª–µ–º–µ–Ω—Ç—ã –∏–≥—Ä–∞–ª–∏ –≤–∞–∂–Ω—É—é —Ä–æ–ª—å –≤ —ç–≤–æ–ª—é—Ü–∏–∏ –≤–æ–ª—å–±–∞—Ö–∏–∏ (Wu et al., 2004). –í–æ–∑–º–æ–∂–Ω–æ, –º–Ω–æ–≥–æ—á–∏—Å–ª–µ–Ω–Ω—ã–µ –ú–ì–≠ –ø–æ–∑–≤–æ–ª—è—é—Ç –≤–æ–ª—å–±–∞—Ö–∏–∏ —Å–ø—Ä–∞–≤–ª—è—Ç—å—Å—è —Å —ç–≤–æ–ª—é—Ü–∏–æ–Ω–Ω—ã–º–∏ –∫—Ä–∏–∑–∏—Å–∞–º–∏, –≤–æ–∑–Ω–∏–∫–∞—é—â–∏–º–∏ –≤ –µ–µ «—Å—Ä–µ–¥–µ –æ–±–∏—Ç–∞–Ω–∏—è» –∏–∑-–∑–∞ –±—ã—Å—Ç—Ä—ã—Ö —ç–≤–æ–ª—é—Ü–∏–æ–Ω–Ω—ã—Ö —Å–∫–∞—á–∫–æ–≤, —Å–æ–≤–µ—Ä—à–∞–µ–º—ã—Ö —Ö–æ–∑—è–µ–≤–∞–º–∏, –Ω–∞–ø—Ä–∏–º–µ—Ä, –¥—Ä–æ–∑–æ—Ñ–∏–ª–∞–º–∏, —É –∫–æ—Ç–æ—Ä—ã—Ö —Å—Ç—Ä–µ—Å—Å –º–æ–∂–µ—Ç –≤—ã–∑—ã–≤–∞—Ç—å –∞–∫—Ç–∏–≤–∏–∑–∞—Ü–∏—é –∏—Ö —Å–æ–±—Å—Ç–≤–µ–Ω–Ω—ã—Ö –ú–ì–≠ –∏ –≤–∑—Ä—ã–≤–Ω–æ–π –º—É—Ç–∞–≥–µ–Ω–µ–∑ (–Ý–∞—Ç–Ω–µ—Ä, –í–∞—Å–∏–ª—å–µ–≤–∞, 1993; Vasilyeva et al., 1999). –ú–ì–≠ –º–æ–≥—É—Ç —Å–ª—É–∂–∏—Ç—å —Å–≤–æ–µ–≥–æ —Ä–æ–¥–∞ «—Ä–µ—Ü–µ–ø—Ç–æ—Ä–∞–º–∏ –≤–Ω–µ—à–Ω–∏—Ö —Å—Ç—Ä–µ—Å—Å–∏—Ä—É—é—â–∏—Ö —Å–∏–≥–Ω–∞–ª–æ–≤, –∏–Ω–∏—Ü–∏–∏—Ä—É—é—â–∏—Ö –≤—Å–ø—ã—à–∫–∏ —Ç—Ä–∞–Ω—Å–ø–æ–∑–∏—Ü–∏–æ–Ω–Ω–æ–π –∏–∑–º–µ–Ω—á–∏–≤–æ—Å—Ç–∏ –≤ –∫—Ä–∏—Ç–∏—á–µ—Å–∫–∏–µ –ø–µ—Ä–∏–æ–¥—ã —ç–≤–æ–ª—é—Ü–∏–∏ –ø–æ–ø—É–ª—è—Ü–∏–π» (–Ý–∞—Ç–Ω–µ—Ä, –í–∞—Å–∏–ª—å–µ–≤–∞, 1993, —Å. 57). –í–æ–∑–º–æ–∂–Ω–æ, –æ–±–∏–ª–∏–µ –∞–∫—Ç–∏–≤–Ω—ã—Ö –ú–ì–≠ —è–≤–ª—è–µ—Ç—Å—è –æ–¥–Ω–∏–º –∏–∑ —Ñ–∞–∫—Ç–æ—Ä–æ–≤, –æ–±–µ—Å–ø–µ—á–∏–≤–∞—é—â–∏—Ö –≤–æ–ª—å–±–∞—Ö–∏–∏ –µ–µ –Ω–µ–æ–±—ã—á–∞–π–Ω—É—é —ç–≤–æ–ª—é—Ü–∏–æ–Ω–Ω—É—é –ø–ª–∞—Å—Ç–∏—á–Ω–æ—Å—Ç—å.
–í–æ–ª—å–±–∞—Ö–∏—è –∏ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏
–Ý–∞–∑–º–µ—Ä –≥–µ–Ω–æ–º–∞ –∏ –ø—Ä–æ—Ç–µ–æ–º–∞. –ü–æ —Å—Ä–∞–≤–Ω–µ–Ω–∏—é —Å–æ —Å–≤–æ–±–æ–¥–Ω–æ–∂–∏–≤—É—â–∏–º–∏ –±–∞–∫—Ç–µ—Ä–∏—è–º–∏ —Ä–∞–∑–º–µ—Ä –≥–µ–Ω–æ–º–∞ –≤–æ–ª—å–±–∞—Ö–∏–∏ –Ω–µ–≤–µ–ª–∏–∫ — 1268 —Ç.–ø.–æ.; –¥–ª—è —Å—Ä–∞–≤–Ω–µ–Ω–∏—è, –≥–µ–Ω–æ–º E.coli —Å–æ–¥–µ—Ä–∂–∏—Ç 5528 —Ç.–ø.–æ. –í –ø—Ä–µ–¥–µ–ª–∞—Ö –≥—Ä—É–ø–ø—ã –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–π —Ä–∞–∑–º–µ—Ä –≥–µ–Ω–æ–º–∞ –∫–æ–ª–µ–±–ª–µ—Ç—Å—è –æ—Ç 1 –º–ª–Ω. –ø.–æ. (—É —Ä–∏–∫–∫–µ—Ç—Å–∏–π) –¥–æ >9 –º–ª–Ω. –ø.–æ. —É Bradyrhizobium japonicum (Boussau et al., 2004).
–ú–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã–µ –≥–µ–Ω–æ–º—ã —Ä–∞–∑–Ω—ã—Ö —ç–≤–∫–∞—Ä–∏–æ—Ç —Å–∏–ª—å–Ω–æ —Ä–∞–∑–ª–∏—á–∞—é—Ç—Å—è –ø–æ —Ä–∞–∑–º–µ—Ä—É, –Ω–æ –≤ —Ü–µ–ª–æ–º –æ–Ω–∏ –∑–Ω–∞—á–∏—Ç–µ–ª—å–Ω–æ –º–µ–Ω—å—à–µ, —á–µ–º —É –≤–æ–ª—å–±–∞—Ö–∏–∏. –°—Ä–∞–≤–Ω–∏—Ç–µ–ª—å–Ω–æ –±–æ–ª—å—à–∏–µ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã–µ –≥–µ–Ω–æ–º—ã —Ö–∞—Ä–∞–∫—Ç–µ—Ä–Ω—ã –¥–ª—è –≤—ã—Å—à–∏—Ö —Ä–∞—Å—Ç–µ–Ω–∏–π (Nicotiana tabacum — 431 —Ç.–ø.–æ., Beta vulgaris — 369 —Ç.–ø.–æ., Arabidopsis thaliana — 367 —Ç.–ø.–æ, Marchantia polymorpha — 187 —Ç.–ø.–æ.); –∑–Ω–∞—á–∏—Ç–µ–ª—å–Ω–æ –º–µ–Ω—å—à–∏–µ — –¥–ª—è –ø—Ä–æ—Å—Ç–µ–π—à–∏—Ö, –≤–æ–¥–æ—Ä–æ—Å–ª–µ–π –∏ –≥—Ä–∏–±–æ–≤ (Saccharomyces cerevisiae — 86 —Ç.–ø.–æ., Chara vulgaris — 68 —Ç.–ø.–æ., Saprolegnia ferax — 47 —Ç.–ø.–æ., Paramecium aurelia — 40 —Ç.–ø.–æ, Laminaria digitata — 38 —Ç.–ø.–æ.); —Å–∞–º—ã–µ –º–∞–ª–µ–Ω—å–∫–∏–µ — –¥–ª—è Metazoa (Loxodonta africana, Mytilus edulis, Arbacia lixula, Bos taurus, Homo sapiens — 16 — 17 —Ç.–ø.–æ., Brugia malayi — 14 —Ç.–ø.–æ.). –ü–æ –≤—Å–µ–π –≤–∏–¥–∏–º–æ—Å—Ç–∏, —É–≤–µ–ª–∏—á–µ–Ω–∏–µ —Ä–∞–∑–º–µ—Ä–æ–≤ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω–æ–≥–æ –≥–µ–Ω–æ–º–∞ —É –≤—ã—Å—à–∏—Ö —Ä–∞—Å—Ç–µ–Ω–∏–π, –∫–∞–∫ –∏ –µ–≥–æ –∫—Ä–∞–π–Ω–µ–µ —É–º–µ–Ω—å—à–µ–Ω–∏–µ —É –∂–∏–≤–æ—Ç–Ω—ã—Ö, –∏–º–µ—é—Ç –≤—Ç–æ—Ä–∏—á–Ω—ã–π —Ö–∞—Ä–∞–∫—Ç–µ—Ä. –ú–∞—Å—Å–∏—Ä–æ–≤–∞–Ω–Ω—ã–π –ø–µ—Ä–µ–Ω–æ—Å –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã—Ö –≥–µ–Ω–æ–≤ –≤ —è–¥—Ä–æ –∏ —Å–æ–æ—Ç–≤–µ—Ç—Å—Ç–≤—É—é—â–µ–µ —É–ø—Ä–æ—â–µ–Ω–∏–µ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω–æ–≥–æ –≥–µ–Ω–æ–º–∞ –ø—Ä–æ–∏–∑–æ—à–ª–∏, –ø–æ-–≤–∏–¥–∏–º–æ–º—É, —É–∂–µ —É –¥—Ä–µ–≤–Ω–µ–π—à–∏—Ö —ç–≤–∫–∞—Ä–∏–æ—Ç, –ø—Ä–∏—á–µ–º —Ä–∞–∑–º–µ—Ä –≥–µ–Ω–æ–º–∞ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π —É –Ω–∏—Ö, –ø–æ-–≤–∏–¥–∏–º–æ–º—É, –∏–∑–Ω–∞—á–∞–ª—å–Ω–æ —Å—Ç–∞–±–∏–ª–∏–∑–∏—Ä–æ–≤–∞–ª—Å—è –ø—Ä–∏–º–µ—Ä–Ω–æ –Ω–∞ —Ç–æ–º —É—Ä–æ–≤–Ω–µ, –∫–æ—Ç–æ—Ä—ã–π –Ω–∞–±–ª—é–¥–∞–µ—Ç—Å—è —Å–µ–π—á–∞—Å —É –Ω–∏–∑—à–∏—Ö (–æ–¥–Ω–æ–∫–ª–µ—Ç–æ—á–Ω—ã—Ö) —ç–≤–∫–∞—Ä–∏–æ—Ç.
–Ý–∞–∑–º–µ—Ä –ø—Ä–æ—Ç–µ–æ–º–∞ (—á–∏—Å–ª–æ –±–µ–ª–∫–æ–≤) —É –≥–∏–ø–æ—Ç–µ—Ç–∏—á–µ—Å–∫–æ–≥–æ –æ–±—â–µ–≥–æ –ø—Ä–µ–¥–∫–∞ –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–π, –ø–æ –ø–æ—Å–ª–µ–¥–Ω–∏–º –æ—Ü–µ–Ω–∫–∞–º, —Å–æ—Å—Ç–∞–≤–ª—è–ª –æ—Ç 3000 –¥–æ 5000. –ì–µ–Ω–æ–º –≤–æ–ª—å–±–∞—Ö–∏–∏ –∫–æ–¥–∏—Ä—É–µ—Ç –Ω–µ–º–Ω–æ–≥–∏–º –±–æ–ª–µ–µ 1000 –±–µ–ª–∫–æ–≤. –ü–æ-–≤–∏–¥–∏–º–æ–º—É, –∑–Ω–∞—á–∏—Ç–µ–ª—å–Ω–æ–µ —á–∏—Å–ª–æ –≥–µ–Ω–æ–≤ –∏ –±–µ–ª–∫–æ–≤ (2300-3800) –±—ã–ª–æ —É—Ç—Ä–∞—á–µ–Ω–æ –æ–±—â–∏–º –ø—Ä–µ–¥–∫–æ–º –≤–æ–ª—å–±–∞—Ö–∏–∏ –∏ —Ä–∏–∫–∫–µ—Ç—Å–∏–π –≤ —Ä–µ–∑—É–ª—å—Ç–∞—Ç–µ –ø–µ—Ä–µ—Ö–æ–¥–∞ –∫ –≤–Ω—É—Ç—Ä–∏–∫–ª–µ—Ç–æ—á–Ω–æ–º—É –ø–∞—Ä–∞–∑–∏—Ç–∏–∑–º—É; –ø–æ—Å–ª–µ —Ä–∞–∑–¥–µ–ª–µ–Ω–∏—è –ª–∏–Ω–∏–π –≤–æ–ª—å–±–∞—Ö–∏–∏ –∏ —Ä–∏–∫–∫–µ—Ç—Å–∏–π –ø–µ—Ä–≤–∞—è –∏–∑ —ç—Ç–∏—Ö –ª–∏–Ω–∏–π —É—Ç—Ä–∞—Ç–∏–ª–∞ –µ—â–µ 200-700 –±–µ–ª–∫–æ–≤ (Boussau et al., 2004).
–£ —ç–≤–∫–∞—Ä–∏–æ—Ç —á–∏—Å–ª–æ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã—Ö –±–µ–ª–∫–æ–≤ –æ–±—ã—á–Ω–æ –º–µ–Ω—å—à–µ, –Ω–æ –Ω–µ –Ω–∞–º–Ω–æ–≥–æ. –í —Ä–µ–∫–æ–Ω—Å—Ç—Ä—É–∏—Ä–æ–≤–∞–Ω–Ω–æ–º –ø—Ä–æ—Ç–µ–æ–º–µ «–ø—Ä–æ—Ç–æ–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏» –º–∏–Ω–∏–º–∞–ª—å–Ω–æ–µ —á–∏—Å–ª–æ –±–µ–ª–∫–æ–≤ — 630 (Gabaldon, Huynen, 2003). –í–∞–∂–Ω–µ–π—à–µ–µ –æ—Ç–ª–∏—á–∏–µ —Å–æ—Å—Ç–æ–∏—Ç –≤ —Ç–æ–º, —á—Ç–æ –ø–æ–¥–∞–≤–ª—è—é—â–µ–µ –±–æ–ª—å—à–∏–Ω—Å—Ç–≤–æ –ø–æ—Å–ª–µ–¥–Ω–∏—Ö –∫–æ–¥–∏—Ä—É–µ—Ç—Å—è —è–¥–µ—Ä–Ω—ã–º–∏ –≥–µ–Ω–∞–º–∏. –¢–∞–∫, —É –≥—Ä–∏–±–∞ S. cerevisae –ª–∏—à—å 8 –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã—Ö –±–µ–ª–∫–æ–≤ –∫–æ–¥–∏—Ä—É–µ—Ç—Å—è –º—Ç–î–ù–ö, —É —á–µ–ª–æ–≤–µ–∫–∞ — 13, —É A. thaliana — 25, —É –∂–≥—É—Ç–∏–∫–æ–Ω–æ—Å—Ü–∞ Reclinomonas americana — 64. –í—Å–µ –æ—Å—Ç–∞–ª—å–Ω—ã–µ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã–µ –±–µ–ª–∫–∏ (—Å–≤—ã—à–µ 600) –∫–æ–¥–∏—Ä—É—é—Ç—Å—è —è–¥–µ—Ä–Ω—ã–º–∏ –≥–µ–Ω–∞–º–∏ (Karlberg, 2004; Reichert, Neupert, 2004). –í—Å–µ –±–µ–ª–∫–∏ –≤–æ–ª—å–±–∞—Ö–∏–∏, –µ—Å—Ç–µ—Å—Ç–≤–µ–Ω–Ω–æ, –∫–æ–¥–∏—Ä—É—é—Ç—Å—è –µ–µ —Å–æ–±—Å—Ç–≤–µ–Ω–Ω—ã–º –≥–µ–Ω–æ–º–æ–º; —Ñ–∞–∫—Ç—ã, —Å–≤–∏–¥–µ—Ç–µ–ª—å—Å—Ç–≤—É—é—â–∏–µ –æ —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–∏—Ä–æ–≤–∫–µ –∫–∞–∫–∏—Ö-–ª–∏–±–æ –±–µ–ª–∫–æ–≤ —Ö–æ–∑—è–∏–Ω–∞ –≤ –±–∞–∫—Ç–µ—Ä–∏—é, –Ω–µ –∏–∑–≤–µ—Å—Ç–Ω—ã.
–û–±–æ–ª–æ—á–∫–∞. –í–∞–∂–Ω–µ–π—à—É—é —Ä–æ–ª—å –≤–æ –≤–∑–∞–∏–º–æ–æ—Ç–Ω–æ—à–µ–Ω–∏—è—Ö —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–Ω—Ç–∞ —Å —ç–≤–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–æ–π –∫–ª–µ—Ç–∫–æ–π –∏–≥—Ä–∞–µ—Ç –µ–≥–æ –Ω–∞—Ä—É–∂–Ω–∞—è –æ–±–æ–ª–æ—á–∫–∞, –æ—Ç —Å–≤–æ–π—Å—Ç–≤ –∫–æ—Ç–æ—Ä–æ–π –∑–∞–≤–∏—Å–∏—Ç –ø—Ä–æ–∏—Å—Ö–æ–¥—è—â–∏–π –º–µ–∂–¥—É –¥–≤—É–º—è –æ—Ä–≥–∞–Ω–∏–∑–º–∞–º–∏ –æ–±–º–µ–Ω –≤–µ—â–µ—Å—Ç–≤–æ–º –∏ –∏–Ω—Ñ–æ—Ä–º–∞—Ü–∏–µ–π.
–í–æ–ª—å–±–∞—Ö–∏–∏, –∂–∏–≤—É—â–∏–µ –≤ —Ü–∏—Ç–æ–ø–ª–∞–∑–º–µ —Ö–æ–∑—è–∏–Ω–∞, –æ–∫—Ä—É–∂–µ–Ω—ã –¥–≤–æ–π–Ω–æ–π –º–µ–±—Ä–∞–Ω–æ–π — —Ç–∞–∫ –∂–µ, –∫–∞–∫ –∏ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏. –í–Ω—É—Ç—Ä–µ–Ω–Ω—è—è –º–µ–º–±—Ä–∞–Ω–∞ «–ø—Ä–∏–Ω–∞–¥–ª–µ–∂–∏—Ç» —Å–∞–º–æ–π –≤–æ–ª—å–±–∞—Ö–∏–∏, –Ω–∞—Ä—É–∂–Ω–∞—è —è–≤–ª—è–µ—Ç—Å—è –ø—Ä–æ–¥—É–∫—Ç–æ–º –∫–ª–µ—Ç–∫–∏ —Ö–æ–∑—è–∏–Ω–∞. –ü—Ä–µ–¥–ø–æ–ª–∞–≥–∞–µ—Ç—Å—è, —á—Ç–æ –¥–≤–æ–π–Ω–∞—è –º–µ–º–±—Ä–∞–Ω–∞ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π –∏–º–µ–µ—Ç —Ç–∞–∫–æ–µ –∂–µ «–¥–≤–æ–π–Ω–æ–µ» –ø—Ä–æ–∏—Å—Ö–æ–∂–¥–µ–Ω–∏–µ.
–°–≤–æ–±–æ–¥–Ω–æ–∂–∏–≤—É—â–∏–µ –≥—Ä–∞–º–æ—Ç—Ä–∏—Ü–∞—Ç–µ–ª—å–Ω—ã–µ –±–∞–∫—Ç–µ—Ä–∏–∏ (–∫ –∫–æ—Ç–æ—Ä—ã–º –æ—Ç–Ω–æ—Å—è—Ç—Å—è –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–∏) –æ–±—ã—á–Ω–æ –∏–º–µ—é—Ç —Å–ª–æ–∂–Ω—É—é –æ–±–æ–ª–æ—á–∫—É (–∫–ª–µ—Ç–æ—á–Ω—É—é —Å—Ç–µ–Ω–∫—É), —Å–æ—Å—Ç–æ—è—â—É—é –∏–∑ —Ç—Ä–µ—Ö —Å–ª–æ–µ–≤: –≤–Ω—É—Ç—Ä–µ–Ω–Ω–µ–π —Ü–∏—Ç–æ–ø–ª–∞–∑–º–∞—Ç–∏—á–µ—Å–∫–æ–π –º–µ–º–±—Ä–∞–Ω—ã, –ø–µ—Ä–∏–ø–ª–∞–∑–º–∞—Ç–∏—á–µ—Å–∫–æ–≥–æ –ø—Ä–æ—Å—Ç—Ä–∞–Ω—Å—Ç–≤–∞, —Å–æ–¥–µ—Ä–∂–∞—â–µ–≥–æ –ø–µ–ø—Ç–∏–¥–æ–≥–ª–∏–∫–∞–Ω, –∏ –Ω–∞—Ä—É–∂–Ω–æ–π –º–µ–º–±—Ä–∞–Ω—ã, –æ—Ç–ª–∏—á–∞—é—â–µ–π—Å—è –ø–æ —Å–≤–æ–µ–º—É —Å—Ç—Ä–æ–µ–Ω–∏—é –æ—Ç —Ü–∏—Ç–æ–ø–ª–∞–∑–º–∞—Ç–∏—á–µ—Å–∫–æ–π –∏ —Å–æ–¥–µ—Ä–∂–∞—â–µ–π –ª–∏–ø–æ–ø–æ–ª–∏—Å–∞—Ö–∞—Ä–∏–¥—ã. –ü—Ä–µ–¥–∫–∏ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π, —Å—Ç–∞–≤ –æ–±–ª–∏–≥–∞—Ç–Ω—ã–º–∏ —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–Ω—Ç–∞–º–∏, —É—Ç—Ä–∞—Ç–∏–ª–∏ –Ω–∞—Ä—É–∂–Ω—ã–µ —Å–ª–æ–∏ —Å–≤–æ–µ–π –æ–±–æ–ª–æ—á–∫–∏, —Å–æ—Ö—Ä–∞–Ω–∏–≤ —Ç–æ–ª—å–∫–æ –≤–Ω—É—Ç—Ä–µ–Ω–Ω—é—é –º–µ–º–±—Ä–∞–Ω—É, –∞ –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º–∞ –æ–±—Ä–∞–∑–æ–≤–∞–ª–∞ –Ω–∞—Ä—É–∂–Ω—É—é –º–µ–º–±—Ä–∞–Ω—É –Ω–æ–≤–æ–ø—Ä–∏–æ–±—Ä–µ—Ç–µ–Ω–Ω—ã—Ö –æ—Ä–≥–∞–Ω–µ–ª–ª.
–í–æ–ª—å–±–∞—Ö–∏–∏ –∏ –∏—Ö –ø—Ä–µ–¥–∫–∏ —è–≤–ª—è—é—Ç—Å—è –æ–±–ª–∏–≥–∞—Ç–Ω—ã–º–∏ —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–Ω—Ç–∞–º–∏ –∏–ª–∏ –ø–∞—Ä–∞–∑–∏—Ç–∞–º–∏ —É–∂–µ –≤ —Ç–µ—á–µ–Ω–∏–µ —Å–æ—Ç–µ–Ω –º–∏–ª–ª–∏–æ–Ω–æ–≤ –ª–µ—Ç –∏ –∑–∞ —ç—Ç–æ –≤—Ä–µ–º—è —É—Ç—Ä–∞—Ç–∏–ª–∏ –º–Ω–æ–≥–∏–µ –≥–µ–Ω—ã, –Ω–µ–æ–±—Ö–æ–¥–∏–º—ã–µ –¥–ª—è —Å–∏–Ω—Ç–µ–∑–∞ –Ω–æ—Ä–º–∞–ª—å–Ω–æ–π –∫–ª–µ—Ç–æ—á–Ω–æ–π —Å—Ç–µ–Ω–∫–∏. –í —á–∞—Å—Ç–Ω–æ—Å—Ç–∏, –ø–æ—á—Ç–∏ –ø–æ–ª–Ω–æ—Å—Ç—å—é —É—Ç—Ä–∞—á–µ–Ω–∞ —Å–∏—Å—Ç–µ–º–∞ —Å–∏–Ω—Ç–µ–∑–∞ –ª–∏–ø–æ–ø–æ–ª–∏—Å–∞—Ö–∞—Ä–∏–¥–æ–≤. –ü—Ä–µ–¥–ø–æ–ª–∞–≥–∞–µ—Ç—Å—è, —á—Ç–æ –æ–Ω–∞ –ø–µ—Ä–µ—Å—Ç–∞–ª–∞ —Ñ—É–Ω–∫—Ü–∏–æ–Ω–∏—Ä–æ–≤–∞—Ç—å –µ—â–µ —É –æ–±—â–µ–≥–æ –ø—Ä–µ–¥–∫–∞ –≤–æ–ª—å–±–∞—Ö–∏–∏ –∏ –µ–µ –±–ª–∏–∂–∞–π—à–∏—Ö —Ä–æ–¥—Å—Ç–≤–µ–Ω–Ω–∏–∫–æ–≤ — –≤–Ω—É—Ç—Ä–∏–∫–ª–µ—Ç–æ—á–Ω—ã—Ö –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–π —ç—Ä–ª–∏—Ö–∏–∏ –∏ –∞–Ω–∞–ø–ª–∞–∑–º—ã (Wu et al., 2004). –í–º–µ—Å—Ç–æ —Å–æ–±—Å—Ç–≤–µ–Ω–Ω–æ–π –Ω–∞—Ä—É–∂–Ω–æ–π –º–µ–º–±—Ä–∞–Ω—ã, –¥–ª—è –æ–±—Ä–∞–∑–æ–≤–∞–Ω–∏—è –∫–æ—Ç–æ—Ä–æ–π –Ω–µ–æ–±—Ö–æ–¥–∏–º—ã –ª–∏–ø–æ–ø–æ–ª–∏—Å–∞—Ö–∞—Ä–∏–¥—ã, —ç—Ç–∏ –±–∞–∫—Ç–µ—Ä–∏–∏ «–ø–æ–ª—å–∑—É—é—Ç—Å—è» –Ω–∞—Ä—É–∂–Ω–æ–π –º–µ–º–±—Ä–∞–Ω–æ–π, –ø—Ä–µ–¥–æ—Å—Ç–∞–≤–ª—è–µ–º–æ–π –∏–º —Ö–æ–∑—è–∏–Ω–æ–º.
–û–¥–Ω–∞–∫–æ, –≤ –æ—Ç–ª–∏—á–∏–µ –æ—Ç –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π, —É –≤–æ–ª—å–±–∞—Ö–∏–∏ —Å–æ—Ö—Ä–∞–Ω—è–µ—Ç—Å—è —Å—Ä–µ–¥–Ω–∏–π —Å–ª–æ–π –∫–ª–µ—Ç–æ—á–Ω–æ–π —Å—Ç–µ–Ω–∫–∏, —Å–æ–¥–µ—Ä–∂–∞—â–∏–π –ø–µ–ø—Ç–∏–¥–æ–≥–ª–∏–∫–∞–Ω. –í –µ–µ –≥–µ–Ω–æ–º–µ –ø—Ä–∏—Å—É—Ç—Å—Ç–≤—É—é—Ç –≥–µ–Ω—ã, —É—á–∞—Å—Ç–≤—É—é—â–∏–µ –≤ –º–µ—Ç–∞–±–æ–ª–∏–∑–º–µ –∫–æ–º–ø–æ–Ω–µ–Ω—Ç–æ–≤ —ç—Ç–æ–≥–æ —Å–ª–æ—è (D-–∞–ª–∞–Ω–∏–Ω-D-–∞–ª–∞–Ω–∏–Ω –ª–∏–≥–∞–∑–∞, D-–∞–ª–∞–Ω–∏–ª-D-–∞–ª–∞–Ω–∏–Ω –∫–∞—Ä–±–æ–∫—Å–∏–ø–µ–ø—Ç–∏–¥–∞–∑–∞, –£–î–§-N-–∞—Ü–µ—Ç–∏–ª–º—É—Ä–∞–º–∞—Ç-–∞–ª–∞–Ω–∏–Ω –ª–∏–≥–∞–∑–∞, N-–∞—Ü–µ—Ç–∏–ª–º—É—Ä–∞–º–æ–∏–ª-L-–∞–ª–∞–Ω–∏–Ω –∞–º–∏–¥–∞–∑–∞, —Ñ–æ—Å—Ñ–æ-N-–∞—Ü–µ—Ç–∏–ª–º—É—Ä–∞–º–æ–∏–ª-–ø–µ–Ω—Ç–∞–ø–µ–ø—Ç–∏–¥ —Ç—Ä–∞–Ω—Å—Ñ–µ—Ä–∞–∑–∞ –∏ –¥—Ä.). –¢–∞–∫–∏–º –æ–±—Ä–∞–∑–æ–º, –∑–∞–º–µ—Ç–Ω–æ–≥–æ —Å—Ö–æ–¥—Å—Ç–≤–∞ –≤ —Å—Ç—Ä–æ–µ–Ω–∏–∏ —Å—Ä–µ–¥–Ω–µ–≥–æ —Å–ª–æ—è –æ–±–æ–ª–æ—á–∫–∏ –≤–æ–ª—å–±–∞—Ö–∏–∏ —Å –º–µ–∂–º–µ–º–±—Ä–∞–Ω–Ω—ã–º –ø—Ä–æ—Å—Ç—Ä–∞–Ω—Å—Ç–≤–æ–º –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π –Ω–µ –Ω–∞–±–ª—é–¥–∞–µ—Ç—Å—è.
–ú–µ—Ç–∞–±–æ–ª–∏–∑–º –∏ —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç. –ë—É–¥—É—á–∏ –∞—ç—Ä–æ–±–Ω–æ–π –±–∞–∫—Ç–µ—Ä–∏–µ–π, –æ—á–µ–Ω—å –±–ª–∏–∑–∫–æ–π –ø–æ —Å—Ç—Ä–æ–µ–Ω–∏—é –±–∞–∑–æ–≤—ã—Ö —Å–∏—Å—Ç–µ–º —ç–Ω–µ—Ä–≥–µ—Ç–∏—á–µ—Å–∫–æ–≥–æ –º–µ—Ç–∞–±–æ–ª–∏–∑–º–∞ –∫ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º, –≤–æ–ª—å–±–∞—Ö–∏—è, –∫–∞–∑–∞–ª–æ—Å—å –±—ã, –º–æ–≥–ª–∞ —Å—Ç–∞—Ç—å –Ω–µ –º–µ–Ω–µ–µ –ø–æ–ª–µ–∑–Ω—ã–º —Å–∏–º–±–∏–æ–Ω—Ç–æ–º. –≠—Ç–æ–≥–æ, –æ–¥–Ω–∞–∫–æ, –Ω–µ –Ω–∞–±–ª—é–¥–∞–µ—Ç—Å—è (—Ç–∞–±–ª. 1). –ú–µ—Ç–∞–±–æ–ª–∏–∑–º –≤–æ–ª—å–±–∞—Ö–∏–∏ –≤ —Ü–µ–ª–æ–º –æ—Ä–≥–∞–Ω–∏–∑–æ–≤–∞–Ω —Ç–∞–∫–∏–º –æ–±—Ä–∞–∑–æ–º, —á—Ç–æ–±—ã –ø—Ä–∏—á–∏–Ω—è—Ç—å —Ö–æ–∑—è–∏–Ω—É –Ω–∞–∏–º–µ–Ω—å—à–∏–π –≤—Ä–µ–¥, –Ω–æ –∏ –≤–∏–¥–∏–º–æ–π –º–µ—Ç–∞–±–æ–ª–∏—Ç–∏—á–µ—Å–∫–æ–π «–ø–æ–ª—å–∑—ã» —ç—Ç–∞ –≤–Ω—É—Ç—Ä–∏–∫–ª–µ—Ç–æ—á–Ω–∞—è –±–∞–∫—Ç–µ—Ä–∏—è –Ω–µ –ø—Ä–∏–Ω–æ—Å–∏—Ç.
–ì–ª–∞–≤–Ω–∞—è —Ñ—É–Ω–∫—Ü–∏—è –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π —Å–æ—Å—Ç–æ–∏—Ç –≤ —Å–∏–Ω—Ç–µ–∑–µ –ê–¢–§ –∑–∞ —Å—á–µ—Ç –∫–∏—Å–ª–æ—Ä–æ–¥–Ω–æ–≥–æ –æ–∫–∏—Å–ª–µ–Ω–∏—è –ø–∏—Ä—É–≤–∞—Ç–∞ — –∫–æ–Ω–µ—á–Ω–æ–≥–æ –ø—Ä–æ–¥—É–∫—Ç–∞ –∏–¥—É—â–µ–≥–æ –≤ —Ü–∏—Ç–æ–ø–ª–∞–∑–º–µ –≥–ª–∏–∫–æ–ª–∏–∑–∞. –ü—Ä–æ–∏–∑–≤–µ–¥–µ–Ω–Ω–∞—è –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º–∏ –ê–¢–§ —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–∏—Ä—É–µ—Ç—Å—è –≤ —Ü–∏—Ç–æ–ø–ª–∞–∑–º—É.
–Ý–æ–¥—Å—Ç–≤–µ–Ω–Ω–∏–∫–∏ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π –∏ –≤–æ–ª—å–±–∞—Ö–∏–π, —Ä–∏–∫–∫–µ—Ç—Å–∏–∏, –≤—ã–∫–∞—á–∏–≤–∞—é—Ç –ê–¢–§ –∏–∑ —Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã —Ö–æ–∑—è–∏–Ω–∞ –≤ –æ–±–º–µ–Ω –Ω–∞ –ê–î–§ –ø—Ä–∏ –ø–æ–º–æ—â–∏ –±–µ–ª–∫–æ–≤ —Å–µ–º–µ–π—Å—Ç–≤–∞ TLC (Andersson et al., 1998). –Ý–∏–∫–∫–µ—Ç—Å–∏–∏, —Ç–∞–∫–∏–º –æ–±—Ä–∞–∑–æ–º, –≤–µ–¥—É—Ç —Å–µ–±—è –∫–∞–∫ –Ω–∞—Å—Ç–æ—è—â–∏–µ «—ç–Ω–µ—Ä–≥–µ—Ç–∏—á–µ—Å–∫–∏–µ –≤–∞–º–ø–∏—Ä—ã» –∏ –ø—Ä–µ–¥—Å—Ç–∞–≤–ª—è—é—Ç –≤ —ç—Ç–æ–º –æ—Ç–Ω–æ—à–µ–Ω–∏–∏ –ø—Ä—è–º—É—é –ø—Ä–æ—Ç–∏–≤–æ–ø–æ–ª–æ–∂–Ω–æ—Å—Ç—å –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º. –í –≥–µ–Ω–æ–º–µ –≤–æ–ª—å–±–∞—Ö–∏–∏ –Ω–µ –æ–±–Ω–∞—Ä—É–∂–µ–Ω—ã –≥–µ–Ω—ã, –æ—Ç–≤–µ—Ç—Å—Ç–≤–µ–Ω–Ω—ã–µ –∑–∞ —Ç–∞–∫–æ–π, —Å –ø–æ–∑–≤–æ–ª–µ–Ω–∏—è —Å–∫–∞–∑–∞—Ç—å, –º–µ–º–±—Ä–∞–Ω–Ω—ã–π —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç –ê–¢–§. –í–æ–ª—å–±–∞—Ö–∏—è, –ø–æ-–≤–∏–¥–∏–º–æ–º—É, –≤–µ–¥–µ—Ç —Å–µ–±—è –±–æ–ª–µ–µ —Å–∫—Ä–æ–º–Ω–æ –∏ –ø—Ä–∏—á–∏–Ω—è–µ—Ç –º–µ–Ω—å—à–∏–π —É—â–µ—Ä–± —Ö–æ–∑—è–∏–Ω—É, –æ–≥—Ä–∞–Ω–∏—á–∏–≤–∞—è—Å—å –≤—ã–∫–∞—á–∏–≤–∞–Ω–∏–µ–º –∏–∑ –µ–≥–æ —Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã –Ω–µ–∫–æ—Ç–æ—Ä—ã—Ö –∞–º–∏–Ω–æ–∫–∏—Å–ª–æ—Ç –∏ —É–≥–ª–µ–≤–æ–¥–æ–≤. –û–¥–Ω–∞–∫–æ –∏ —ç–Ω–µ—Ä–≥–∏–µ–π –≤ –≤–∏–¥–µ –ê–¢–§ –æ–Ω–∞ —Å–≤–æ–µ–≥–æ —Ö–æ–∑—è–∏–Ω–∞, —Ä–∞–∑—É–º–µ–µ—Ç—Å—è, –Ω–µ —Å–Ω–∞–±–∂–∞–µ—Ç.
–•–æ—Ç—è –º–µ—Ç–∞–±–æ–ª–∏–∑–º —É–≥–ª–µ–≤–æ–¥–æ–≤ —É –≤–æ–ª—å–±–∞—Ö–∏–∏ –≤ —Ü–µ–ª–æ–º –æ–≥—Ä–∞–Ω–∏—á–µ–Ω, —É –Ω–µ–µ –≤—Å–µ –∂–µ –ø—Ä–∏—Å—É—Ç—Å—Ç–≤—É–µ—Ç –Ω–µ–æ–±—Ö–æ–¥–∏–º—ã–π –º–∏–Ω–∏–º–∞–ª—å–Ω—ã–π «–∫–æ–º–ø–ª–µ–∫—Ç» –±–µ–ª–∫–æ–≤, –æ–±–µ—Å–ø–µ—á–∏–≤–∞—é—â–∏—Ö –ø–æ–ª–Ω—ã–π —Ü–∏–∫–ª –∫–∞—Ç–∞–±–æ–ª–∏–∑–º–∞ —É–≥–ª–µ–≤–æ–¥–æ–≤ —Å —Ü–µ–ª—å—é –ø–æ–ª—É—á–µ–Ω–∏—è —ç–Ω–µ—Ä–≥–∏–∏. –ì–µ–∫—Å–æ–∑—ã (–≥–ª—é–∫–æ–∑–∞, —Ñ—Ä—É–∫—Ç–æ–∑–∞) —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–∏—Ä—É—é—Ç—Å—è –∏–∑ —Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã —Ö–æ–∑—è–∏–Ω–∞. –í «–∫–æ–º–ø–ª–µ–∫—Ç» –≤—Ö–æ–¥—è—Ç: 1) –º–µ–º–±—Ä–∞–Ω–Ω—ã–π –±–µ–ª–æ–∫, –æ–±–µ—Å–ø–µ—á–∏–≤–∞—é—â–∏–π —Å–æ–ø—Ä—è–∂–µ–Ω–Ω—ã–π —Å —Ñ–æ—Å—Ñ–æ—Ä–∏–ª–∏—Ä–æ–≤–∞–Ω–∏–µ–º —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç –≥–µ–∫—Å–æ–∑ –≤ –∫–ª–µ—Ç–∫—É, 2) –≥–ª–∏–∫–æ–ª–∏–∑, –Ω–∞—á–∏–Ω–∞—é—â–∏–π—Å—è —Å —Ñ—Ä—É–∫—Ç–æ–∑–æ-1,6-–¥–∏—Ñ–æ—Å—Ñ–∞—Ç–∞, 3) –Ω–µ–æ–∫–∏—Å–ª–∏—Ç–µ–ª—å–Ω—ã–π –ø–µ–Ω—Ç–æ–∑–æ—Ñ–æ—Å—Ñ–∞—Ç–Ω—ã–π –ø—É—Ç—å, 4) –ø–æ–ª–Ω—ã–π —Ü–∏–∫–ª —Ç—Ä–∏–∫–∞—Ä–±–æ–Ω–æ–≤—ã—Ö –∫–∏—Å–ª–æ—Ç, 5) –¥—ã—Ö–∞—Ç–µ–ª—å–Ω–∞—è —ç–ª–µ–∫—Ç—Ä–æ–Ω–Ω–æ—Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–Ω–∞—è —Ü–µ–ø—å –æ–∫–∏—Å–ª–∏—Ç–µ–ª—å–Ω–æ–≥–æ —Ñ–æ—Å—Ñ–æ—Ä–∏–ª–∏—Ä–æ–≤–∞–Ω–∏—è.
–ù–∞–ª–∏—á–∏–µ —Å–æ–±—Å—Ç–≤–µ–Ω–Ω—ã—Ö –≥–µ–Ω–æ–≤ –≥–ª–∏–∫–æ–ª–∏–∑–∞ –æ—Ç–ª–∏—á–∞–µ—Ç –≤–æ–ª—å–±–∞—Ö–∏—é –æ—Ç –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π –∏ —Ä–∏–∫–∫–µ—Ç—Å–∏–π (Andersson et al., 1998; Wu et al., 2004) –∏ –ø–æ–∫–∞–∑—ã–≤–∞–µ—Ç, —á—Ç–æ –æ–Ω–∞ –µ—â–µ –≤ –º–µ–Ω—å—à–µ–π —Å—Ç–µ–ø–µ–Ω–∏, —á–µ–º —Ä–∏–∫–∫–µ—Ç—Å–∏—è, «–∫–æ–º–ø–ª–µ–º–µ–Ω—Ç–∞—Ä–Ω–∞» –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º–µ —Å —Ç–æ—á–∫–∏ –∑—Ä–µ–Ω–∏—è –º–µ—Ç–∞–±–æ–ª–∏–∑–º–∞. –í–º–µ—Å—Ç–µ —Å —Ç–µ–º –æ–Ω–∞ –ø–æ—Ç–µ–Ω—Ü–∏–∞–ª—å–Ω–æ –º–µ–Ω–µ–µ –≤—Ä–µ–¥–Ω–∞, –ø–æ—Å–∫–æ–ª—å–∫—É –ø–µ—Ä–µ—Ö–≤–∞—Ç—ã–≤–∞–µ—Ç –º–µ—Ç–∞–±–æ–ª–∏—Ç—ã —É —Ö–æ–∑—è–∏–Ω–∞ –Ω–∞ –±–æ–ª–µ–µ —Ä–∞–Ω–Ω–∏—Ö —ç—Ç–∞–ø–∞—Ö –∏—Ö –±–∏–æ—Ö–∏–º–∏—á–µ—Å–∫–æ–π «–æ–±—Ä–∞–±–æ—Ç–∫–∏» –∏ –±–µ—Ä–µ—Ç –Ω–∞ —Å–µ–±—è –Ω–µ —Ç–æ–ª—å–∫–æ —Å–∞–º—ã–µ —ç–Ω–µ—Ä–≥–µ—Ç–∏—á–µ—Å–∫–∏ –≤—ã–≥–æ–¥–Ω—ã–µ (–∞—ç—Ä–æ–±–Ω—ã–µ) —ç—Ç–∞–ø—ã –∫–∞—Ç–∞–±–æ–ª–∏–∑–º–∞ —É–≥–ª–µ–≤–æ–¥–æ–≤, –Ω–æ –∏ –º–µ–Ω–µ–µ –≤—ã–≥–æ–¥–Ω—ã–µ –∞–Ω–∞—ç—Ä–æ–±–Ω—ã–µ.
–ë–æ–ª—å—à–æ–µ —á–∏—Å–ª–æ —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–µ—Ä–æ–≤ –∞–º–∏–Ω–æ–∫–∏—Å–ª–æ—Ç –ø–æ–∑–≤–æ–ª—è–µ—Ç –ø—Ä–µ–¥–ø–æ–ª–æ–∂–∏—Ç—å, —á—Ç–æ –≤–æ–ª—å–±–∞—Ö–∏–∏ –ø–æ–ª—É—á–∞—é—Ç –∏–∑ –Ω–∏—Ö –∑–Ω–∞—á–∏—Ç–µ–ª—å–Ω—É—é —á–∞—Å—Ç—å —ç–Ω–µ—Ä–≥–∏–∏; –∫—Ä–æ–º–µ —Ç–æ–≥–æ, —ç—Ç–æ –ø–æ–∑–≤–æ–ª—è–µ—Ç –≤–æ–ª—å–±–∞—Ö–∏–∏ –æ–±—Ö–æ–¥–∏—Ç—å—Å—è –±–µ–∑ –º–Ω–æ–≥–∏—Ö —Ñ–µ—Ä–º–µ–Ω—Ç–æ–≤ –∞–º–∏–Ω–æ–∫–∏—Å–ª–æ—Ç–Ω–æ–≥–æ –º–µ—Ç–∞–±–æ–ª–∏–∑–º–∞. –¢–∞ –∂–µ —á–µ—Ä—Ç–∞ — –Ω–∞–ª–∏—á–∏–µ –∞–º–∏–Ω–æ–∫–∏—Å–ª–æ—Ç–Ω—ã—Ö —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–µ—Ä–æ–≤ –∏ –∫—Ä–∞–π–Ω–µ –Ω–µ–ø–æ–ª–Ω—ã–π –Ω–∞–±–æ—Ä —Ñ–µ—Ä–º–µ–Ω—Ç–æ–≤ –∞–º–∏–Ω–æ–∫–∏—Å–ª–æ—Ç–Ω–æ–≥–æ –º–µ—Ç–∞–±–æ–ª–∏–∑–º–∞ — —Ö–∞—Ä–∞–∫—Ç–µ—Ä–Ω–∞ –∏ –¥–ª—è —Ä–µ–∫–æ–Ω—Å—Ç—Ä—É–∏—Ä–æ–≤–∞–Ω–Ω–æ–π «–ø—Ä–æ—Ç–æ–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏» — –≥–∏–ø–æ—Ç–µ—Ç–∏—á–µ—Å–∫–æ–≥–æ –ø—Ä–µ–¥–∫–∞ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π (Gabaldon, Huynen, 2003), –∏ –¥–ª—è —Ä–∏–∫–∫–µ—Ç—Å–∏–π.
–ü–æ–º–∏–º–æ –≥–ª–∏–∫–æ–ª–∏–∑–∞, –≤–æ–ª—å–±–∞—Ö–∏—è —Ä–∞—Å–ø–æ–ª–∞–≥–∞–µ—Ç –µ—â–µ –Ω–µ—Å–∫–æ–ª—å–∫–∏–º–∏ –º–µ—Ç–∞–±–æ–ª–∏—á–µ—Å–∫–∏–º–∏ –ø—É—Ç—è–º–∏, –æ—Ç—Å—É—Ç—Å—Ç–≤—É—é—â–∏–º–∏ —É —Ä–∏–∫–∫–µ—Ç—Å–∏–∏ (–≤ —Ç–æ–º —á–∏—Å–ª–µ —Å–∏–Ω—Ç–µ–∑ –Ω—É–∫–ª–µ–æ—Ç–∏–¥-–º–æ–Ω–æ—Ñ–æ—Å—Ñ–∞—Ç–æ–≤, —Ä–∏–±–æ—Ñ–ª–∞–≤–∏–Ω–∞, –¥–µ–≥—Ä–∞–¥–∞—Ü–∏—è —Ç—Ä–µ–æ–Ω–∏–Ω–∞, –º–µ—Ç–∞–±–æ–ª–∏–∑–º –ø–∏—Ä–∏–º–∏–¥–∏–Ω–æ–≤ –∏ –¥—Ä.). –í–æ–∑–º–æ–∂–Ω–æ, –Ω–µ—Å–∫–æ–ª—å–∫–æ –±–æ–ª—å—à–∞—è –±–∏–æ—Ö–∏–º–∏—á–µ—Å–∫–∞—è —Å–∞–º–æ–¥–æ—Å—Ç–∞—Ç–æ—á–Ω–æ—Å—Ç—å –≤–æ–ª—å–±–∞—Ö–∏–∏ –ø–æ —Å—Ä–∞–≤–Ω–µ–Ω–∏—é —Å —Ä–∏–∫–∫–µ—Ç—Å–∏–µ–π —è–≤–ª—è–µ—Ç—Å—è –æ–¥–Ω–æ–π –∏–∑ –ø—Ä–µ–¥–ø–æ—Å—ã–ª–æ–∫ –±–æ–ª—å—à–µ–π —ç–≤–æ–ª—é—Ü–∏–æ–Ω–Ω–æ–π –ø–ª–∞—Å—Ç–∏—á–Ω–æ—Å—Ç–∏ –≤ —Å–º—ã—Å–ª–µ –≤—ã—Ä–∞–±–æ—Ç–∫–∏ —Ä–∞–∑–ª–∏—á–Ω—ã—Ö —Å—Ä–µ–¥—Å—Ç–≤ –≤–æ–∑–¥–µ–π—Å—Ç–≤–∏—è –Ω–∞ —Ö–æ–∑—è–∏–Ω–∞. –í —Ü–µ–ª–æ–º –º–µ—Ç–∞–±–æ–ª–∏—á–µ—Å–∫–∏–µ —Å–∏—Å—Ç–µ–º—ã –≤–æ–ª—å–±–∞—Ö–∏–∏ —Ä–µ–¥—É—Ü–∏—Ä–æ–≤–∞–Ω—ã –≤ –∑–Ω–∞—á–∏—Ç–µ–ª—å–Ω–æ –º–µ–Ω—å—à–µ–π —Å—Ç–µ–ø–µ–Ω–∏, —á–µ–º —É —Ä–∏–∫–∫–µ—Ç—Å–∏–∏, –∏ —Å–æ—Ö—Ä–∞–Ω—è—é—Ç –±–æ–ª—å—à–µ —Å—Ö–æ–¥—Å—Ç–≤–∞ —Å –≥–∏–ø–æ—Ç–µ—Ç–∏—á–µ—Å–∫–∏–º –æ–±—â–∏–º –ø—Ä–µ–¥–∫–æ–º –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–π (Boussau et al., 2004).
–ü—Ä–µ–¥–æ–∫ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π, –ø–æ-–≤–∏–¥–∏–º–æ–º—É, –∫–∞–∫ –∏ –≤–æ–ª—å–±–∞—Ö–∏—è, –æ–±–ª–∞–¥–∞–ª —Ü–µ–ª—ã–º —Ä—è–¥–æ–º –º–µ—Ç–∞–±–æ–ª–∏—á–µ—Å–∫–∏—Ö –ø—É—Ç–µ–π, –Ω–µ —Å–≤—è–∑–∞–Ω–Ω—ã—Ö –Ω–∞–ø—Ä—è–º—É—é —Å —Å–∏–Ω—Ç–µ–∑–æ–º –ê–¢–§ (–Ω–∞–ø—Ä–∏–º–µ—Ä, –º–µ—Ç–∞–±–æ–ª–∏–∑–º —Ñ—Ä—É–∫—Ç–æ–∑—ã –∏ –º–∞–Ω–Ω–æ–∑—ã, —Å–∏–Ω—Ç–µ–∑ –ª–∏–ø–∏–¥–æ–≤, –Ω—É–∫–ª–µ–æ—Ç–∏–¥–æ–≤ –∏ –≤–∏—Ç–∞–º–∏–Ω–æ–≤). –ú–Ω–æ–≥–∏–µ –∏–∑ —ç—Ç–∏—Ö –≥–µ–Ω–æ–≤ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω–æ–≥–æ –ø—Ä–æ–∏—Å—Ö–æ–∂–¥–µ–Ω–∏—è –ø–µ—Ä–µ—à–ª–∏ –≤ —è–¥–µ—Ä–Ω—ã–π –≥–µ–Ω–æ–º, –∏ —Å–æ–æ—Ç–≤–µ—Ç—Å—Ç–≤—É—é—â–∏–µ —Ñ–µ—Ä–º–µ–Ω—Ç—ã –∏ –º–µ—Ç–∞–±–æ–ª–∏—á–µ—Å–∫–∏–µ –ø—É—Ç–∏ —Å—Ç–∞–ª–∏ —Ñ—É–Ω–∫—Ü–∏–æ–Ω–∏—Ä–æ–≤–∞—Ç—å –≤ –¥—Ä—É–≥–∏—Ö —á–∞—Å—Ç—è—Ö —ç–≤–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–æ–π –∫–ª–µ—Ç–∫–∏ (Gabaldon, Huynen, 2003). –í–æ–ª—å–±–∞—Ö–∏—è, –Ω–∞–ø—Ä–æ—Ç–∏–≤, –æ—Å—Ç–∞–≤–∏–ª–∞ –≤—Å–µ –ø–æ–¥–æ–±–Ω—ã–µ –º–µ—Ç–∞–±–æ–ª–∏—á–µ—Å–∫–∏–µ —Å–∏—Å—Ç–µ–º—ã «–ø—Ä–∏ —Å–µ–±–µ». –Ø–≤–Ω—ã—Ö —Å–ª–µ–¥–æ–≤ –∫—Ä—É–ø–Ω–æ–º–∞—Å—à—Ç–∞–±–Ω–æ–≥–æ –ø–µ—Ä–µ–Ω–æ—Å–∞ –µ–µ –≥–µ–Ω–æ–≤ –≤ –≥–µ–Ω–æ–º —Ö–æ–∑—è–∏–Ω–∞ –Ω–µ –æ–±–Ω–∞—Ä—É–∂–µ–Ω–æ.
–ö–æ—Ä–µ–Ω–Ω–æ–µ —Ä–∞–∑–ª–∏—á–∏–µ –º–µ–∂–¥—É –≤–æ–ª—å–±–∞—Ö–∏–µ–π –∏ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º–∏ –∑–∞–∫–ª—é—á–∞–µ—Ç—Å—è –≤ –æ—Ä–≥–∞–Ω–∏–∑–∞—Ü–∏–∏ —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–∞ –ø—Ä–æ—Ç–µ–∏–Ω–æ–≤ (—Ç–∞–±–ª. 1). –í–æ–ª—å–±–∞—Ö–∏—è –∏—Å–ø–æ–ª—å–∑—É–µ—Ç —Å–µ–∫—Ä–µ—Ç–æ—Ä–Ω—É—é —Å–∏—Å—Ç–µ–º—É —Ç–∏–ø–∞ IV –¥–ª—è —ç–∫—Å–ø–æ—Ä—Ç–∞ —Å–≤–æ–∏—Ö –±–µ–ª–∫–æ–≤ –≤ —Ü–∏—Ç–æ–ø–ª–∞–∑–º—É —Ö–æ–∑—è–∏–Ω–∞ (Masui et al., 2000; Wu et al., 2004), —Ç–æ–≥–¥–∞ –∫–∞–∫ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è, –Ω–∞–ø—Ä–æ—Ç–∏–≤, –∏–º–ø–æ—Ä—Ç–∏—Ä—É–µ—Ç –±–µ–ª–∫–∏, –∫–æ–¥–∏—Ä—É–µ–º—ã–µ —è–¥–µ—Ä–Ω—ã–º–∏ –≥–µ–Ω–∞–º–∏ –∏ —Å–∏–Ω—Ç–µ–∑–∏—Ä—É–µ–º—ã–µ –≤ —Ü–∏—Ç–æ–ø–ª–∞–∑–º–µ. –ù–∞ –Ω–∞—Ä—É–∂–Ω–æ–π –∏ –≤–Ω—É—Ç—Ä–µ–Ω–Ω–µ–π –º–µ–º–±—Ä–∞–Ω–∞—Ö –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏ —Å—É—â–µ—Å—Ç–≤—É—é—Ç —Å–ø–µ—Ü–∏–∞–ª—å–Ω—ã–µ –±–µ–ª–∫–æ–≤—ã–µ –∫–æ–º–ø–ª–µ–∫—Å—ã (TOM –∏ TIM —Å–æ–æ—Ç–≤–µ—Ç—Å—Ç–≤–µ–Ω–Ω–æ), –æ—Å—É—â–µ—Å—Ç–≤–ª—è—é—â–∏–µ —ç—Ç–æ—Ç –∏–º–ø–æ—Ä—Ç (Rehling et al., 2001). –°—Ö–æ–¥—Å—Ç–≤–∞ –≤ —Å—Ç—Ä–æ–µ–Ω–∏–∏ —Å–∏—Å—Ç–µ–º —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–∞ –±–µ–ª–∫–æ–≤ —É –≤–æ–ª—å–±–∞—Ö–∏–∏ –∏ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏ –Ω–µ –Ω–∞–±–ª—é–¥–∞–µ—Ç—Å—è. –ö—Ä–∞–π–Ω–µ –∏–Ω—Ç–µ—Ä–µ—Å–µ–Ω —Ç–æ—Ç —Ñ–∞–∫—Ç, —á—Ç–æ —Ç–µ –∏–∑ –∫–æ–¥–∏—Ä—É–µ–º—ã—Ö –≤ —è–¥—Ä–µ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã—Ö –±–µ–ª–∫–æ–≤, –∫–æ—Ç–æ—Ä—ã–µ –∏–º–µ—é—Ç –±–∞–∫—Ç–µ—Ä–∏–∞–ª—å–Ω–æ–µ –ø—Ä–æ–∏—Å—Ö–æ–∂–¥–µ–Ω–∏–µ, —Å–∏–Ω—Ç–µ–∑–∏—Ä—É—é—Ç—Å—è –ø—Ä–µ–∏–º—É—â–µ—Å—Ç–≤–µ–Ω–Ω–æ –Ω–∞ —Ä–∏–±–æ—Å–æ–º–∞—Ö, –∞—Å—Å–æ—Ü–∏–∏—Ä–æ–≤–∞–Ω–Ω—ã—Ö —Å –Ω–∞—Ä—É–∂–Ω–æ–π –º–µ–º–±—Ä–∞–Ω–æ–π –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π, —Ç–æ–≥–¥–∞ –∫–∞–∫ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã–µ –±–µ–ª–∫–∏ —á–∏—Å—Ç–æ —ç–≤–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–æ–≥–æ –ø—Ä–æ–∏—Å—Ö–æ–∂–¥–µ–Ω–∏—è —á–∞—â–µ —Å–∏–Ω—Ç–µ–∑–∏—Ä—É—é—Ç—Å—è –Ω–∞ —Ü–∏—Ç–æ–ø–ª–∞–∑–º–∞—Ç–∏—á–µ—Å–∫–∏—Ö —Ä–∏–±–æ—Å–æ–º–∞—Ö, —É–¥–∞–ª–µ–Ω–Ω—ã—Ö –æ—Ç –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π (Marc et al., 2002).
–°–∏–≥–Ω–∞–ª—å–Ω–æ-—Ä–µ–≥—É–ª—è—Ç–æ—Ä–Ω—ã–µ —Å–∏—Å—Ç–µ–º—ã. –≠–≤–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–∞—è –∫–ª–µ—Ç–∫–∞ –∏–º–µ–µ—Ç —Ü–µ–ª—ã–π —Ä—è–¥ —ç—Ñ—Ñ–µ–∫—Ç–∏–≤–Ω—ã—Ö —Å—Ä–µ–¥—Å—Ç–≤ –¥–ª—è —Ä–µ–≥—É–ª—è—Ü–∏–∏ –¥–µ—è—Ç–µ–ª—å–Ω–æ—Å—Ç–∏ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π (Cummins, 2001). –í —á–∞—Å—Ç–Ω–æ—Å—Ç–∏, —Å–∏–≥–Ω–∞–ª—ã –ø–µ—Ä–µ–¥–∞—é—Ç—Å—è –≤ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—é –ø—Ä–∏ –ø–æ–º–æ—â–∏ –∏–æ–Ω–æ–≤ Ca2+. –°–∏–≥–Ω–∞–ª—å–Ω–∞—è —Ä–æ–ª—å –∏–æ–Ω–æ–≤ –∫–∞–ª—å—Ü–∏—è –≤ –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º–µ –æ–±—ã—á–Ω–æ –æ–ø–æ—Å—Ä–µ–¥—É–µ—Ç—Å—è —Å–ø–µ—Ü–∏–∞–ª—å–Ω—ã–º–∏ –±–µ–ª–∫–∞–º–∏ — –∫–∞–ª—å–º–æ–¥—É–ª–∏–Ω–∞–º–∏; –≤ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è—Ö –∏–æ–Ω—ã –∫–∞–ª—å—Ü–∏—è –º–æ–≥—É—Ç –¥–µ–π—Å—Ç–≤–æ–≤–∞—Ç—å –Ω–µ–ø–æ—Å—Ä–µ–¥—Å—Ç–≤–µ–Ω–Ω–æ –Ω–∞ —Ñ–µ—Ä–º–µ–Ω—Ç—ã –±–µ–∑ –ø–æ—Å—Ä–µ–¥–Ω–∏—á–µ—Å—Ç–≤–∞ –¥—Ä—É–≥–∏—Ö –±–µ–ª–∫–æ–≤. –Ý–µ–≥—É–ª—è—Ü–∏—è –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π –æ—Å—É—â–µ—Å—Ç–≤–ª—è–µ—Ç—Å—è —Ç–∞–∫–∂–µ –ø—Ä–∏ –ø–æ–º–æ—â–∏ —Ü–ê–ú–§, –∫–æ—Ç–æ—Ä–∞—è –¥–µ–π—Å—Ç–≤—É–µ—Ç —á–µ—Ä–µ–∑ –ø—Ä–æ—Ç–µ–∏–Ω–∫–∏–Ω–∞–∑—É –ê, –∏–ª–∏ –ø—É—Ç–µ–º —Å–≤—è–∑—ã–≤–∞–Ω–∏—è —Å —Ä–µ—Ü–µ–ø—Ç–æ—Ä–Ω—ã–º –±–µ–ª–∫–æ–º –≤–Ω–µ—à–Ω–µ–π —Å—Ç–æ—Ä–æ–Ω—ã –≤–Ω—É—Ç—Ä–µ–Ω–Ω–µ–π –º–µ–º–±—Ä–∞–Ω—ã –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏. –ï—Å—Ç—å –¥–∞–Ω–Ω—ã–µ –æ —Ä–µ–≥—É–ª—è—Ü–∏–∏ —Ñ—É–Ω–∫—Ü–∏–π –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π —Ü–ì–ú–§ –∏ –ø—Ä–æ—Ç–µ–∏–Ω–∫–∏–Ω–∞–∑–∞–º–∏ C (–ö—É–ª–∏–Ω—Å–∫–∏–π, 1997). –í –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è—Ö –ø—Ä–∏—Å—É—Ç—Å—Ç–≤—É–µ—Ç –∑–Ω–∞—á–∏—Ç–µ–ª—å–Ω–æ–µ –∫–æ–ª–∏—á–µ—Å—Ç–≤–æ –±–µ–ª–∫–æ–≤, —É—á–∞—Å—Ç–≤—É—é—â–∏—Ö –≤ –ø—Ä–∏–µ–º–µ –∏ –ø–µ—Ä–µ–¥–∞—á–µ —Å–∏–≥–Ω–∞–ª–æ–≤, –≤–∫–ª—é—á–∞—è –ì–¢–§- –∏ Ca2+ — —Å–≤—è–∑—ã–≤–∞—é—â–∏–µ –±–µ–ª–∫–∏ –∏ —Ü–µ–ª—ã–π —Ä—è–¥ —Ä–∞–∑–ª–∏—á–Ω—ã—Ö –ø—Ä–æ—Ç–µ–∏–Ω–∫–∏–Ω–∞–∑ (Reichert, Neupert, 2004).
–ù–∏ –æ–¥–Ω–æ –∏–∑ —ç—Ç–∏—Ö —Å—Ä–µ–¥—Å—Ç–≤ –∫–ª–µ—Ç–∫–∞ —Ö–æ–∑—è–∏–Ω–∞ –Ω–µ –º–æ–∂–µ—Ç –∏—Å–ø–æ–ª—å–∑–æ–≤–∞—Ç—å –¥–ª—è —Ä–µ–≥—É–ª—è—Ü–∏–∏ –¥–µ—è—Ç–µ–ª—å–Ω–æ—Å—Ç–∏ –≤–æ–ª—å–±–∞—Ö–∏–∏ –∏–∑-–∑–∞ –æ—Ç—Å—É—Ç—Å—Ç–≤–∏—è —É –ø–æ—Å–ª–µ–¥–Ω–µ–π —Å–æ–æ—Ç–≤–µ—Ç—Å—Ç–≤—É—é—â–∏—Ö —Ä–µ—Ü–µ–ø—Ç–æ—Ä–æ–≤, –ø—Ä–æ—Ç–µ–∏–Ω–∫–∏–Ω–∞–∑ –∏ –∏–æ–Ω–Ω—ã—Ö –∫–∞–Ω–∞–ª–æ–≤ (—É –≤–æ–ª—å–±–∞—Ö–∏–∏ –Ω–µ—Ç –º–µ–º–±—Ä–∞–Ω–Ω—ã—Ö –∫–∞–Ω–∞–ª–æ–≤ –¥–ª—è —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–∞ –∏–æ–Ω–æ–≤ –∫–∞–ª—å—Ü–∏—è, –ø—Ä–æ—Ç–µ–∏–Ω–∫–∏–Ω–∞–∑ –ê, —Ä–µ—Ü–µ–ø—Ç–æ—Ä–æ–≤ —Ü–ê–ú–§ –∏ —Ç.–¥.).
–°–∞–º–æ–µ –≥–ª–∞–≤–Ω–æ–µ —Å—Ä–µ–¥—Å—Ç–≤–æ, –æ–±–µ—Å–ø–µ—á–∏–≤–∞—é—â–µ–µ –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º–µ –ø–æ–ª–Ω—ã–π –∫–æ–Ω—Ç—Ä–æ–ª—å –Ω–∞–¥ –¥–µ—è—Ç–µ–ª—å–Ω–æ—Å—Ç—å—é –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π, –Ω–µ—Å–æ–º–Ω–µ–Ω–Ω–æ, –æ—Å–Ω–æ–≤–∞–Ω–æ –Ω–∞ —Ç–æ–º, —á—Ç–æ –±–æ–ª—å—à–∞—è —á–∞—Å—Ç—å –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω–æ–≥–æ –ø—Ä–æ—Ç–µ–æ–º–∞ –∫–æ–¥–∏—Ä—É–µ—Ç—Å—è —è–¥–µ—Ä–Ω—ã–º–∏ –≥–µ–Ω–∞–º–∏. –ë–æ–ª—å—à–∏–Ω—Å—Ç–≤–æ –∏—Ö –∏–º–µ–µ—Ç –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–∞–ª—å–Ω–æ–µ –ø—Ä–æ–∏—Å—Ö–æ–∂–¥–µ–Ω–∏–µ –∏ –∏–∑–Ω–∞—á–∞–ª—å–Ω–æ –Ω–∞—Ö–æ–¥–∏–ª–æ—Å—å –≤ —Ö—Ä–æ–º–æ—Å–æ–º–µ –ø—Ä–µ–¥–∫–∞ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π, –Ω–æ –≤–ø–æ—Å–ª–µ–¥—Å—Ç–≤–∏–∏ –±—ã–ª–æ –ø–µ—Ä–µ–Ω–µ—Å–µ–Ω–æ –≤ —è–¥–µ—Ä–Ω—ã–π –≥–µ–Ω–æ–º (—ç—Ç–∏–º –∂–µ –æ–±—ä—è—Å–Ω—è–µ—Ç—Å—è –∏ –º–∞–ª—ã–π —Ä–∞–∑–º–µ—Ä –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã—Ö –≥–µ–Ω–æ–º–æ–≤ –ø–æ —Å—Ä–∞–≤–Ω–µ–Ω–∏—é —Å —Ç–∞–∫–æ–≤—ã–º –≤–æ–ª—å–±–∞—Ö–∏–∏). –≠–∫—Å–ø—Ä–µ—Å—Å–∏—è —ç—Ç–∏—Ö –≥–µ–Ω–æ–≤ –∏ –ø–æ—Å–ª–µ–¥—É—é—â–∞—è –¥–æ—Å—Ç–∞–≤–∫–∞ —Å–æ–æ—Ç–≤–µ—Ç—Å—Ç–≤—É—é—â–∏—Ö –±–µ–ª–∫–æ–≤ –≤ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏, –µ—Å—Ç–µ—Å—Ç–≤–µ–Ω–Ω–æ, –Ω–∞—Ö–æ–¥–∏—Ç—Å—è –ø–æ–¥ –∫–æ–Ω—Ç—Ä–æ–ª–µ–º —è–¥–µ—Ä–Ω–æ-—Ü–∏—Ç–æ–ø–ª–∞–∑–º–∞—Ç–∏—á–µ—Å–∫–∏—Ö —Å–∏–≥–Ω–∞–ª—å–Ω—ã—Ö, —Ä–µ–≥—É–ª—è—Ç–æ—Ä–Ω—ã—Ö –∏ —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–Ω—ã—Ö —Å–∏—Å—Ç–µ–º. –ö–∞–∫ –≥–æ–≤–æ—Ä–∏–ª–æ—Å—å –≤—ã—à–µ, –∑–∞–º–µ—Ç–Ω—ã—Ö —Å–ª–µ–¥–æ–≤ –ø–µ—Ä–µ–Ω–æ—Å–∞ –≥–µ–Ω–æ–≤ –≤–æ–ª—å–±–∞—Ö–∏–∏ –≤ —è–¥–µ—Ä–Ω—ã–π –≥–µ–Ω–æ–º —Ö–æ–∑—è–∏–Ω–∞ –Ω–µ –æ–±–Ω–∞—Ä—É–∂–µ–Ω–æ. –°–ª–µ–¥–æ–≤–∞—Ç–µ–ª—å–Ω–æ, –∏ —ç—Ç–æ –º–æ—â–Ω–æ–µ —Å—Ä–µ–¥—Å—Ç–≤–æ –≤–æ–∑–¥–µ–π—Å—Ç–≤–∏—è –Ω–µ –º–æ–∂–µ—Ç –∏—Å–ø–æ–ª—å–∑–æ–≤–∞—Ç—å—Å—è –∫–ª–µ—Ç–∫–æ–π –≤ –æ—Ç–Ω–æ—à–µ–Ω–∏–∏ –ø–∞—Ä–∞–∑–∏—Ç–∏—á–µ—Å–∫–æ–π –±–∞–∫—Ç–µ—Ä–∏–∏.
–ï—Å–ª–∏ —Å—Ä–µ–¥—Å—Ç–≤–∞ —É–ø—Ä–∞–≤–ª–µ–Ω–∏—è –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º–∏ –Ω–µ–ø—Ä–∏–º–µ–Ω–∏–º—ã –∫ –≤–æ–ª—å–±–∞—Ö–∏–∏, –≤–æ–∑–º–æ–∂–Ω–æ, —Ö–æ–∑—è–∏–Ω –º–æ–∂–µ—Ç —Ä–µ–≥—É–ª–∏—Ä–æ–≤–∞—Ç—å –µ–µ –∂–∏–∑–Ω–µ–¥–µ—è—Ç–µ–ª—å–Ω–æ—Å—Ç—å –∫–∞–∫–∏–º–∏-—Ç–æ –∏–Ω—ã–º–∏ —Å–ø–æ—Å–æ–±–∞–º–∏, –≤–æ–∑–¥–µ–π—Å—Ç–≤—É—è –Ω–∞ —Å–∏–≥–Ω–∞–ª—å–Ω–æ-—Ä–µ–≥—É–ª—è—Ç–æ—Ä–Ω—ã–µ —Å–∏—Å—Ç–µ–º—ã –ø–∞—Ä–∞–∑–∏—Ç–∞? –û–¥–Ω–∞–∫–æ –∏ —ç—Ç–æ—Ç –ø—É—Ç—å –¥–ª—è —Ö–æ–∑—è–µ–≤ –≤–æ–ª—å–±–∞—Ö–∏–∏ –ø—Ä–∞–∫—Ç–∏—á–µ—Å–∫–∏ –∑–∞–∫—Ä—ã—Ç, –ø–æ—Å–∫–æ–ª—å–∫—É –≤–æ–ª—å–±–∞—Ö–∏—è –æ—Ç–ª–∏—á–∞–µ—Ç—Å—è –ø–æ—á—Ç–∏ –ø–æ–ª–Ω–æ–π —Ä–µ–¥—É–∫—Ü–∏–µ–π —Å–∏–≥–Ω–∞–ª—å–Ω–æ-—Ä–µ–≥—É–ª—è—Ç–æ—Ä–Ω—ã—Ö —Å–∏—Å—Ç–µ–º.
–£ –Ω–µ–µ –æ–±–Ω–∞—Ä—É–∂–µ–Ω–æ —Ç–æ–ª—å–∫–æ —Ç—Ä–∏ –≥–µ–Ω–∞, —Å–≤—è–∑–∞–Ω–Ω—ã—Ö —Å –ø—Ä–∏–µ–º–æ–º –∏ –ø–µ—Ä–µ–¥–∞—á–µ–π —Å–∏–≥–Ω–∞–ª–æ–≤, –∏ –≤—Å–µ–≥–æ —à–µ—Å—Ç—å –ø—Ä–µ–¥–ø–æ–ª–æ–∂–∏—Ç–µ–ª—å–Ω—ã—Ö —Ä–µ–≥—É–ª—è—Ç–æ—Ä–æ–≤ —Ç—Ä–∞–Ω—Å–∫—Ä–∏–ø—Ü–∏–∏. –°–∫—É–¥–Ω—ã–π –Ω–∞–±–æ—Ä —Ä–µ–≥—É–ª—è—Ç–æ—Ä–æ–≤ –æ—Ç–º–µ—á–µ–Ω –∏ —É –¥—Ä—É–≥–∏—Ö —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–Ω—Ç–æ–≤ –∏ –æ–±—ä—è—Å–Ω—è–µ—Ç—Å—è –æ–±—ã—á–Ω–æ –ø–æ—Å—Ç–æ—è–Ω—Å—Ç–≤–æ–º —É—Å–ª–æ–≤–∏–π –∏—Ö –æ–±–∏—Ç–∞–Ω–∏—è, —á—Ç–æ –¥–µ–ª–∞–µ—Ç –∞–¥–∞–ø—Ç–∏–≤–Ω—ã–µ –º–æ–¥–∏—Ñ–∏–∫–∞—Ü–∏–∏ –Ω–µ–æ–±—è–∑–∞—Ç–µ–ª—å–Ω—ã–º–∏ –¥–ª—è –≤—ã–∂–∏–≤–∞–Ω–∏—è (Andersson et al., 1998; Seshadri et al., 2003; Wu et al., 2004 ). –£–∫–∞–∑–∞–Ω–Ω–∞—è –ø—Ä–∏—á–∏–Ω–∞ –º–æ–∂–µ—Ç –±—ã—Ç—å –Ω–µ –µ–¥–∏–Ω—Å—Ç–≤–µ–Ω–Ω–æ–π. –Ý–µ–¥—É–∫—Ü–∏—è —Å–∏–≥–Ω–∞–ª—å–Ω–æ-—Ä–µ–≥—É–ª—è—Ç–æ—Ä–Ω—ã—Ö —Å–∏—Å—Ç–µ–º –¥–µ–ª–∞–µ—Ç –≤–Ω—É—Ç—Ä–∏–∫–ª–µ—Ç–æ—á–Ω—ã—Ö –±–∞–∫—Ç–µ—Ä–∏–π –º–µ–Ω–µ–µ –∑–∞–≤–∏—Å–∏–º—ã–º–∏ –æ—Ç –≤—Å–µ–≤–æ–∑–º–æ–∂–Ω—ã—Ö —Å–∏–≥–Ω–∞–ª–æ–≤, –ø–æ—Å—Ç—É–ø–∞—é—â–∏—Ö –∏–∑–≤–Ω–µ, —Ç–æ –µ—Å—Ç—å –æ—Ç —Ö–æ–∑—è–∏–Ω–∞, –∏ —Å–∏–ª—å–Ω–æ —Å–Ω–∏–∂–∞–µ—Ç –≤–µ—Ä–æ—è—Ç–Ω–æ—Å—Ç—å —Ç–æ–≥–æ, —á—Ç–æ —Ö–æ–∑—è–∏–Ω —Å—É–º–µ–µ—Ç –≤—ã—Ä–∞–±–æ—Ç–∞—Ç—å –∫–∞–∫–∏–µ-—Ç–æ —Å–ø–æ—Å–æ–±—ã —É–ø—Ä–∞–≤–ª–µ–Ω–∏—è —Å–∏–º–±–∏–æ–Ω—Ç–æ–º. –í–æ–ª—å–±–∞—Ö–∏—è —Ñ–∞–∫—Ç–∏—á–µ—Å–∫–∏ —É–ø—Ä–∞–≤–ª—è–µ—Ç —Ä–µ–ø—Ä–æ–¥—É–∫—Ü–∏–µ–π, —Ä–∞–∑–≤–∏—Ç–∏–µ–º –∏ –¥–∞–∂–µ —ç–≤–æ–ª—é—Ü–∏–µ–π —Å–≤–æ–∏—Ö —Ö–æ–∑—è–µ–≤, –∏ –¥–µ–ª–∞–µ—Ç —ç—Ç–æ —Ç–∞–∫, –∫–∞–∫ –≤—ã–≥–æ–¥–Ω–æ –µ–π. –î–ª—è —ç—Ç–æ–≥–æ –æ–Ω–∞ –∏—Å–ø–æ–ª—å–∑—É–µ—Ç —Ä–∞–∑–Ω–æ–æ–±—Ä–∞–∑–Ω—ã–µ –∏ —Å–ª–æ–∂–Ω—ã–µ —Å–∏–≥–Ω–∞–ª—å–Ω–æ-—Ä–µ–≥—É–ª—è—Ç–æ—Ä–Ω—ã–µ —Å–∏—Å—Ç–µ–º—ã —ç–≤–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–æ–π –∫–ª–µ—Ç–∫–∏, –∫–æ—Ç–æ—Ä—ã–µ –ø—Ä–µ–¥–æ—Å—Ç–∞–≤–ª—è—é—Ç –µ–π –º–Ω–æ–∂–µ—Å—Ç–≤–æ –ø–æ—Ç–µ–Ω—Ü–∏–∞–ª—å–Ω—ã—Ö «–∑–∞—Ü–µ–ø–æ–∫» — —Ç–æ—á–µ–∫ –ø—Ä–∏–ª–æ–∂–µ–Ω–∏—è —Ä–µ–≥—É–ª–∏—Ä—É—é—â–∏—Ö –∞–≥–µ–Ω—Ç–æ–≤. –£ —Å–∞–º–æ–π –≤–æ–ª—å–±–∞—Ö–∏–∏ —Ç–∞–∫–∏—Ö —Ç–æ—á–µ–∫ –ø—Ä–∏–ª–æ–∂–µ–Ω–∏—è –ø—Ä–∞–∫—Ç–∏—á–µ—Å–∫–∏ –Ω–µ—Ç.
–í–æ–ª—å–±–∞—Ö–∏—è –∫–∞–∫ «–∞–Ω—Ç–∏–º–æ–¥–µ–ª—å–Ω—ã–π» –æ–±—ä–µ–∫—Ç –¥–ª—è —Ä–µ–∫–æ–Ω—Å—Ç—Ä—É–∫—Ü–∏–∏ –ø—Ä–æ–∏—Å—Ö–æ–∂–¥–µ–Ω–∏—è —ç–≤–∫–∞—Ä–∏–æ—Ç
–¢–∞–∫–∏–º –æ–±—Ä–∞–∑–æ–º, –≤–∑–∞–∏–º–æ–æ—Ç–Ω–æ—à–µ–Ω–∏—è –∫–ª–µ—Ç–∫–∏ —Å –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º–∏ –∏ –≤–æ–ª—å–±–∞—Ö–∏–µ–π –≤–æ –º–Ω–æ–≥–∏—Ö –æ—Ç–Ω–æ—à–µ–Ω–∏—è—Ö –ø—Ä–µ–¥—Å—Ç–∞–≤–ª—è—é—Ç –ø–æ–ª–Ω—É—é –ø—Ä–æ—Ç–∏–≤–æ–ø–æ–ª–æ–∂–Ω–æ—Å—Ç—å (—Ç–∞–±–ª. 1). –í–æ–∑–Ω–∏–∫–∞–µ—Ç –≤–æ–ø—Ä–æ—Å: –ø–æ—á–µ–º—É —Å—Ç–æ–ª—å –±–ª–∏–∑–∫–æ—Ä–æ–¥—Å—Ç–≤–µ–Ω–Ω—ã–µ –≤–∏–¥—ã –º–∏–∫—Ä–æ–æ—Ä–≥–∞–Ω–∏–∑–º–æ–≤, –∫–∞–∫ –≤–æ–ª—å–±–∞—Ö–∏—è –∏ –ø—Ä–µ–¥–æ–∫ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π, –ø–æ—Å—Ç—Ä–æ–∏–ª–∏ —Å–≤–æ–∏ –≤–∑–∞–∏–º–æ–æ—Ç–Ω–æ—à–µ–Ω–∏—è —Å —ç–≤–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–æ–π –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º–æ–π –Ω–∞ —Å—Ç–æ–ª—å —Ä–∞–∑–Ω—ã—Ö –ø—Ä–∏–Ω—Ü–∏–ø–∞—Ö? –ò–ª–∏, –±–æ–ª–µ–µ –∫–æ–Ω–∫—Ä–µ—Ç–Ω–æ, –ø–æ—á–µ–º—É –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è –ø–æ–ª–Ω–æ—Å—Ç—å—é «–ø–æ–¥—á–∏–Ω–∏–ª–∞—Å—å» –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º–µ, —Ç–æ–≥–¥–∞ –∫–∞–∫ –≤–æ–ª—å–±–∞—Ö–∏—è, –Ω–∞–ø—Ä–æ—Ç–∏–≤, –≤–æ –º–Ω–æ–≥–æ–º —Å–∞–º–∞ –∫–æ–Ω—Ç—Ä–æ–ª–∏—Ä—É–µ—Ç –µ–µ —Ñ—É–Ω–∫—Ü–∏–æ–Ω–∏—Ä–æ–≤–∞–Ω–∏–µ?
–¢–∞–±–ª–∏—Ü–∞ 1
|
–°—Ö–æ–¥—Å—Ç–≤–æ |
–Ý–∞–∑–ª–∏—á–∏–µ |
|
–ê—ç—Ä–æ–±–Ω—ã–π —ç–Ω–µ—Ä–≥–µ—Ç–∏—á–µ—Å–∫–∏–π –º–µ—Ç–∞–±–æ–ª–∏–∑–º (—Ü–∏–∫–ª –ö—Ä–µ–±—Å–∞, –æ–∫–∏—Å–ª–∏—Ç–µ–ª—å–Ω–æ–µ —Ñ–æ—Å—Ñ–æ—Ä–∏–ª–∏—Ä–æ–≤–∞–Ω–∏–µ) –¢—Ä–∞–Ω—Å–ø–æ—Ä—Ç –º–∞–ª—ã—Ö –º–æ–ª–µ–∫—É–ª –û–±–æ–ª–æ—á–∫–∞ (–≤–Ω—É—Ç—Ä–µ–Ω–Ω—è—è –º–µ–º–±—Ä–∞–Ω–∞ — «—Å–≤–æ—è», –≤–Ω–µ—à–Ω—è—è — «—Ö–æ–∑—è–π—Å–∫–∞—è») –ë–∞–∑–æ–≤—ã–µ –∏–Ω—Ñ–æ—Ä–º–∞—Ü–∏–æ–Ω–Ω—ã–µ —Å–∏—Å—Ç–µ–º—ã (–∫–æ–ª—å—Ü–µ–≤–∞—è —Ö—Ä–æ–º–æ—Å–æ–º–∞, —Ä–µ–ø–ª–∏–∫–∞—Ü–∏—è, —Ç—Ä–∞–Ω—Å–∫—Ä–∏–ø—Ü–∏—è, —Ç—Ä–∞–Ω—Å–ª—è—Ü–∏—è, —Ä–∏–±–æ—Å–æ–º—ã –∏ –¥—Ä.) |
–õ–æ–∫–∞–ª–∏–∑–∞—Ü–∏—è –±–æ–ª—å—à–∏–Ω—Å—Ç–≤–∞ –≥–µ–Ω–æ–≤: –≤ —è–¥—Ä–µ (–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è) –∏–ª–∏ –≤ «—Å–≤–æ–µ–π» —Ö—Ä–æ–º–æ—Å–æ–º–µ (–≤–æ–ª—å–±–∞—Ö–∏—è) –ù–∞–ø—Ä–∞–≤–ª–µ–Ω–∏–µ —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–∞ –±–µ–ª–∫–æ–≤: «—ç–∫—Å–ø–æ—Ä—Ç» (–≤–æ–ª—å–±–∞—Ö–∏—è) –∏–ª–∏ «–∏–º–ø–æ—Ä—Ç» (–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è) –ù–∞–ø—Ä–∞–≤–ª–µ–Ω–∏–µ —Ä–µ–≥—É–ª—è—Ç–æ—Ä–Ω—ã—Ö –≤–æ–∑–¥–µ–π—Å—Ç–≤–∏–π (—Å–æ–≤–ø–∞–¥–∞–µ—Ç —Å –Ω–∞–ø—Ä–∞–≤–ª–µ–Ω–∏–µ–º —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–∞ –±–µ–ª–∫–æ–≤) –ù–∞–ø—Ä–∞–≤–ª–µ–Ω–∏–µ –ø–µ—Ä–µ–Ω–æ—Å–∞ –≥–µ–Ω–æ–≤: «—ç–∫—Å–ø–æ—Ä—Ç» (–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è) –∏–ª–∏ «–∏–º–ø–æ—Ä—Ç» (–≤–æ–ª—å–±–∞—Ö–∏—è) |
–ù–∞–º –ø—Ä–µ–¥—Å—Ç–∞–≤–ª—è–µ—Ç—Å—è, —á—Ç–æ –∫–ª—é—á–æ–º –∫ —ç—Ç–æ–π –∑–∞–≥–∞–¥–∫–µ —è–≤–ª—è–µ—Ç—Å—è —Ç–æ—Ç —Ñ–∞–∫—Ç, —á—Ç–æ –±–æ–ª—å—à–∏–Ω—Å—Ç–≤–æ –≥–µ–Ω–æ–≤ –ø—Ä–æ—Ç–æ–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏ –±—ã–ª–∏ –ø–µ—Ä–µ–Ω–µ—Å–µ–Ω—ã –≤ —è–¥–µ—Ä–Ω—ã–π –≥–µ–Ω–æ–º –Ω–∞ —Ä–∞–Ω–Ω–∏—Ö —ç—Ç–∞–ø–∞—Ö —ç–≤–∫–∞—Ä–∏–æ—Ç–∏–∑–∞—Ü–∏–∏ (Martin, 2003), —Ç–æ–≥–¥–∞ –∫–∞–∫ –≥–µ–Ω—ã –≤–æ–ª—å–±–∞—Ö–∏–∏ –≤ –≥–µ–Ω–æ–º —Ö–æ–∑—è–∏–Ω–∞, –ø–æ-–≤–∏–¥–∏–º–æ–º—É, –ø—Ä–∞–∫—Ç–∏—á–µ—Å–∫–∏ –Ω–µ –ø–µ—Ä–µ–Ω–æ—Å–∏–ª–∏—Å—å (Wu et al., 2004). –ö—Ä–æ–º–µ —Ç–æ–≥–æ, –º–Ω–æ–≥–∏–µ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã–µ –±–µ–ª–∫–∏, –∫–æ–¥–∏—Ä—É–µ–º—ã–µ —è–¥–µ—Ä–Ω—ã–º–∏ –≥–µ–Ω–∞–º–∏, –¥–∞–∂–µ –Ω–µ –Ω–µ—Å—É—Ç –ø—Ä–∏–∑–Ω–∞–∫–æ–≤ –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–∞–ª—å–Ω–æ–≥–æ –ø—Ä–æ–∏—Å—Ö–æ–∂–¥–µ–Ω–∏—è. –û–Ω–∏, –ø–æ-–≤–∏–¥–∏–º–æ–º—É, –≤–æ–∑–Ω–∏–∫–ª–∏ —É —ç–≤–∫–∞—Ä–∏–æ—Ç —É–∂–µ –ø–æ—Å–ª–µ –ø—Ä–∏–æ–±—Ä–µ—Ç–µ–Ω–∏—è –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω–æ–≥–æ —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–Ω—Ç–∞ (Karlberg, 2004). –í–∫–ª—é—á–µ–Ω–∏–µ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã—Ö –≥–µ–Ω–æ–≤ –≤ —è–¥–µ—Ä–Ω—ã–π –≥–µ–Ω–æ–º, –∏–Ω—Ç–µ–≥—Ä–∞—Ü–∏—è –∏—Ö –≤ —è–¥–µ—Ä–Ω–æ-—Ü–∏—Ç–æ–ø–ª–∞–∑–º–∞—Ç–∏—á–µ—Å–∫–∏–µ –≥–µ–Ω–Ω—ã–µ —Å–µ—Ç–∏ –∏ —Å–∏–≥–Ω–∞–ª—å–Ω–æ-—Ä–µ–≥—É–ª—è—Ç–æ—Ä–Ω—ã–µ —Å–∏—Å—Ç–µ–º—ã, –∞ —Ç–∞–∫–∂–µ –∏–Ω—Ç—Ä–æ–¥—É–∫—Ü–∏—è –≤ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏ «—á—É–∂–¥—ã—Ö» –∏–º —ç–≤–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–∏—Ö –±–µ–ª–∫–æ–≤ (–≥–µ–Ω—ã –∫–æ—Ç–æ—Ä—ã—Ö –∏–∑–Ω–∞—á–∞–ª—å–Ω–æ —Å—Ñ–æ—Ä–º–∏—Ä–æ–≤–∞–ª–∏—Å—å –≤ —è–¥—Ä–µ) –∏—Å–∫–ª—é—á–∏–ª–∏ –≤—Å—è–∫—É—é –≤–æ–∑–º–æ–∂–Ω–æ—Å—Ç—å —ç–≥–æ–∏—Å—Ç–∏—á–µ—Å–∫–æ–π —ç–≤–æ–ª—é—Ü–∏–∏ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π (Martin, Herrmann-Reinhold, 1998; Rand et al., 2001).
–í–æ–ª—å–±–∞—Ö–∏—è, –Ω–∞–ø—Ä–æ—Ç–∏–≤, —Å–æ—Ö—Ä–∞–Ω–∏–ª–∞ –¥–æ—Å—Ç–∞—Ç–æ—á–Ω–æ –≤—ã—Å–æ–∫–∏–π —É—Ä–æ–≤–µ–Ω—å —Å–∞–º–æ—Å—Ç–æ—è—Ç–µ–ª—å–Ω–æ—Å—Ç–∏ –Ω–µ —Ç–æ–ª—å–∫–æ –≤ –æ—Ç–Ω–æ—à–µ–Ω–∏–∏ —ç–∫—Å–ø—Ä–µ—Å—Å–∏–∏ —Å–æ–±—Å—Ç–≤–µ–Ω–Ω—ã—Ö –≥–µ–Ω–æ–≤, –Ω–æ –∏ –Ω–∞ –º–µ—Ç–∞–±–æ–ª–∏—á–µ—Å–∫–æ–º —É—Ä–æ–≤–Ω–µ. –≠—Ç–æ –ø–æ–∑–≤–æ–ª—è–µ—Ç –µ–π –≤—Ä–µ–º—è –æ—Ç –≤—Ä–µ–º–µ–Ω–∏ —Å–æ–≤–µ—Ä—à–∞—Ç—å –≥–æ—Ä–∏–∑–æ–Ω—Ç–∞–ª—å–Ω—ã–µ –ø–µ—Ä–µ—Ö–æ–¥—ã –º–µ–∂–¥—É —Ä–∞–∑–Ω—ã–º–∏ –≤–∏–¥–∞–º–∏ —Ö–æ–∑—è–µ–≤, –∞ —Ç–∞–∫–∂–µ –±—ã—Å—Ç—Ä–æ —ç–≤–æ–ª—é—Ü–∏–æ–Ω–∏—Ä–æ–≤–∞—Ç—å «—ç–≥–æ–∏—Å—Ç–∏—á–µ—Å–∫–∏–º» –æ–±—Ä–∞–∑–æ–º, –≤—ã—Ä–∞–±–∞—Ç—ã–≤–∞—è —Ä–∞–∑–ª–∏—á–Ω—ã–µ —Å–ø–æ—Å–æ–±—ã —É–ø—Ä–∞–≤–ª–µ–Ω–∏—è —Å–≤–æ–∏–º–∏ —Ö–æ–∑—è–µ–≤–∞–º–∏, –ø–æ—Ä–æ–π –¥–∞–ª–µ–∫–æ –Ω–µ –±–µ–∑–±–æ–ª–µ–∑–Ω–µ–Ω–Ω—ã–µ –¥–ª—è –ø–æ—Å–ª–µ–¥–Ω–∏—Ö.
–° —É–∫–∞–∑–∞–Ω–Ω—ã–º –ø—Ä–∏–Ω—Ü–∏–ø–∏–∞–ª—å–Ω—ã–º —Ä–∞–∑–ª–∏—á–∏–µ–º –≤ –ª–æ–∫–∞–ª–∏–∑–∞—Ü–∏–∏ –±–æ–ª—å—à–∏–Ω—Å—Ç–≤–∞ –≥–µ–Ω–æ–≤, –Ω–µ–æ–±—Ö–æ–¥–∏–º—ã—Ö –¥–ª—è –∂–∏–∑–Ω–µ–¥–µ—è—Ç–µ–ª—å–Ω–æ—Å—Ç–∏ –≤–æ–ª—å–±–∞—Ö–∏–∏ –∏ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π, —Ç–µ—Å–Ω–æ —Å–≤—è–∑–∞–Ω–æ –¥—Ä—É–≥–æ–µ –ø—Ä–∏–Ω—Ü–∏–ø–∏–∞–ª—å–Ω–æ–µ —Ä–∞–∑–ª–∏—á–∏–µ — –≤ –Ω–∞–ø—Ä–∞–≤–ª–µ–Ω–∏–∏ —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–∞ –±–µ–ª–∫–æ–≤. –ï—Å–ª–∏ –≤–æ–ª—å–±–∞—Ö–∏—è —ç–∫—Å–ø–æ—Ä—Ç–∏—Ä—É–µ—Ç —Å–æ–±—Å—Ç–≤–µ–Ω–Ω—ã–µ –±–µ–ª–∫–∏ –≤ —Ü–∏—Ç–æ–ø–ª–∞–∑–º—É —Ö–æ–∑—è–∏–Ω–∞, —á—Ç–æ –ø–æ–∑–≤–æ–ª—è–µ—Ç –µ–π —Ä–µ–≥—É–ª–∏—Ä–æ–≤–∞—Ç—å –¥–µ—è—Ç–µ–ª—å–Ω–æ—Å—Ç—å –µ–≥–æ —Ü–∏—Ç–æ—Å–∫–µ–ª–µ—Ç–∞ –∏ –¥—Ä—É–≥–∏—Ö –º–æ–ª–µ–∫—É–ª—è—Ä–Ω—ã—Ö —Å–∏—Å—Ç–µ–º, —Ç–æ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏, –Ω–∞–ø—Ä–æ—Ç–∏–≤, –∏–º–ø–æ—Ä—Ç–∏—Ä—É—é—Ç –Ω–µ–æ–±—Ö–æ–¥–∏–º—ã–µ –∏–º –±–µ–ª–∫–∏ –∏–∑ —Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã. –ü–æ-–≤–∏–¥–∏–º–æ–º—É, —Å–∏—Å—Ç–µ–º—ã, –æ–±–µ—Å–ø–µ—á–∏–≤–∞—é—â–∏–µ —ç—Ç–æ—Ç –∏–º–ø–æ—Ä—Ç, –¥–æ–ª–∂–Ω—ã –±—ã–ª–∏ —Å–ª–æ–∂–∏—Ç—å—Å—è –æ—á–µ–Ω—å —Ä–∞–Ω–æ, —Ç–∞–∫ –∫–∞–∫ –±–µ–∑ –Ω–∏—Ö –ø–µ—Ä–µ–Ω–æ—Å –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã—Ö –≥–µ–Ω–æ–≤ –≤ —è–¥—Ä–æ –ø—Ä–∏–≤–µ–ª –±—ã –∫ –≥–∏–±–µ–ª–∏ —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–Ω—Ç–æ–≤.
–°–æ–≥–ª–∞—Å–Ω–æ –Ω–∞—à–∏–º –ø—Ä–µ–¥—Å—Ç–∞–≤–ª–µ–Ω–∏—è–º –æ –ø—Ä–æ–∏—Å—Ö–æ–∂–¥–µ–Ω–∏–∏ —ç–≤–∫–∞—Ä–∏–æ—Ç (–ú–∞—Ä–∫–æ–≤, –ö—É–ª–∏–∫–æ–≤, 2005), –≤ —ç–≤–æ–ª—é—Ü–∏–∏ –ø—Ä–µ–¥–∫–∞ –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã –±—ã–ª –ø–µ—Ä–∏–æ–¥ –∞–∫—Ç–∏–≤–Ω–æ–π –∏–Ω–∫–æ—Ä–ø–æ—Ä–∞—Ü–∏–∏ —á—É–∂–µ—Ä–æ–¥–Ω–æ–≥–æ –≥–µ–Ω–µ—Ç–∏—á–µ—Å–∫–æ–≥–æ –º–∞—Ç–µ—Ä–∏–∞–ª–∞ (—Ä–∏—Å. 1). –ù–∞–º–∏ –æ–±–æ—Å–Ω–æ–≤–∞–Ω–æ –ø—Ä–µ–¥–ø–æ–ª–æ–∂–µ–Ω–∏–µ, —á—Ç–æ –ø—Ä–µ–¥–∫–æ–º –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã –±—ã–ª–∞ –∞—Ä—Ö–µ–±–∞–∫—Ç–µ—Ä–∏—è (–≤–æ–∑–º–æ–∂–Ω–æ, –º–µ—Ç–∞–Ω–æ–≥–µ–Ω–Ω–∞—è), –∫–æ—Ç–æ—Ä–∞—è –≤ —É—Å–ª–æ–≤–∏—è—Ö –∫—Ä–∏–∑–∏—Å–∞, –≤—ã–∑–≤–∞–Ω–Ω–æ–≥–æ —Ä–æ—Å—Ç–æ–º –∫–æ–Ω—Ü–µ–Ω—Ç—Ä–∞—Ü–∏–∏ –∫–∏—Å–ª–æ—Ä–æ–¥–∞, –ø—Ä–∏–æ–±—Ä–µ–ª–∞ —Å–ø–æ—Å–æ–±–Ω–æ—Å—Ç—å –±—ã—Å—Ç—Ä–æ –∏ —ç—Ñ—Ñ–µ–∫—Ç–∏–≤–Ω–æ –∏–Ω–∫–æ—Ä–ø–æ—Ä–∏—Ä–æ–≤–∞—Ç—å –≤ —Å–≤–æ–π –≥–µ–Ω–æ–º –î–ù–ö –Ω–µ—Ä–æ–¥—Å—Ç–≤–µ–Ω–Ω—ã—Ö –≤–∏–¥–æ–≤ –º–∏–∫—Ä–æ–æ—Ä–≥–∞–Ω–∏–∑–º–æ–≤. –≠—Ç–∞ –∞—Ä—Ö–µ–±–∞–∫—Ç–µ—Ä–∏—è –∑–∞–∏–º—Å—Ç–≤–æ–≤–∞–ª–∞ –≥–µ–Ω—ã –∏ –≥–µ–Ω–Ω—ã–µ –∫–æ–º–ø–ª–µ–∫—Å—ã —É —Ä–∞–∑–Ω—ã—Ö –±–∞–∫—Ç–µ—Ä–∏–π, –≤ –ø–µ—Ä–≤—É—é –æ—á–µ—Ä–µ–¥—å — –∞–Ω–∞—ç—Ä–æ–±–Ω—ã—Ö –∏ –º–∏–∫—Ä–æ–∞—ç—Ä–æ—Ñ–∏–ª—å–Ω—ã—Ö –±—Ä–æ–¥–∏–ª—å—â–∏–∫–æ–≤. –í –∏—Ç–æ–≥–µ —Å—Ñ–æ—Ä–º–∏—Ä–æ–≤–∞–ª—Å—è —Ö–∏–º–µ—Ä–Ω—ã–π –º–∏–∫—Ä–æ–æ—Ä–≥–∞–Ω–∏–∑–º —Å –∞—Ä—Ö–µ–±–∞–∫—Ç–µ—Ä–∏–∞–ª—å–Ω—ã–º–∏ —Å–∏—Å—Ç–µ–º–∞–º–∏ —Ä–µ–ø–ª–∏–∫–∞—Ü–∏–∏, —Ç—Ä–∞–Ω—Å–∫—Ä–∏–ø—Ü–∏–∏, —Ç—Ä–∞–Ω—Å–ª—è—Ü–∏–∏ –∏ –±–∞–∑–æ–≤–æ–π —Ä–µ–≥—É–ª—è—Ç–æ—Ä–∏–∫–æ–π, –∏ —Å –±–∞–∫—Ç–µ—Ä–∏–∞–ª—å–Ω—ã–º –º–µ—Ç–∞–±–æ–ª–∏–∑–º–æ–º –∏ –ø–µ—Ä–∏—Ñ–µ—Ä–∏—á–µ—Å–∫–∏–º–∏ —Å–∏–≥–Ω–∞–ª—å–Ω–æ-—Ä–µ–≥—É–ª—è—Ç–æ—Ä–Ω—ã–º–∏ —Å–∏—Å—Ç–µ–º–∞–º–∏. –≠—Ç–æ—Ç –º–∏–∫—Ä–æ–æ—Ä–≥–∞–Ω–∏–∑–º –≤ –¥–∞–ª—å–Ω–µ–π—à–µ–º –ø—Ä–∏–æ–±—Ä–µ–ª —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–Ω—Ç–æ–≤ — –∞—ç—Ä–æ–±–Ω—ã—Ö –∞–ª—å—Ñ–∞–ø—Ä–æ—Ç–µ–æ–±–∞–∫—Ç–µ—Ä–∏–π, —Å—Ç–∞–≤—à–∏—Ö –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º–∏.
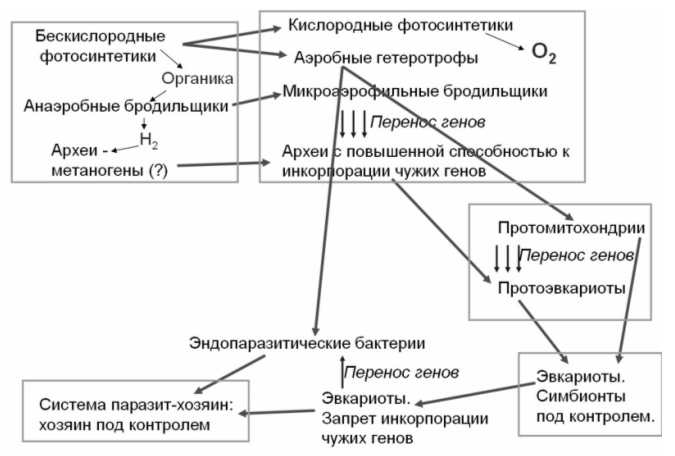
–Ý–∏—Å. 1. –°—Ö–µ–º–∞ –ø—Ä–æ–∏—Å—Ö–æ–∂–¥–µ–Ω–∏—è —ç–≤–∫–∞—Ä–∏–æ—Ç –∏ –ø–æ–∑–¥–Ω–µ–π—à–µ–≥–æ –ø—Ä–∏–æ–±—Ä–µ—Ç–µ–Ω–∏—è –∏–º–∏ –±–∞–∫—Ç–µ—Ä–∏–π-—ç–Ω–¥–æ–ø–∞—Ä–∞–∑–∏—Ç–æ–≤
–í–∫–ª—é—á–µ–Ω–∏–µ –≥–µ–Ω–æ–≤ –ø—Ä–æ—Ç–æ–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π –≤ —Ü–µ–Ω—Ç—Ä–∞–ª—å–Ω—ã–π (—è–¥–µ—Ä–Ω—ã–π) –≥–µ–Ω–æ–º, —Å–æ–≥–ª–∞—Å–Ω–æ —ç—Ç–æ–π —Ç–µ–æ—Ä–∏–∏, –º–æ–≥–ª–æ –Ω–∞—á–∞—Ç—å—Å—è –¥–∞–∂–µ —Ä–∞–Ω—å—à–µ, —á–µ–º —Å–ª–æ–∂–∏–ª–∞—Å—å —ç–Ω–¥–æ—Å–∏–º–±–∏–æ—Ç–∏—á–µ—Å–∫–∞—è —Å–∏—Å—Ç–µ–º–∞, —Ç–æ –µ—Å—Ç—å –≤ —Ç–æ—Ç –ø–µ—Ä–∏–æ–¥, –∫–æ–≥–¥–∞ –ø—Ä–µ–¥–æ–∫ –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã –∏ –ø—Ä–æ—Ç–æ–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏ —Å—É—â–µ—Å—Ç–≤–æ–≤–∞–ª–∏ –µ—â–µ –ø–æ—Ä–æ–∑–Ω—å, –Ω–æ –≤ —Ç–µ—Å–Ω–æ–º –∫–æ–Ω—Ç–∞–∫—Ç–µ –≤ –ø—Ä–µ–¥–µ–ª–∞—Ö –æ–¥–Ω–æ–≥–æ –∏ —Ç–æ–≥–æ –∂–µ –º–∏–∫—Ä–æ–±–Ω–æ–≥–æ —Å–æ–æ–±—â–µ—Å—Ç–≤–∞. –í —ç—Ç–æ—Ç –ø–µ—Ä–∏–æ–¥ –ø—Ä–æ–∏—Å—Ö–æ–¥–∏–ª–∞ –≤–∑–∞–∏–º–Ω–∞—è «–ø–æ–¥–≥–æ–Ω–∫–∞» –º–µ—Ç–∞–±–æ–ª–∏–∑–º–∞ –∏ —Å–∏–≥–Ω–∞–ª—å–Ω–æ-—Ä–µ–≥—É–ª—è—Ç–æ—Ä–Ω—ã—Ö —Å–∏—Å—Ç–µ–º –¥–≤—É—Ö –º–∏–∫—Ä–æ–±–æ–≤, –≥–æ—Ç–æ–≤–∏–≤—à–∞—è –ø–æ—á–≤—É –¥–ª—è –ø–æ—Å–ª–µ–¥—É—é—â–µ–≥–æ –∏—Ö –æ–±—ä–µ–¥–∏–Ω–µ–Ω–∏—è –≤ –µ–¥–∏–Ω—ã–π –æ—Ä–≥–∞–Ω–∏–∑–º. –í–æ–∑–º–æ–∂–Ω–æ, —Ç–æ–≥–¥–∞ –∂–µ –Ω–∞—á–∞–ª–∞ —Å–∫–ª–∞–¥—ã–≤–∞—Ç—å—Å—è –∏ —Å–∏—Å—Ç–µ–º–∞ —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–∞ –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º–∞—Ç–∏—á–µ—Å–∫–∏—Ö –ø—Ä–æ—Ç–µ–∏–Ω–æ–≤ –≤ –±—É–¥—É—â–∏–µ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏. –ü–æ—Å–ª–µ –æ–±—ä–µ–¥–∏–Ω–µ–Ω–∏—è –ø–µ—Ä–µ–Ω–æ—Å –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∞–ª—å–Ω—ã—Ö –≥–µ–Ω–æ–≤ –≤ —Ü–µ–Ω—Ç—Ä–∞–ª—å–Ω—ã–π –≥–µ–Ω–æ–º –ø—Ä–æ–¥–æ–ª–∂–∞–ª—Å—è.
–¢–∞–∫–∏–º –æ–±—Ä–∞–∑–æ–º, –æ—Ç–Ω–æ—à–µ–Ω–∏—è –ø—Ä–µ–¥–∫–∞ –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã —Å –±—É–¥—É—â–∏–º–∏ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º–∏ –∏ –æ—Ä–≥–∞–Ω–∏–∑–º–æ–≤-—Ö–æ–∑—è–µ–≤ —Å –≤–æ–ª—å–±–∞—Ö–∏–µ–π –∏–∑–Ω–∞—á–∞–ª—å–Ω–æ —Å—Ç—Ä–æ–∏–ª–∏—Å—å –Ω–∞ –¥–∏–∞–º–µ—Ç—Ä–∞–ª—å–Ω–æ –ø—Ä–æ—Ç–∏–≤–æ–ø–æ–ª–æ–∂–Ω–æ–π –æ—Å–Ω–æ–≤–µ. –û—Å–æ–±–µ–Ω–Ω–æ —á–µ—Ç–∫–æ —ç—Ç–∞ –ø—Ä–æ—Ç–∏–≤–æ–ø–ª–æ–∂–Ω–æ—Å—Ç—å –ø—Ä–æ—è–≤–ª—è–µ—Ç—Å—è –≤ –Ω–∞–ø—Ä–∞–≤–ª–µ–Ω–∏–∏ —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–∞ –ø—Ä–æ—Ç–µ–∏–Ω–æ–≤. –í —ç—Ç–æ–º –∞—Å–ø–µ–∫—Ç–µ –ø—Ä–µ–¥–æ–∫ –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã «–ø–æ—Å—Ç—É–ø–∞–ª» —Å –ø—Ä–æ—Ç–æ–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º–∏ –ø—Ä–∏–º–µ—Ä–Ω–æ —Ç–∞–∫–∏–º –∂–µ –æ–±—Ä–∞–∑–æ–º, –∫–∞–∫ –≤–æ–ª—å–±–∞—Ö–∏—è — —Å –∫–ª–µ—Ç–∫–∞–º–∏ —Ö–æ–∑—è–∏–Ω–∞. –í —Å–≤—è–∑–∏ —Å —ç—Ç–∏–º –≤—Å–ø–æ–º–Ω–∏–º, —á—Ç–æ –Ω–∞–ø—Ä–∞–≤–ª–µ–Ω–∏–µ –º–µ–º–±—Ä–∞–Ω–Ω–æ–≥–æ —Ç—Ä–∞–Ω—Å–ø–æ—Ä—Ç–∞ –ê–¢–§, –Ω–∞–±–ª—é–¥–∞–µ–º–æ–µ —É –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π –∏ –±–ª–∏–∂–∞–π—à–∏—Ö —Ä–æ–¥—Å—Ç–≤–µ–Ω–Ω–∏–∫–æ–≤ –≤–æ–ª—å–±–∞—Ö–∏–∏ — —Ä–∏–∫–∫–µ—Ç—Å–∏–π, —Ç–æ–∂–µ –ø—Ä–æ—Ç–∏–≤–æ–ø–æ–ª–æ–∂–Ω–æ–µ. –Ý–∏–∫–∫–µ—Ç—Å–∏–∏ –≤—ã–∫–∞—á–∏–≤–∞—é—Ç —ç–Ω–µ—Ä–≥–∏—é –≤ –≤–∏–¥–µ –ê–¢–§ –∏–∑ —Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã —Ö–æ–∑—è–∏–Ω–∞, –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–∏ –∂–µ, –Ω–∞–ø—Ä–æ—Ç–∏–≤, —Å–∞–º–∏ —è–≤–ª—è—é—Ç—Å—è «–∂–µ—Ä—Ç–≤–∞–º–∏ —ç–Ω–µ—Ä–≥–µ—Ç–∏—á–µ—Å–∫–æ–≥–æ –≤–∞–º–ø–∏—Ä–∏–∑–º–∞», –æ—Å—É—â–µ—Å—Ç–≤–ª—è–µ–º–æ–≥–æ –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º–æ–π. –í–æ–∑–º–æ–∂–Ω–æ, –≤–æ –≤–∑–∞–∏–º–æ–æ—Ç–Ω–æ—à–µ–Ω–∏—è—Ö –ø—Ä–µ–¥–∫–æ–≤ –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã –∏ –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π –¥–µ–π—Å—Ç–≤–∏—Ç–µ–ª—å–Ω–æ –ø—Ä–∏—Å—É—Ç—Å—Ç–≤–æ–≤–∞–ª —ç–ª–µ–º–µ–Ω—Ç –ø–∞—Ä–∞–∑–∏—Ç–∏–∑–º–∞, –∫–∞–∫ –ø—Ä–µ–¥–ø–æ–ª–æ–∂–∏–ª –û.–ö–∞—Ä–ª–±–µ—Ä–≥ (Karlberg, 2004), –æ–¥–Ω–∞–∫–æ –Ω–∞–º –ø—Ä–µ–¥—Å—Ç–∞–≤–ª—è–µ—Ç—Å—è –±–æ–ª–µ–µ –≤–µ—Ä–æ—è—Ç–Ω—ã–º, —á—Ç–æ –≤ —Ä–æ–ª–∏ –ø–∞—Ä–∞–∑–∏—Ç–∞ –≤—ã—Å—Ç—É–ø–∞–ª–∞ –Ω–µ –ø—Ä–æ—Ç–æ–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è, –∞ –±–æ–ª–µ–µ –∫—Ä—É–ø–Ω—ã–π –æ—Ä–≥–∞–Ω–∏–∑–º — –ø—Ä–µ–¥–æ–∫ –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã.
–°—É—â–µ—Å—Ç–≤–æ–≤–∞–Ω–∏–µ –≥–∏–ø–æ—Ç–µ—Ç–∏—á–µ—Å–∫–æ–≥–æ –æ—Ä–≥–∞–Ω–∏–∑–º–∞ —Å –∞–Ω–æ–º–∞–ª—å–Ω–æ –≤—ã—Å–æ–∫–æ–π —Å–ø–æ—Å–æ–±–Ω–æ—Å—Ç—å—é –∫ –∏–Ω–∫–æ—Ä–ø–æ—Ä–∞—Ü–∏–∏ —á—É–∂–∏—Ö –≥–µ–Ω–æ–≤ –Ω–µ –º–æ–≥–ª–æ –±—ã—Ç—å –Ω–∏ –¥–æ–ª–≥–∏–º, –Ω–∏ —Å—Ç–∞–±–∏–ª—å–Ω—ã–º. –ë–ª–∞–≥–æ–¥–∞—Ä—è —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–∑—É —Å –∞—ç—Ä–æ–±–Ω–æ–π –±–∞–∫—Ç–µ—Ä–∏–µ–π –ø–µ—Ä–≤–∏—á–Ω–∞—è –ø—Ä–∏—á–∏–Ω–∞ –ø–µ—Ä–µ—Ö–æ–¥–∞ –∫ —Ç–∞–∫–æ–π —Å—Ç—Ä–∞—Ç–µ–≥–∏–∏ –±—ã–ª–∞ —É—Å—Ç—Ä–∞–Ω–µ–Ω–∞ –∏ «–∫–∏—Å–ª–æ—Ä–æ–¥–Ω—ã–π» –∫—Ä–∏–∑–∏—Å –≤ —Ü–µ–ª–æ–º —Ä–∞–∑—Ä–µ—à–µ–Ω. –ü–æ—Å–ª–µ —ç—Ç–æ–≥–æ —ç–≤–∫–∞—Ä–∏–æ—Ç—ã, –ø–æ-–≤–∏–¥–∏–º–æ–º—É, –¥–æ–≤–æ–ª—å–Ω–æ –±—ã—Å—Ç—Ä–æ –≤—ã—Ä–∞–±–æ—Ç–∞–ª–∏ –º–æ—â–Ω—ã–µ —Å–∏—Å—Ç–µ–º—ã –∑–∞—â–∏—Ç—ã –æ—Ç –ª–∞—Ç–µ—Ä–∞–ª—å–Ω–æ–≥–æ –ø–µ—Ä–µ–Ω–æ—Å–∞, –≤–º–µ—Å—Ç–æ –∫–æ—Ç–æ—Ä–æ–≥–æ —Ä–∞–∑–≤–∏–ª–∏—Å—å –±–æ–ª–µ–µ —Å–ª–æ–∂–Ω—ã–µ –∏ –ø—Ä–∏ —ç—Ç–æ–º —Ö–æ—Ä–æ—à–æ –∫–æ–Ω—Ç—Ä–æ–ª–∏—Ä—É–µ–º—ã–µ —Å—Ä–µ–¥—Å—Ç–≤–∞ —Ä–µ–∫–æ–º–±–∏–Ω–∞—Ü–∏–∏, —Å–≤—è–∑–∞–Ω–Ω—ã–µ —Å –ø–æ–ª–æ–≤—ã–º –ø—Ä–æ—Ü–µ—Å—Å–æ–º (–º–µ—Ö–∞–Ω–∏–∑–º—ã –º–µ–π–æ–∑–∞, —Å–ª–∏—è–Ω–∏—è –≥–∞–º–µ—Ç, –º–µ–∂–≤–∏–¥–æ–≤–æ–π —Ä–µ–ø—Ä–æ–¥—É–∫—Ç–∏–≤–Ω–æ–π –∏–∑–æ–ª—è—Ü–∏–∏).
«–ó–∞–ø—Ä–µ—Ç» –≥–æ—Ä–∏–∑–æ–Ω—Ç–∞–ª—å–Ω–æ–≥–æ –ø–µ—Ä–µ–Ω–æ—Å–∞, –æ—Å–æ–±–µ–Ω–Ω–æ —Å–∏–ª—å–Ω–æ –≤—ã—Ä–∞–∂–µ–Ω–Ω—ã–π —É Metazoa (–∫ –∫–æ–∏–º –æ—Ç–Ω–æ—Å—è—Ç—Å—è –≤—Å–µ —Ö–æ–∑—è–µ–≤–∞ –≤–æ–ª—å–±–∞—Ö–∏–∏), –ø—Ä–∏–≤–µ–ª –∫ —Ç–æ–º—É, —á—Ç–æ –ø–µ—Ä–µ–Ω–æ—Å –≥–µ–Ω–æ–≤ –Ω–æ–≤–æ–æ–ø—Ä–∏–æ–±—Ä–µ—Ç–µ–Ω–Ω—ã—Ö —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–Ω—Ç–æ–≤ –≤ —Ü–µ–Ω—Ç—Ä–∞–ª—å–Ω—ã–π –≥–µ–Ω–æ–º, –ø–æ–¥ –∫–æ–Ω—Ç—Ä–æ–ª—å —Ä–µ–≥—É–ª—è—Ç–æ—Ä–Ω—ã—Ö —Å–∏—Å—Ç–µ–º –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã, –æ–∫–∞–∑–∞–ª—Å—è —Å–∏–ª—å–Ω–æ –∑–∞—Ç—Ä—É–¥–Ω–µ–Ω. –í —Ä–µ–∑—É–ª—å—Ç–∞—Ç–µ –Ω–æ–≤—ã–µ —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–Ω—Ç—ã (–∏ —ç–Ω–¥–æ–ø–∞—Ä–∞–∑–∏—Ç—ã) —Å–æ—Ö—Ä–∞–Ω—è—é—Ç –Ω–µ —Ç–æ–ª—å–∫–æ –æ—Ç–Ω–æ—Å–∏—Ç–µ–ª—å–Ω—É—é —Å–∞–º–æ—Å—Ç–æ—è—Ç–µ–ª—å–Ω–æ—Å—Ç—å, –Ω–æ –∏ —Å–ø–æ—Å–æ–±–Ω–æ—Å—Ç—å –∫ —ç–≥–æ–∏—Å—Ç–∏—á–µ—Å–∫–æ–π —ç–≤–æ–ª—é—Ü–∏–∏.
–ë–æ–ª–µ–µ —Ç–æ–≥–æ, –ø–æ—Å–∫–æ–ª—å–∫—É —É –ø—Ä–æ–∫–∞—Ä–∏–æ—Ç –Ω–µ—Ç —Å—Ç–æ–ª—å –∂–µ—Å—Ç–∫–∏—Ö –æ–≥—Ä–∞–Ω–∏—á–µ–Ω–∏–π –ª–∞—Ç–µ—Ä–∞–ª—å–Ω–æ–≥–æ –ø–µ—Ä–µ–Ω–æ—Å–∞, —ç—Ç–∏ –Ω–æ–≤—ã–µ –æ–±–∏—Ç–∞—Ç–µ–ª–∏ —ç–≤–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–æ–π –∫–ª–µ—Ç–∫–∏ –∏–º–µ—é—Ç –≤–æ–∑–º–æ–∂–Ω–æ—Å—Ç—å –≤–∫–ª—é—á–∏—Ç—å –≤ —Å–≤–æ–π –≥–µ–Ω–æ–º –∏ –∑–∞—Ç–µ–º –∏—Å–ø–æ–ª—å–∑–æ–≤–∞—Ç—å –≤ —Å–≤–æ–∏—Ö —Ü–µ–ª—è—Ö —Ä–∞–∑–Ω–æ–æ–±—Ä–∞–∑–Ω—ã–µ —Ä–µ–≥—É–ª—è—Ç–æ—Ä–Ω—ã–µ –≥–µ–Ω—ã —Ö–æ–∑—è–µ–≤. –ò–º–µ–Ω–Ω–æ —Ç–∞–∫–∏–º –æ–±—Ä–∞–∑–æ–º, –ø–æ-–≤–∏–¥–∏–º–æ–º—É, –≤–Ω—É—Ç—Ä–∏–∫–ª–µ—Ç–æ—á–Ω—ã–µ –±–∞–∫—Ç–µ—Ä–∏–∏ –æ–±–∑–∞–≤–µ–ª–∏—Å—å –∞–Ω–∫–∏—Ä–∏–Ω–æ–≤—ã–º–∏ –±–µ–ª–∫–∞–º–∏ — —ç–≤–∫–∞—Ä–∏–æ—Ç–∏—á–µ—Å–∫–∏–º–∏ —Ä–µ–≥—É–ª—è—Ç–æ—Ä–∞–º–∏ —Ü–∏—Ç–æ—Å–∫–µ–ª–µ—Ç–∞, –º–∏—Ç–æ–∑–∞ –∏ –¥—Ä—É–≥–∏—Ö –≤–∞–∂–Ω—ã—Ö —Ñ—É–Ω–∫—Ü–∏–π, –≤–∫–ª—é—á–∞—è –∞–ø–æ–ø—Ç–æ–∑ — –ø—Ä–æ–≥—Ä–∞–º–º–∏—Ä—É–µ–º—É—é –∫–ª–µ—Ç–æ—á–Ω—É—é —Å–º–µ—Ä—Ç—å (Shohat et al., 2002; Dong, 2004; Wu et al., 2004). –í –∏—Ç–æ–≥–µ —Å–ª–æ–∂–∏–ª–∞—Å—å —Å–∏—Ç—É–∞—Ü–∏—è, –∑–µ—Ä–∫–∞–ª—å–Ω–æ –ø—Ä–æ—Ç–∏–≤–æ–ø–æ–ª–æ–∂–Ω–∞—è —Ç–æ–π, –∫–æ—Ç–æ—Ä–∞—è –∏–º–µ–ª–∞ –º–µ—Å—Ç–æ –ø—Ä–∏ —Å—Ç–∞–Ω–æ–≤–ª–µ–Ω–∏–∏ —ç–Ω–¥–æ—Å–∏–º–±–∏–æ–∑–∞ —Å –ø—Ä–æ—Ç–æ–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º–∏.
–¢–∞–∫–∏–º –æ–±—Ä–∞–∑–æ–º, –ø–æ –Ω–∞—à–µ–º—É –º–Ω–µ–Ω–∏—é, –æ–¥–Ω–∏–º –∏–∑ –æ–ø—Ä–µ–¥–µ–ª—è—é—â–∏—Ö —Ñ–∞–∫—Ç–æ—Ä–æ–≤ —Å—Ç–∞–Ω–æ–≤–ª–µ–Ω–∏—è —É—Å–ø–µ—à–Ω–æ–≥–æ –∏ –ø–µ—Ä—Å–ø–µ–∫—Ç–∏–≤–Ω–æ–≥–æ –≤ —ç–≤–æ–ª—é—Ü–∏–æ–Ω–Ω–æ–º –æ—Ç–Ω–æ—à–µ–Ω–∏–∏ —Å–∏–º–±–∏–æ–∑–∞ –ø—Ä–æ—Ç–æ—ç–≤–∫–∞—Ä–∏–æ—Ç —Å –ø—Ä–æ—Ç–æ–º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏—è–º–∏ –±—ã–ª–∞ –ø–æ—Å—Ç—É–ª–∏—Ä–æ–≤–∞–Ω–Ω–∞—è –Ω–∞–º–∏ —Ä–∞–Ω–µ–µ –ø–æ–≤—ã—à–µ–Ω–Ω–∞—è —Å–ø–æ—Å–æ–±–Ω–æ—Å—Ç—å –ø—Ä–µ–¥–∫–∞ –Ω—É–∫–ª–µ–æ—Ü–∏—Ç–æ–ø–ª–∞–∑–º—ã –∫ –∏–Ω–∫–æ—Ä–ø–æ—Ä–∞—Ü–∏–∏ —á—É–∂–µ—Ä–æ–¥–Ω–æ–≥–æ –≥–µ–Ω–µ—Ç–∏—á–µ—Å–∫–æ–≥–æ –º–∞—Ç–µ—Ä–∏–∞–ª–∞, –∫–æ—Ç–æ—Ä–∞—è —Ä–∞–∑–≤–∏–ª–∞—Å—å –≤ —Å–≤—è–∑–∏ —Å —Ä–æ—Å—Ç–æ–º –∫–æ–Ω—Ü–µ–Ω—Ç—Ä–∞—Ü–∏–∏ —Å–≤–æ–±–æ–¥–Ω–æ–≥–æ –∫–∏—Å–ª–æ—Ä–æ–¥–∞ –≤ —Å—Ä–µ–¥–µ, –≤—ã–∑–≤–∞–Ω–Ω–æ–≥–æ –ø–µ—Ä–µ—Ö–æ–¥–æ–º —á–∞—Å—Ç–∏ —Ñ–æ—Ç–æ–∞–≤—Ç–æ—Ç—Ä–æ—Ñ–Ω—ã—Ö –±–∞–∫—Ç–µ—Ä–∏–π –∫ –æ–∫—Å–∏–≥–µ–Ω–Ω–æ–º—É —Ñ–æ—Ç–æ—Å–∏–Ω—Ç–µ–∑—É. –ü–∞–ª–µ–æ–Ω—Ç–æ–ª–æ–≥–∏—á–µ—Å–∫–∏–µ –¥–∞–Ω–Ω—ã–µ –ø–æ–∑–≤–æ–ª—è—é—Ç –ø—Ä–µ–¥–ø–æ–ª–æ–∂–∏—Ç–µ–ª—å–Ω–æ –¥–∞—Ç–∏—Ä–æ–≤–∞—Ç—å –ø–æ—è–≤–ª–µ–Ω–∏–µ —ç–≤–∫–∞—Ä–∏–æ—Ç –∏–Ω—Ç–µ—Ä–≤–∞–ª–æ–º –æ—Ç 3.0 –¥–æ 2.5 –º–ª—Ä–¥. –ª–µ—Ç –Ω–∞–∑–∞–¥ (–¢–∏–º–æ—Ñ–µ–µ–≤, 1982; Brocks et al., 1999; –Ý–æ–∑–∞–Ω–æ–≤, 2003).
–Ý–∞–±–æ—Ç–∞ –≤—ã–ø–æ–ª–Ω–µ–Ω–∞ –≤ —Ä–∞–º–∫–∞—Ö –ø–æ–¥–ø—Ä–æ–≥—Ä–∞–º–º—ã 2 –ü—Ä–æ–≥—Ä–∞–º–º—ã 25 –ü—Ä–µ–∑–∏–¥–∏—É–º–∞ –Ý–ê–ù «–ü—Ä–æ–∏—Å—Ö–æ–∂–¥–µ–Ω–∏–µ –∏ —ç–≤–æ–ª—é—Ü–∏—è –±–∏–æ—Å—Ñ–µ—Ä—ã».
–°–ø–∏—Å–æ–∫ –ª–∏—Ç–µ—Ä–∞—Ç—É—Ä—ã
–ó–∞–≤–∞—Ä–∑–∏–Ω –ì.–ê. –°—Ç–∞–Ω–æ–≤–ª–µ–Ω–∏–µ –±–∏–æ—Å—Ñ–µ—Ä—ã // –í–µ—Å—Ç–Ω. –Ý–ê–ù. 2001. –¢. 71. ‚Ññ 11. –°. 988 — 1001.
–ó–∞—Ö–∞—Ä–æ–≤ –ò.–ê. –ë–∞–∫—Ç–µ—Ä–∏–∏ —É–ø—Ä–∞–≤–ª—è—é—Ç –ø–æ–ª–æ–≤—ã–º —Ä–∞–∑–º–Ω–æ–∂–µ–Ω–∏–µ–º –Ω–∞—Å–µ–∫–æ–º—ã—Ö // –ü—Ä–∏—Ä–æ–¥–∞. 1999. ‚Ññ5. –°. 28-34.
–ó–∞—Ö–∞—Ä–æ–≤ –ò.–ê., –ì–æ—Ä—è—á–µ–≤–∞ –ò.–ò., –®–∞–π–∫–µ–≤–∏—á –ï.–í. –∏ –¥—Ä. Wolbachia, –Ω–æ–≤—ã–π –±–∞–∫—Ç–µ—Ä–∏–∞–ª—å–Ω—ã–π –∞–≥–µ–Ω—Ç, –≤—ã–∑—ã–≤–∞—é—â–∏–π –∏–∑–º–µ–Ω–µ–Ω–∏–µ —Å–æ–æ—Ç–Ω–æ—à–µ–Ω–∏—è –ø–æ–ª–æ–≤ —É –¥–≤—É—Ç–æ—á–µ—á–Ω–æ–π –±–æ–∂—å–µ–π –∫–æ—Ä–æ–≤–∫–∏ Adalia bipunctata L. // –ì–µ–Ω–µ—Ç–∏–∫–∞. 2000. –¢. 36. ‚Ññ 4. –°. 482-486.
–ö—É–ª–∏–Ω—Å–∫–∏–π –í.–ò. –ü–µ—Ä–µ–¥–∞—á–∞ –∏ —Ç—Ä–∞–Ω—Å–¥—É–∫—Ü–∏—è –≥–æ—Ä–º–æ–Ω–∞–ª—å–Ω–æ–≥–æ —Å–∏–≥–Ω–∞–ª–∞ –≤ —Ä–∞–∑–Ω—ã–µ —á–∞—Å—Ç–∏ –∫–ª–µ—Ç–∫–∏ // –°–æ—Ä–æ—Å–æ–≤—Å–∫–∏–π –æ–±—Ä–∞–∑–æ–≤–∞—Ç–µ–ª—å–Ω—ã–π –∂—É—Ä–Ω. 1997. ‚Ññ 8. –°. 14-19.
–õ–∏—Ç–æ—à–µ–Ω–∫–æ –ê.–ò. –≠–≤–æ–ª—é—Ü–∏—è –º–∏—Ç–æ—Ö–æ–Ω–¥—Ä–∏–π // –¶–∏—Ç–æ–ª–æ–≥–∏—è. –ì–µ–Ω–µ—Ç–∏–∫–∞. 2002. –¢. 36. ‚Ññ 5. –°. 49-57.
–ú–∞–ª—å—Ü–µ–≤–∞ –ë.–ú. –°–∏–º–±–∏–æ—Ç–∏—á–µ—Å–∫–∞—è —Å–∏—Å—Ç–µ–º–∞ — —Ñ–∏–ª—è—Ä–∏–∏ –∏ –±–∞–∫—Ç–µ—Ä–∏—è Wolbachia: —ç–≤–æ–ª—é—Ü–∏—è —Å–∏—Å—Ç–µ–º—ã, –ø–∞—Ç–æ–≥–µ–Ω–µ–∑ –∏ –ª–µ—á–µ–Ω–∏–µ —Ñ–∏–ª—è—Ä–∏–∞—Ç–æ–∑–æ–≤ // –í–µ—Ç–µ—Ä–∏–Ω–∞—Ä–∏—è. 2004. ‚Ññ 1. –°. 34-38.
–ú–∞—Ä–∫–æ–≤ –ê.–í. –ü—Ä–æ–±–ª–µ–º–∞ –ø—Ä–æ–∏—Å—Ö–æ–∂–¥–µ–Ω–∏—è —ç—É–∫–∞—Ä–∏–æ—Ç // –ü–∞–ª–µ–æ–Ω—Ç–æ–ª. –∂—É—Ä–Ω. 2005. –í –ø–µ—á–∞—Ç–∏.
–ú–∞—Ä–∫–æ–≤ –ê.–í., –ö—É–ª–∏–∫–æ–≤ –ê.–ú. –ü—Ä–æ–∏—Å—Ö–æ–∂–¥–µ–Ω–∏–µ —ç–≤–∫–∞—Ä–∏–æ—Ç: –≤—ã–≤–æ–¥—ã –∏–∑ –∞–Ω–∞–ª–∏–∑–∞ –±–µ–ª–∫–æ–≤—ã—Ö –≥–æ–º–æ–ª–æ–≥–∏–π –≤ —Ç—Ä–µ—Ö –Ω–∞–¥—Ü–∞—Ä—Å—Ç–≤–∞—Ö –∂–∏–≤–æ–π –ø—Ä–∏—Ä–æ–¥—ã // –ü–∞–ª–µ–æ–Ω—Ç–æ–ª. –∂—É—Ä–Ω. 2005. –í –ø–µ—á–∞—Ç–∏.
–Ý–∞—Ç–Ω–µ—Ä –í.–ê., –í–∞—Å–∏–ª—å–µ–≤–∞ –õ.–ê. –ú–æ–±–∏–ª—å–Ω—ã–µ –≥–µ–Ω–µ—Ç–∏—á–µ—Å–∫–∏–µ —ç–ª–µ–º–µ–Ω—Ç—ã (–ú–ì–≠) –∏ —ç–≤–æ–ª—é—Ü–∏—è –≥–µ–Ω–æ–º–æ–≤ // –°–æ–≤—Ä–µ–º–µ–Ω–Ω—ã–µ –ø—Ä–æ–±–ª–µ–º—ã —Ç–µ–æ—Ä–∏–∏ —ç–≤–æ–ª—é—Ü–∏–∏. –ú.: –ù–∞—É–∫–∞, 1993. –°. 43-59.
–Ý–æ–∑–∞–Ω–æ–≤ –ê.–Æ. –ò—Å–∫–æ–ø–∞–µ–º—ã–µ –±–∞–∫—Ç–µ—Ä–∏–∏, —Å–µ–¥–∏–º–µ–Ω—Ç–æ–≥–µ–Ω–µ–∑ –∏ —Ä–∞–Ω–Ω–∏–µ —Å—Ç–∞–¥–∏–∏ —ç–≤–æ–ª—é—Ü–∏–∏ –±–∏–æ—Å—Ñ–µ—Ä—ã // –ü–∞–ª–µ–æ–Ω—Ç–æ–ª. –∂—É—Ä–Ω. 2003. ‚Ññ 6. –°. 41 — 49.
–¢–∏–º–æ—Ñ–µ–µ–≤ –ë.–í. –ú–∏–∫—Ä–æ—Ñ–æ—Å—Å–∏–ª–∏–∏ —Ä–∞–Ω–Ω–µ–≥–æ –¥–æ–∫–µ–º–±—Ä–∏—è. –õ.: –ù–∞—É–∫–∞, 1982. 128 —Å.
Andersson S.G., Zomorodipour A., Andersson J.O. et al. The genome sequence of Rickettsia prowazekii and the origin of mitochondria // Nature. 1998. V. 396. N 6707. P. 133-140.
Bandi C., Anderson T.J.C., Genchi C., Blaxter M.L. Phylogeny of Wolbachia-like bacteria in filarial nematodes // Proc. R. Soc. London. Ser. B. 1998. V. 265. P. 2407–2413.
Bordenstein S.R., Wernegreen J.J. Bacteriophage flux in endosymbionts (Wolbachia): infection frequency, lateral transfer, and recombination rates // Mol. Biol. Evol. 2004. V. 21. ‚Ññ 10. P. 1981-1991.
Boussau B., Karlberg E.O., Frank A.C. et al. Computational inference of scenarios for alphaproteobacterial genome evolution // Proc. Natl. Acad. Sci. USA. 2004. V. 101. ‚Ññ 26. P. 9722-9727.
Bressac C., Rousset F. The reproductive incompatibility system in Drosophila simulans: Dapi-staining analysis of the Wolbachia symbionts in sperm cysts // J. Invert. Pathol. 1993. V.61. P.226–230.
Brocks J.J., Logan G.A., Buick R., Summons R.E. Archean molecular fossils and the early rise of eukaryotes // Science. 1999. V. 285. ‚Ññ 5430. P. 1025-1027.
Callaini G., Dallai R., Riparbelli M.G. Wolbachia-induced delay of paternal chromatin condensation does not prevent maternal chromosomes from entering anaphase in incompatible crosses of Drosophila simulans // J. Cell. Sci. 1997. V. 110. P. 271–280.
Chirgwin S.R., Coleman S.U., Porthouse K.H. et. al. Removal of Wolbachia from Brugia pahangi is closely linked to worm death and fecundity but does not result in altered lymphatic lesion formation in Mongolian gerbils (Meriones unguiculatus) // Infect. Immun. 2003. V. 71. ‚Ññ 12. P. 6986–6994.
Cummins J.M. Mitochondria: potential roles in embryogenesis and nucleocytoplasmic transfer // Human Reproduction Update. 2001. V. 7. ‚Ññ 2. P. 217 — 228.
Dolan M.F., Melnitsky H., Margulis L., Kolnicki R. Motility proteins and the origin of the nucleus // Anat. Rec. 2002. ‚Ññ 268. P. 290-301.
Dong X. The role of membrane-bound ankyrin-repeat protein ACD6 in programmed cell death and plant defense // Sci STKE. 2004. V. 221. P. e6.
Dyall S.D., Johnson P.J. Origins of hydrogenosomes and mitochondria: evolution and organelle biogenesis // Curr. Opin. Microbiol. 2000. V. 3. ‚Ññ 4. P. 404-411.
Dyer K.A., Jaenike J. Evolutionarily stable infection by a male-killing endosymbiont in Drosophila innubila: molecular evidence from the host and parasite genomes // Genetics. 2004. V. 168. ‚Ññ 3. P. 1443-1455.
Emelyanov V.V. Common evolutionary origin of mitochondrial and rickettsial respiratory chains // Arch. Biochem. Biophys. 2003. V. 420. ‚Ññ 1. P. 130-141.
Esser C., Ahmadinejad N., Wiegand C. et al. A genome phylogeny for mitochondria among alpha-proteobacteria and a predominantly eubacterial ancestry of yeast nuclear genes // Mol. Biol. Evol. 2004. V. 21. ‚Ññ 9. P.1643-1660.
Gabaldon T., Huynen M.A. Reconstruction of the proto-mitochondrial metabolism // Science. 2003. V. 301. ‚Ññ 5633. P. 609.
Gavotte L., Vavre F., Henri H. et al. Diversity, distribution and specificity of WO phage infection in Wolbachia of four insect species // Insect Mol. Biol. 2004. V. 13. ‚Ññ 2. P. 147-153.
Girin C, Bouletreau M. Microorganism-associated variation in host infestation efficiency in a parasitoid wasp Trichogramma bourarachae // Experientia. 1995. V. 52. P. 398–402.
Gupta R.S. Protein phylogenies and signature sequences: a reappraisal of evolutionary relationships among Archaebacteria, Eubacteria, and Eukaryotes // Microbiol. and Molecul. Biol. Rev. 1998. V. 62. ‚Ññ 4. P. 1435-1491.
Hariri A.R., Werren J.H., Wilkinson G.S. Distribution and reproductive effects of Wolbachia in stalk-eyed flies (Diptera: Diopsidae) // Heredity. 1998. V. 81. P. 254-260.
Heath B.D., Butcher R.D., Whitfield W.G., Hubbard S.F. Horizontal transfer of Wolbachia between phylogenetically distant insect species by a naturally occurring mechanism // Curr Biol. 1999. V. 9. ‚Ññ 6. P. 313-316.
Hurst G.D.D., Jiggins F.M., Schulenburg J. H.G. et al. Male-killing Wolbachia in two species of insect // Proc.R.Soc.Lond.Ser.B.1999. V. 266. P.735-740.
Hurst G.D., Johnson A.P., Schulenburg J.H., Fuyama Y. Male-killing Wolbachia in Drosophila: a temperature-sensitive trait with a threshold bacterial density // Genetics. 2000. V. 156. ‚Ññ 2. P. 699-709.
Jiggins F.M., Hurst G.D.D., Majerus M.E.N. Sex ratio distortion in Acraea encedon is caused by a male-killing bacterium // Heredity. 1998. V.81. P. 87–91.
Karlberg O. Mitochondrial evolution: turning bugs into features. // Comprehensive Summaries of Uppsala Dissert. Fac. Sci. and Technol. 2004. V. 961. P. 1-37.
Kurland C.G., Andersson S.G. E. Origin and evolution of the mitochondrial proteome // Microbiol. and Molecul. Biol. Rev. 2000. V. 64. ‚Ññ. 4. P. 786-820.
LeGrand J.-J., LeGrand-Hamelin E., Juchault P. Sex determination in Crustacea // Biol. Rev. 1987. V.62. P. 439–470.
Marc P., Margeot A., Devaux F. et al. Genome-wide analysis of mRNAs targeted to yeast mitochondria // EMBO Rep. 2002. V. 3. ‚Ññ 2. P. 159-164.
Martin W. Gene transfer from organelles to the nucleus: Frequent and in big chunks // Proc. Natl. Acad. Sci. USA. 2003. V. 100. ‚Ññ 15. P. 8612-8614.
Martin W., Herrmann-Reinhold G. Gene transfer from organelles to the nucleus: how much, what happens, and why? // Plant Physiol. 1998. V. 118. P. 9-17.
Martin W., Russell M.J. On the origins of cells: a hypothesis for the evolutionary transitions from abiotic geochemistry to chemoautotrophic prokaryotes, and from prokaryotes to nucleated cells // Phil. Trans. R. Soc. Lond. Ser. B. 2003. V. 358. ‚Ññ 1429. P. 59-85.
Masui S., Sasaki T., Ishikawa H. Genes for the type IV secretion system in an intracellular symbiont, Wolbachia, a causative agent of various sexual alterations in arthropods // J. Bacteriol. 2000. V.182. P.6529-6531.
Noda H, Miyoshi T, Koizumi Y. In vitro cultivation of Wolbachia in insect and mammalian cell lines // In Vitro Cell Dev. Biol. Anim. 2002. V. 38. ‚Ññ 7. P. 423-427.
Rand D.M., Clark A.G., Kann L.M. Sexually antagonistic cytonuclear fitness interactions in Drosophila melanogaster // Genetics. 2001. V. 159. P. 173-187.
Rehling P., Wiedemann N., Pfanner N., Truscott K.N. The mitochondrial import machinery for preproteins // Crit. Rev. Biochem. Mol. Biol. 2001. V. 36. ‚Ññ 3. P. 291-336.
Reichert A.S., Neupert W. Mitochondriomics or what makes us breathe // Trends in genetics. 2004. V. 20. ‚Ññ 11. P. 555-562.
Richardson P.M., Holmes W.P., Saul G.B. 1987. The effect of tetracycline on reciprocal cross incompatibility in Mormoniella [=Nasonia] vitripennis // J. Invert. Pathol. 1987. V. 50. P. 176–183.
Roger A.J. Reconstructing early events in eukaryotic evolution // Amer. Nat. 1999. V. 154. ‚Ññ S4. P. S146 — S163.
Schneider A., Ebert D. Covariation of mitochondrial genome size with gene lengths: evidence for gene length reduction during mitochondrial evolution // J. Mol. Evol. 2004. V. 59. ‚Ññ 1. P. 90-96.
Schopf J.W. (ed.) Earth's earliest biosphere: Its origin and evolution. Princeton: Univ. Press, 1983. 544 p.
Seshadri R., Paulsen I.T., Eisen J.A. et al. Complete genome sequence of the Q-fever pathogen Coxiella burnetii // Proc. Natl. Acad. Sci. USA. 2003. V. 100. P. 5455–5460.
Shohat G., Spivak-Kroizman T., Eisenstein M., Kimchi A. The regulation of death-associated protein (DAP) kinase in apoptosis // Eur Cytokine Netw. 2002. V. 13. ‚Ññ 4. P. 398-400.
Stouthamer R., Breeuwer J.A.J., Hurst G.D.D. Wolbachia pipientis: microbial manipulator of arthropod reproduction // Annu. Rev. Microbiol. 1999. V. 53. P. 71–102.
Stouthamer R., Kazmer D.J. Cytogenetics of microbe-associated parthenogenesis and its consequences for gene flow in Trichogramma wasps // Heredity. 1994. V.73. P. 317–327.
Van Borm S., Wenseleers T., Billen J., Boomsma J.J. Wolbachia in leafcutter ants: a widespread symbiont that may induce male killing or incompatible matings // J. Evol. Biol. 2001. V. 14. ‚Ññ 5. P. 805-814.
Van Meer M.M., Witteveldt J., Stouthamer R. Phylogeny of the arthropod endosymbiont Wolbachia based on the wsp gene // Insect Mol Biol. 1999. V. 8. ‚Ññ 3. P. 399-408.
Vasilyeva L.A., Bubenshchikova E.V., Ratner V.A. Heavy heat shock induced retrotransposon transposition in Drosophila // Genet Res. 1999. V. 74. ‚Ññ 2. P. 111-119.
Vellai T., Takacs K., Vida G. A new aspect to the origin and evolution of eukaryotes // J. Mol. Evol. 1998. V. 46. ‚Ññ 5. P. 499-507.
Vellai T., Vida G. The origin of eukaryotes: the difference between prokaryotic and eukaryotic cells // Proc. R. Soc. Lond. Ser. B. 1999. V. 266. ‚Ññ 1428. P. 1571-1577.
Werren J.H. Biology of Wolbachia // Annu. Rev. Entomol. 1997. V. 42. P.587–609.
Werren J.H.,Windsor D., Guo L. Distribution of Wolbachia among neotropical arthropods // Proc. R. Soc. London Ser. B. 1995a. V. 262. P. 197–204.
Werren J.H., Zhang W., Guo L.R. Evolution and phylogeny of Wolbachia: reproductive parasites of arthropods. // Proc. R. Soc. Lond. Ser. B. 1995b. V. 261. P. 55–63.
Wu M., Sun L.V., Vamathevan J. et al. Phylogenomics of the reproductive parasite Wolbachia pipientis wMel: a streamlined genome overrun by mobile genetic elements // PLoS Biol. 2004. V.2. ‚Ññ 3. P. 327-341.
PARASITIC BACTERIUM WOLBACHIA AND THE ORIGIN OF EUKARYOTIC CELL
© 200_ –≥. A.V.Markov 1, I.A.Zakharov 2
1Paleontological Institute RAS
E-mail: markov_a@inbox.ru
2Vavilov Institute of General Genetics RAS
E-mail: zakharov@vigg.ru
Acquisition of endosymbiotic alphaproteobacteria that gave rise to mitichondria was one of the key events in the origin of eukaryotic cell. To reconstruct this process, it is important to analyse relations that developed later between the eukaryotes and other alphaproteobacteria. Wolbachia pipientis, a bactrerium that inhabits cells of numerous terrestrial invertebrates and exerts diverse effects on its hosts, is taken as a model object. Although Wolbachia is similar to mitochondria in many important features (basic metabolism, small molecules membrane transport, envelope structure, etc.), their relationships with nucleocytoplasm are different. Mitochondria import most of required proteins from the nucleocytoplasm and are under the control of nucleocytoplasmic regulatory systems. On the contrary, Wolbachia exports its proteins into the host's cytoplasm, thus causing dramatic aberrations in the ontogeny and reproduction of the host. This difference may be due to the fact that most of the protomitochondrial genes had been transferred into the central (nuclear) genome at the early stages of development of endosymbiotic system, while Wolbachia genes were not transferred into the nucleus. This fits well to the hypothesis suggested previously, that there was a period of rapid lateral gene transfer in the evolution of proto-eukaryotes; acquisition of mitochondria took place during this period. Later eukaryotes, and especially metazoans, developed powerful mechanisms for prevention of lateral gene transfer. Therefore the genes of the newly acquired endosymbionts can not be transferred into the central genome, and the endosymbionts retain the ability for egoistic evolution.
Key words: origin of eukaryotic cell, symbiogenesis, lateral gene transfer, Wolbachia, alphaproteobacteria