
Проблемы Эволюции |
Сенсационная книга австралийских иммунологов. Популярно изложено строение иммунной системы позвоночных и механизм образования новых специфических антител методом соматического "гипермутирования" иммуноглобулиновых генов и отбора лимфоцитов. Обоснована гипотеза о возможном механизме наследования приобретенных признаков в иммунной системе. (М.: Мир, 2002. 237 с.)
Организм человека постоянно подвергается нападению агрессивных патогенных вирусов и бактерий. Как иммунной системе удается отбивать эти атаки? Как она различает, где «свои» и где «чужие»? Каким образом наш организм быстро создает целые армии новых антител для борьбы с доселе неизвестными патогенами? Каковы механизмы иммунологической памяти, позволяющей клеткам иммунной системы эффективнее бороться с возбудителем при повторной встрече с ним. Если хоть на минуту задуматься над этими вопросами, можно понять, что научное и философское значение ответов на них выходит за узкие рамки иммунной системы. Именно поэтому иммунная система столь интересна для исследования, а за работы, раскрывающие механизмы иммунитета, присуждено так много Нобелевских премий.
В этой и двух следующих главах (гл. 4 и 5) мы расскажем о развитии иммунологии, об эволюции иммунной системы позвоночных и о современных молекулярно-генетических исследованиях в этой области. По мере того как мы находим ответы на поставленные вопросы, нашим глазам открываются все новые научные, практические и этические проблемы. В свете этих новых знаний, многое из того, что раньше нам казалось незыблемым, сейчас представляется спорным. В иммунологии сошлись все современные идеи генетики, теории развития и теории эволюции. Наша задача показать, что недавние научные открытия ставят под вопрос неодарвинистские концепции эволюции. В гл. 6 мы изложим свои представления о том, как сложные молекулярные процессы в иммунной системе могут приводить к переносу генетической информации из соматических клеток в половые. Эта концепция составляет главную тему нашей книги, а именно что признаки, приобретенные в течение жизни, могут передаваться потомкам.
Основные понятия иммунологии
• Антиген
Антигены - чужеродные белки и углеводы, которые стимулируют образование специфических антител, связывающихся с данным антигеном, но не с другими неродственными антигенами. Собственные антигены - белки или углеводы, которые являются составной частью данного организма. В норме иммунного ответа против собственных антигенов нет.
• Антигены гистосовместимости/киллерные Т-клетки
Антигены гистосовместимости называются также антигенами главного комплекса гис-тосовместимости, или ШС-антигенами. Эти антигены проявляются в большинстве клеток тела. Киллерные Т-клетки одного индивида могут распознавать МНС-антигены другого неидентичного индивида и реагировать на них, отторгая пересаженные ткани. МНС-антигены также действуют как антигенпрезентирующие структуры, например, представляя фрагменты вирусных белков (пептиды) киллерным Т-клеткам, активируя их и заставляя атаковать и лизировать зараженные клетки.
• Антитело
Белок, продуцируемый В-лимфоцитом (белая кровяная клетка) в ответ на чужеродный антиген (бактериальные клетки, вирусные частицы и их токсичные продукты). Типичное строение имеет иммуноглобулин G (IgG) - белковый гетеродимер (рис. 3.2). Существует множество разных антител, каждое из которых распознает определенный антиген.
• Вариабельная (V-) область/антигенсвязывающии центр
На концах как Н-, так и 1-цепей находится вариабельная (изменчивая) последовательность аминокислот (рис. 3.2). Эта область называется также антигенсвязываю-щим центром. V-области образуют антигенсвязывающий центр антитела (или Т-кле-точного рецептора).
• В-лимфоциты
Развивающиеся в костном мозге белые кровяные клетки, продуцирующие антитела. В-клетки связываются и отбираются антигеном, что приводит к активации выделения антител или пролиферации клеток.
• Гаптены
Небольшие химические соединения (бензольные кольца и их производные), созданные химиками, которые сами по себе не способны вызвать образование антител. Если гаптены присоединены к крупному «носителю» (чужеродному белку), их можно использовать для индукции анти-гаптеновых антител.
• Гены «домашнего хозяйства»
(от англ. housekeeping - домашнее хозяйство) Все жизненно необходимые гены, белковые или РНК продукты которых существенны для основных функций клетки (например, ферменты энергетических путей, ферменты репликации ДНК и т.д.)
• Иммуноглобулин
Название белка антитела, сокращенно Ig. Существует пять классов иммуноглобули-нов: 1дМ, IgD, IgG, IgA, IgE. Классификация основана на последовательности аминокислот С-областей Н-цепей; каждый класс Ig выполняет свою функцию.
• Клональная селекция/специфичность антител
На поверхности каждой отдельной зрелой В-клетки проявляются антитела одной специфичности, т.е. для синтеза каждой молекулы Ig используется один набор генов вариабельной области антитела. Чужеродный антиген, попадающий в организм, стимулирует только те В-клетки, с которыми он может связываться. Эти клетки активируются и начинают делиться (пролиферируют), образуя клон специфичных В-клеток, причем все потомки имеют идентичную специфичность (рис. 4.1).
• Константная (С) область/классы иммуноглобулинов
Аминокислотная последовательность молекулы антитела, которая не принимает участия в связывании антигена и, следовательно, не меняется от одной молекулы к дру-8 гой. Константные С-области тяжелых цепей определяют функцию антитела, например, способность запустить фагоцитоз. С-области тяжелых цепей подразделяются на пять основных типов последовательностей (и, следовательно, функций), называемых классами иммуноглобулинов (см. выше).
• Протестом
Единица «защиты» определена как минимальная критическая концентрация специфичного антитела в крови, необходимая для защиты против инфекции.
• Т-лимфоциты
Развивающиеся в тимусе белые кровяные клетки, на поверхности которых экспресси-руются сходные с антителами молекулы, называемые Т-клеточными рецепторами (ТкР). Существует два типа Т-клеток: киллерные Т-клетки и хвлперные Т-клетки.
• Фагоциты/фагоцитоз
Фагоциты - белые кровяные клетки, которые захватывают (фагоцитируют) и переваривают бактерии и клеточные обломки.
• Цитокины/интерфероны
Белки, выделяемые активированными хелперными Т-клетками, которые дают сигналы к активации и дифференцировке другом белым кровяным клеткам, включая другие Т- и В-клетки.
Начать это путешествие в знание мы должны с объяснения некоторых понятий. Нам необходимо рассмотреть наиболее важные клетки, молекулы и гены иммунной системы и дать определения основных терминов (табл. 3.1 и 5.1).
Краткая история прививок и вакцинаций
Научные основы вакцинации были заложены в XVIII—XIX столетиях. В Европе прививка в качестве защитной меры от оспы была впервые предложена леди Мэри Уортли Монтагью (Montagu). Эта женщина в 22-летнем возрасте перенесла жестокую оспу, оставившую следы на ее лице. В 1717 г. леди Монтагью вместе со своим мужем, британским послом в Константинополе, путешествовала по Турции. Ее внимание привлек местный обычай, называемый «прививкой». В письме на родину, датированном 1 апреля 1717 г., она писала: «Оспа, такая страшная и беспощадная у нас, здесь довольно безвредна. Местные старухи каждую осень ходят из дома в дом с ореховой скорлупой, полной оспенных корочек, и предлагают сделать «прививки». Через восемь дней решившиеся на эту процедуру как прежде здоровы» (и иммунизированы против оспы).
Леди Монтагью сразу поняла смысл этого обычая и рассказала о нем английским врачам. Доктор Чарльз Майтланд (Maitland) привил оспу ее сыну и дочери. Она добилась разрешения короля на прививку шести заключенных из Ньюгейтской тюрьмы. Эту прививку также провел доктор Майтланд. Испытания оказались успешными, после чего принцесса Уэльсская захотела привить своих дочерей. Заметим, что в Китае и Индии прививку оспы практиковали за несколько столетий до ее введения в Европе. Болячками больного оспой расцарапывали кожу здорового человека, который обычно после этого переносил инфекцию в слабой, не смертельной форме, выздоравливал и оставался устойчивым к последующим заражениям оспой.
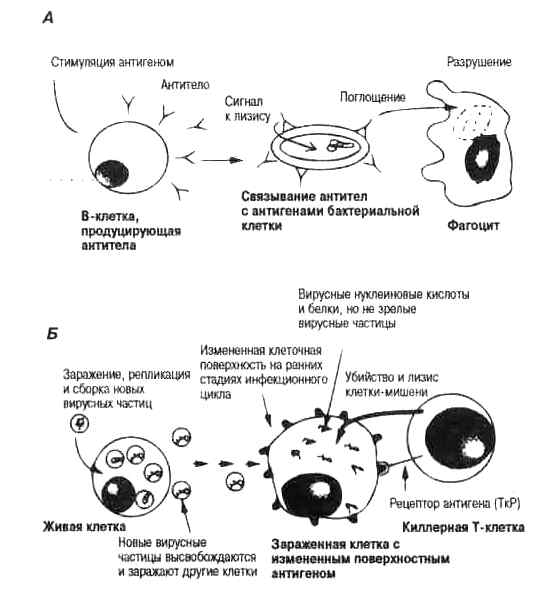
Рис. 3.1. Антитела и киллерные Т-клетки. Сильно упрощенная схема защитной роли антител и киллерных Т-клеток (основные термины см. в табл. 3.1).
А.
Вслед за стимуляцией антигеном В-клетки отбираются и активизируются для образования специфичных к данному антигену антител. Если антигеном являются бактериальные клетки (как показано на рисунке), антитела связываются с поверхностными антигенами бактерий, запуская реакции двух типов. С одной стороны, антитела могут привлекать другие белки плазмы (комплемент), которые действуют вместе с антителами, разрушая (лизируя) и, таким образом, убивая бактериальные клетки. С другой стороны, связанные антитела могут запускать поглощение и внутриклеточное переваривание бактериальных клеток особыми белыми кровяными клетками — фагоцитами (процесс переваривания называется фагоцитозом).
Б. Киллерные Т-клетки защищают от вирусных инфекций. Вирус заражает клетку и размножается. Синтезируются вирусные белки. В конце концов, происходит сборка новых вирусных частиц, которые заражают соседние клетки, вызывая, таким образом, острое заболевание. Зараженные клетки экспрессируют клеточные поверхностные антигены гистосовместимости, измененные в результате образования комплекса с фрагментами вирусного белка (пептидами). Именно этот измененный поверхностный антиген распознается Т-клетками с помощью поверхностных рецепторов (ТкР), что приводит к пролиферации и активации Т-клеток. Когда активированная Т-клетка связывается с клеткой-мишенью своими рецепторами, клетка-мишень разрушается и погибает. Так как измененный поверхностный антиген может экспресси-роваться до того, как завершится сборка зрелых вирусных частиц, Т-клетки способны разрушить эту «клеточную фабрику», т. е. предотвратить производство вирусного потомства и, таким образом, избежать дальнейшего заражения.
Большой вклад в разработку этой проблемы внес Эдуард Дженнер (Jenner). В 1798 г. он доказал, что оспу можно предупредить, если привить человеку коровью оспу, которую вызывает более слабый родственный вирус. Его исследования опирались на общее наблюдение, что доярки, переболевшие коровьей оспой, никогда не болеют во время эпидемий. Сам Дженнер помнил, что в детстве очень тяжело перенес прививку человеческой оспы, поэтому у него были личные причины улучшать метод. Прививка коровьей оспы оказалась более безопасной и легкой процедурой. С тех пор вакцинация против оспы и полиомиелита стали яркими примерами успеха профилактической медицины. В 1977 г. оспа была исключена из списка заболеваний, по которым Всемирная организация здравоохранения (ВОЗ) проводит обязательную вакцинацию.
Научные основы вакцинации были разработаны во второй половине девятнадцатого века отцом современной микробиологии и иммунологии Луи Пастером. В контролируемых испытаниях он установил эффективность использования «ослабленных», не представляющих угрозу, форм возбудителя для иммунизации против вирулентных штаммов. Ослабленные бактерии или вирусы несут те же антигены (или молекулярные признаки, распознаваемые иммунной системой), что и исходные болезнетворные штаммы, но они потеряли способность вызывать заболевание.

Рис. 3.2. Схема строения молекулы антитела. Антитела являются гетеродимерами, так как основная составляющая их единица состоит из разных белковых цепочек: тяжелой (Н) и легкой (L) цепей (см. табл. 3.1). Две Н + L-пары, образующие основную молекулу, удерживаются вместе химическими связями. Такое строение характерно для lgG-антител и связанных с клеточной поверхностью мономерных IgM (и IgD). Обратите внимание, что антигенсвязывающий центр образован взаимодействием вариабельных областей Н- и 1-цепей. Константная область Н-цепи определяет класс иммуноглобулина и защитную функцию антитела (см. табл.3.1). Внизу рисунка в рамке приведены сильно упрощенные изображения антител, которые используются в других рисунках (рис. 1.2, 3.1, 3.6, 3.7и 4.1).
И в настоящее время наиболее эффективные вакцины — ослабленные штаммы (например, против желтой лихорадки и полиомиелита). Сейчас для создания вакцин используются молекулярно-генетические методы. Этими методами в ослабленные вирусные или бактериальные штаммы вводят ДНК-последовательности, кодирующие нужные антигены, и получают чистые белковые антигены, используемые для вакцинации. Некоторые из таких вакцин нового поколения уже используются в клинике. Сейчас мы знаем, что вакцинация стимулирует образование активированных Т-лимфоцитов и защитных антител, которые помогают нашему организму ликвидировать вирусную или бактериальную инфекцию (рис. 3.1). В общих чертах структура антитела показана на рис. 3.2.
Переливание крови и начало современной иммунологии
К началу XX века стало ясно, что антитела против холеры (заболевания тонкого кишечника, сопровождающегося тяжелой диареей) высокоспецифичны, они связывают антигены холерного вибриона и неспособны связывать никакие другие антигены. За открытие специфической природы антител, роли антител и фа-гоцитирующих клеток в иммунном ответе Пауль Эрлих и Илья Мечников были удостоены Нобелевской премии. Специфичность антител всесторонне продемонстрирована в начале этого века Карлом Ландштейнером (Landsteiner). В 1930 году он был удостоен Нобелевской премии. Ему принадлежит и ряд других важных открытий. Но самые известные его работы касаются системы АВО эритроцитарных антигенов человека. Это открытие дало объяснение совместимости доноров и реципиентов при переливании крови:
Антигены эритроцитов Антитела, в плазме крови тех же людей A анти-В В анти-А АВ Нет 0 (нет ни А, ни В) анти-А и анти-В
Эритроциты (красные кровяные клетки) типа А, смешанные с плазмой крови, содержащей анти-А-антитела, слипаются (агглютинируют). Эритроциты типа А, подвергшиеся действию анти-В-плазмы, не агглютинируют. Таким образом, если человеку с группой крови А нечаянно перелита В-кровь, содержащая анти-А-антитела, в кровеносных сосудах может происходить агглютинация. Лучше всего человеку с группой крови А переливать кровь А, а человеку с группой крови В переливать кровь В. При отсутствии нужной донорской крови в случае острой необходимости людям с группами крови А или В можно переливать 0-эритроциты, отмытые от плазмы крови (в которой содержатся анти-А- и анти-В-антитела). У людей с группой крови 0 эритроциты не имеют на поверхности ни антигенов А, ни антигенов В, но в плазме таких людей присутствуют антитела двух типов (анти-А и анти-В). Вот почему переливать им кровь, несущую антигены А или В, нельзя. Это может вызвать гемолиз. Таким образом, 0 — универсальный донорский тип эритроцитов, а АВ, наоборот, — универсальный реципиент.
Открытие Ландштейнера помогло объяснить, почему переливания крови нередко заканчивались для пациентов трагически. В настоящее время вопрос о подборе донорской крови для переливания решить еще сложнее, требуется согласование по Rh-антигену, который имеет отношение к гемолитической болезни новорожденных. С тех первых иммунологических опытов многочисленные лабораторные исследования позволили выделить и полностью охарактеризовать многие белки, клетки и гены иммунной системы позвоночных. Мы уже не только знаем, как образуются антитела и рецепторы Т-клеток, но знаем и нук-леотидные последовательности генов, вовлеченных в этот процесс. Иммунология решает много важных проблем, и главная из них: сколько же существует специфических антител?
Этот ключевой вопрос был поставлен работами Ландштейнера. Его эксперименты в этой области менее известны неспециалистам, чем открытие системы АВО, хотя они и привели к далеко идущим выводам. Эксперименты Ландштейнера показали гигантский размах разнообразия антител, которые можно получить у лабораторных животных. Превосходный химик, он присоединял мелкие искусственно синтезированные молекулы сложных углеродных колец (например, производных бензола) к белковым антигенам разных типов и демонстрировал образование специфических антител к ним у лабораторных кроликов и мышей. Эти мелкие молекулы (гаптены) сами по себе обычно не вызывали образования антител. Однако будучи присоединенными к белковому носителю, они образовывали гаптен-бел-ковые комплексы, которые становились мощными антигенами, вызывающими образование антител, специфичных и к гаптеновой части, и — еще больше — к белковой.
Само по себе образование антител против таких антигенов не было сколько-нибудь удивительным, так как иммунологи давно получали антитела путем искусственной вакцинации крыс, мышей, кроликов, морских свинок, коз и лошадей. Поразительным было другое, Ландштейнер смог выявить антитела против всех новых химических соединений и лекарств, только что созданных зарождающейся в те годы фармацевтической промышленностью. Этих новых антигенов никогда раньше не было в природе! Этот результат поставил нас перед следующей научной — или даже философской — проблемой. Почему химические вещества, созданные в лабораториях современных фармацевтов, которых до этого никогда не было на Земле, могут вызывать иммунный ответ? Не могло быть никакого давления естественного отбора, направленного на образование антител против субстрата, которого никогда не существовало! Однако Ландштейнер смог показать, что лабораторные животные создают антитела, специфически связывающиеся с любой уникальной молекулярной структурой.
Истинную специфичность антител, полученных Ландштейнером, можно продемонстрировать простым лабораторным опытом. Например, было обнаружено, что антитела к гаптенуА не могут быть удалены из антисыворотки реакциями с гаптена-ми В, С, D, Е, G, Н... и т. д. Другими словами, антитела к гапте-ну А специфичны и не имеют сродства (или имеют очень слабое сродство) ко всему ряду рассматриваемых гаптенов. Однако в более чувствительных тестах — реакциях преципитации — можно наблюдать картину перекрестной реактивности (рис. 3.3). На рисунке знак минус (—) означает, что нет заметного осаждения; один или несколько знаков плюс (от + до +++) указывают на интенсивность осаждения и означают присутствие нерастворимого комплекса антиген—антитело; очень слабое осаждение обозначается (±). По-видимому, антигены D и G как-то связаны с А. И в самом деле, Ландштейнер смог показать, что D и G имеют с А общую молекулярную структуру.
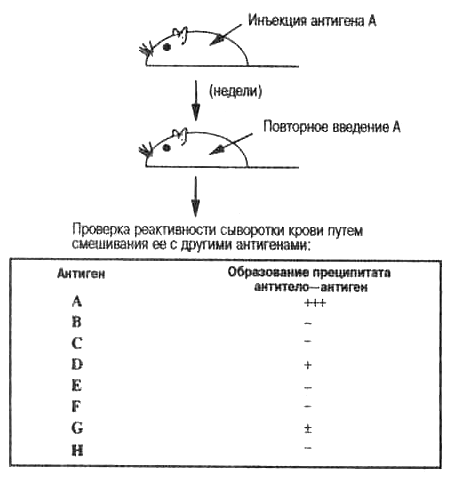
Рис. 3.3. Основа специфичности антител. Иммунизация определенным антигеном (А) вызывает образование антител, которые связываются с А, но не с В, С и т. д. Простейший способ проверки антител состоит в смешивании сыворотки крови с антигенами. Антитела связывают антигены, и на дне пробирки образуется осадок (преципитат). Преципитат в пробирке свидетельствует о наличии антитела, которое может связываться с данным антигеном (- нет преципитата; + следы, +++ сильный преципитат). В данном примере антигены D и G имеют формы (эпитопы, или детерминанты), похожие на А; говорят, что они перекрестно реагируют с А. (также см. табл. 3.1 и рис. 3.6)
Эксперименты Ландштейнера послужили основой первой оценки размера потенциального репертуара антител. Тридцать лет назад был обычным такой комментарий генетических и эволюционных следствий, вытекающих из результатов Ландштейнера: «Тем не менее, трудно понять, какие преимущества дает существование генов для синтеза антител против многих недавно синтезированных органических соединений, таких как п-амино-бензоат, 2,4-динитробензол и т. д., которые совершенно не похожи на микробные патогены. Сохранение такого избытка генетического багажа в течение бесконечного времени до тех пор, пока не появится мишень для них, кажется неправдоподобным»
На самом деле это неправдоподобно в рамках дарвиновского естественного отбора генов, кодирующих определенные специфичные антитела.
Итак, к 1930-м годам стало ясно, что потенциальный репертуар антител должен быть гигантским и насчитывать миллионы или больше специфичностей. Ответ на другой фундаментальный вопрос все еще не был ясен: как могла в ходе эволюции появиться система, способная производить антитела, которые никогда не были частью эволюционной истории данного вида? Если инфекционные болезни были орудием эволюции современной иммунной системы, то, несомненно, частные и специфические молекулярные характеристики множества возможных антигенов никогда не были ее движущей силой. Правильнее, по-видимому, считать, что в ходе эволюции возникла биологическая стратегия, способная производить иммунный ответ на неожиданное.
Будем считать, что инфекционные болезни были главной, если не единственной, селективной силой в эволюции иммунной системы позвоночных. Тогда мы можем довольно легко рассматривать этот процесс в терминах дарвиновского «выживания наиболее приспособленной» иммунной системы. Если это так, то гены иммуноглобулинов (Ig), ответственные за кодирование антител, передаются потомкам через половые клетки, и их сохранение в ходе эволюции определяется теми же дарвиновскими правилами, которым подчинены и другие гены. Теперь мы критически рассмотрим сказанное.
Детальные сравнительные исследования разных видов беспозвоночных (насекомых) и позвоночных показывают, что система приобретенного иммунитета, которую мы сейчас обсуждаем, существует у хрящевых рыб (акул и скатов) и, следовательно, появилась по крайней мере 400—500 миллионов лет назад. У этих рыб есть гены, родственные генам вариабельной области Ig (IgV), или генам рецепторов Т-клеток (ТкР) [5]. В исследованиях Роберта Райсона (Raison) из Технологического университета Сиднея и других показано, что еще более примитивные позвоночные — круглоротые (миксины и миноги) — не имеют системы приобретенного иммунитета; у них нет ни IgV, ни ТкР-генов. До сих пор идет поиск недостающего звена. Однако пока не известны эволюционные переходы между кругло-ротыми и хрящевыми рыбами. И нет никаких гарантий, что недостающие звенья когда-нибудь будут найдены, так как все они, возможно, вымерли. На рис. 3.4 показаны основные представители позвоночных, у которых работа иммунной системы изучена подробно. Даже у холоднокровных позвоночных — рыб — можно обнаружить основные элементы системы приобретенного иммунитета теплокровных. Иммунные системы всех изученных позвоночных имеют следующие свойства:
• они способны создавать гигантское разнообразие антител и Т-клеток, обеспечивающее ответ на практически любой антиген;
• они способны к усиленному ответу при повторной встрече с антигеном (имеют память);
• они способны обеспечивать аутотолерантность.
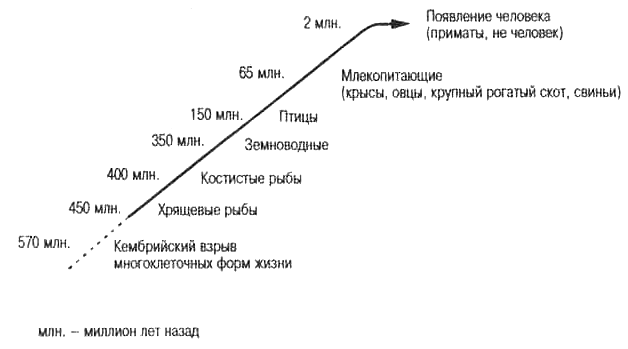
Рис. 3.4. Позвоночные, у которых обнаружена сходная с млекопитающими система иммунитета.
Если мы иммунизированы коклюшной или столбнячной вакциной, наша иммунная система «помнит» первую встречу с этими антигенами, позволяя нам быстрее и сильнее реагировать на новую встречу с тем же самым антигеном образованием более высоких концентраций антител в крови. Эти свойства — направляемое антигеном изменение соматических клеток, специфичность, аутотолерантность и память — являются признаками иммунных систем всех позвоночных. У акул и других холоднокровных животных из-за низких температур окружающей среды иммунный ответ медленнее, чем у теплокровных наземных позвоночных.
Большая часть информации о клеточных и молекулярных процессах в иммунной системе получена экспериментальной иммунологией в опытах с иммунизацией мышей инбредных линий. Также много данных получено в клинических наблюдениях; сейчас мы знаем, что практически любая клетка, молекула и ген, обнаруженные у мышей, существуют и у человека. Хотя на других позвоночных проведено гораздо меньше исследований, очевидно, что при переходе от холоднокровных хрящевых рыб к теплокровным наземным животным сложность иммунной системы возрастала. Например, мы знаем, что генетическая стратегия, используемая для сохранения длинных последовательностей ДНК, кодирующих большое число различных антител у акул, менее экономична, чем у мышей и человека. У кроликов последовательности ДНК используются еще более эффективно. Однако самая эффективная система описана у кур и других птиц. Это станет понятным, когда мы обсудим уникальную природу генов, кодирующих антитела.
Теперь кратко рассмотрим структуру молекулы антитела. Все антитела имеют общий план строения — это белки, состоящие из нескольких субъединиц. На рис. 3.2 показано строение наиболее обычного антитела, называемого IgG. Эта структура была впервые описана в 1960-е годы в лаборатории Джералда Эдель-мана (Edelman) и Родни Портера ( Porter), которые были удостоены Нобелевской премии в 1972 г. Антигенсвязывающий центр состоит из вариабельных (V) областей тяжелой (Н) и легкой (L) белковых цепей, объединенных в HL-гетеродимер. Каждая молекула антитела состоит из двух идентичных HL ге-теродимеров, кроме пентамера IgM, у которого десять HL-гете-родимеров (рис. 3.2 и 3.5). Константная (постоянная) С-область молекулы запускает лизис (разрушение) или фагоцитоз (поглощение фагоцитом) чужих бактериальных клеток и частиц после связывания с ними антитела (рис. 3.1).
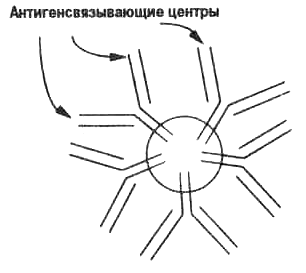
Рис. 3.5. Строение пентамерной молекулы IgМ антитела, состоящей из 10 HL-гетеродимеров (5 мономеров молекулы IgМ). Подробности в табл. 3.1. Каждый антигенсвязывающий центр имеет невысокую аффинность, но связывание во многих центрах увеличивает среднюю авидность антитела (см. рис. 3.7).
По правилам традиционной генетики для кодирования Н-цепи антитела нужен один ген, а для кодирования L-цепи — другой. Достаточно ли в нашем геноме ДНК для кодирования всех специфичных антител (скажем, миллиона)? Этот важный вопрос был поставлен в 1960-е годы Мелвином Коном (Cohn) и другими учеными сразу после расшифровки генетического кода. Этот вопрос и проблема механизма аутотолерантности заставили усилить внимание к стратегии, которой должна следовать иммунная система при создании того разнообразия связывающих антигены рецепторов, которое необходимо для борьбы с инфекционными заболеваниями. Стратегия ли это «зародышевой линии», при которой все специфичные антитела закодированы в яйцеклетках и сперматозоидах? Или же иммунная система использует особую «соматическую» стратегию, при которой гены в лимфоцитах мутируют или случайно рекомбинируют, образуя дополнительное разнообразие в репертуаре HL-центров?
В 1960-е и начале 1970-х годов среди ученых, придерживающихся этих двух принципиально различных мнений, происходили кратковременные, но частые теоретические сражения. Тем не менее к концу 1970-х годов благодаря молекулярно-ге-нетаческим работам Сусуми Тонегава (Tonegawa), получившего в 1987 г. Нобелевскую премию, эта проблема была в основном решена. Сейчас мы знаем, что часть разнообразия создается генами зародышевой линии, но случайные соматические процессы (рекомбинация и мутация) также необходимы для образования гигантского разнообразия антител и рецепторов Т-клеток. То есть, в течение жизни наш организм «учится» бороться с многочисленными захватчиками и создает в лимфоцитах много новых ДНК-последовательностей, кодирующих антитела. Далее мы обсудим данные, указывающие на то, что ДНК-последовательности из лимфоцитов могут быть включены в половые клетки и переданы следующим поколениям.
Теперь мы конкретизируем основные элементы проблемы создания репертуара антител и молекулярные детали иммунного ответа. Тяжелая цепь каждого антитела представляет собой белок, состоящий примерно из 400 аминокислот (100 в V-обла-сти и 300 в С-области), а каждая легкая цепь состоит примерно из 200 аминокислот (100 в V-области и 100 в С-области). Так как каждая аминокислота определяется кодоном из трех оснований (приложение), в последовательности ДНК, необходимой для кодирования каждого HL-гетеродимера, должно быть по крайней мере 1800 (600 • 3) оснований при условии, что и Н-, и L-це-пи кодируются традиционными генами. Если существует 1 млн. разнообразных антител (по современным представлениям эта оценка разумна), это означает, что в геноме человека почти 2 млрд. (1800 • 1 000 000 или 1,8 • 109) оснований кодируют только возможный репертуар антител. Даже если ограничиться только существенной информацией, то есть V-областями, а именно они составляют антигенсвязывающий центр, то это число уменьшится до 0,6 • 109 оснований. А весь геном человека содержит максимум 3—4 млрд. оснований! Таким образом, по самым минимальным оценкам, от 1/6 до 1/2 всей ДНК должны кодировать молекулы антител!
Когда 30 лет назад впервые оценили это число, исследователи поняли, что Ig-гены, кодирующие антитела, должны иметь особую стратегию хранения информации, отличную от других генов. Эти другие гены мы будем называть «однокопийными», или просто генами «домашнего хозяйства». Кроме того, в других работах, проведенных в 1970-е годы, было показано, что в промежутках между генами расположены некодирующие последовательности ДНК, (их часто называют «избыточной» ДНК). Было показано, что на «избыточную» ДНК приходится примерно 98 процентов или даже больше от всей ДНК генома позвоночных. («Избыточная» ДНК не кодирует белковые последовательности, но, по-видимому, играет какую-либо важную функциональную роль. Она может участвовать в упаковке хромосом или в регуляции активности генов и репликации ДНК.) Эти вычисления означали, что если антитела кодируются традиционными генами, то в зародышевой линии хватит кодирующей ДНК только для 10 000 антител, а не для 1 млн., как был оценен репертуар антител. А что же остается для всех генов «домашнего хозяйства?»
Итак, уже к концу 1960-х годов стало очевидно, что все разнообразие антител не может быть закодировано только в половых клетках. Жизнь нуждается в гораздо большем, чем только в производстве антител! Одним из возможных решений явилось предположение, что разнообразие Ig-генов, ответственных за кодирование антител, каким-то образом генерируется соматическими событиями. Работа Сусуми Тонегава, продемонстрировавшая уникальные перестройки ДНК, кодирующей V-области антител, и работы многих других исследователей, показавшие соматическое мутирование V-генов, наконец, разрешили эту проблему. Обсуждение этого вопроса мы продолжим в разделе, посвященном структуре Ig-генов.
Иммунная система развивалась для борьбы с острыми инфекционными заболеваниями. Возбудитель, попадая в организм, начинает размножаться, но то же самое делают и его враги — Т- и В-лимфоциты. Исход болезни зависит от того, у кого скорость размножения выше. Теперь мы кратко рассмотрим, каковы роли некоторых действующих лиц в этом состязании.
Антитела относятся к классу растворимых белков, называемых иммуноглобулинами (сокращенно Ig). Их продуцируют и выделяют в кровь и тканевую жидкость белые кровяные клетки, которые называются В-лимфоцитами. В элиминации чужеродного агента участвуют и некоторые дополнительные факторы, которые вызывают лизис (разрушение) бактериальных клеток, покрытых антителами. Антитела могут нейтрализовать вирусные частицы, прочно связываясь с ними и тем самым препятствуя их проникновению в клетки-мишени. Кроме того, специальные клетки, называемые фагоцитами, могут заглатывать покрытые антителами частицы и разрушать их. Этот процесс изображен на рис. 3.1. Выгодно, если антитело связывается с антигеном при очень низких концентрациях того и другого, то есть на ранних стадиях инфекции, когда в организме присутствует только очень небольшое число болезнетворных агентов. Однако это возможно лишь в том случае, если защитные антитела прочно связываются с антигеном, или обладают высокой авидностью. Если авидность антитела низкая, связывания при низких концентрациях антигена или антитела может и не произойти.
Если заболевание вызвано вирусом, иммунная система реагирует также образованием «клеток-убийц» (цитотоксических Т-лимфоцитов). Каждый Т-лимфоцит несет на поверхности специфические рецепторы, сходные с антителами. Эти рецепторы называются рецепторами Т-клеток — ТкР. Они распознают и связывают измененные молекулы на поверхностной мембране инфицированных вирусом клеток, что приводит к лизису этих клеток. Цитотоксические Т-клетки не вредят нормальным незараженным клеткам, так как не могут связывать их своими ТкР.
К сожалению, не у всех из нас иммунная система работает надежно и эффективно. Кто-то страдает от астмы или аллергии из-за того, что в отношении какого-либо внешнего раздражителя иммунная система заходит слишком далеко. Другие живут с рассеяным склерозом, потому что иммунная система разрушает их собственные нервные волокна, или страдают от иммунного дефицита, который затрудняет борьбу с инфекциями.
К концу 1960-х годов исследования естественных иммуноде-фицитов человека показали, что существует две основные категории острых нарушений иммунитета. Дети, не способные производить антитела (агаммоглобулинемия), не могут бороться с обычными бактериальными инфекциями, но нормально переносят детские вирусные инфекции, например корь. И наоборот, дети, у которых не было нормального тимуса (атимиче-ские), производят антитела и удовлетворительно справляются с бактериальными инфекциями, но не способны излечиваться от вирусных инфекций. В конце 1960-х гг. Боб Бландэн, работавший в Центре медицинских исследований имени Джона Кертина в Канберре, экспериментально показал, что излечение от острых вирусных инфекций у мышей зависит от ответа Т-лимфоцитов на инфекцию. К началу 1970-х гг. Боб совместно с другими исследователями из его лаборатории обнаружил, что Т-лимфоциты убивают инфицированные вирусом клетки до завершения цикла репликации вируса, пресекая, таким образом, инфекцию в зародыше. Другие исследователи показали, что Т-лимфоциты выделяют растворимые факторы (интерфероны), которые предотвращают размножение вируса в окружающих клетках. Интерфероны и другие растворимые цитокины сейчас производят с помощью клонирования и экспрессии генов цитокинов в бактериальном хозяине. Чистые цитокины назначают пациентам, страдающим некоторыми формами иммунного дефицита, для увеличения активности костного мозга и Т-клеток и, следовательно, улучшения ответа на инфекцию.
В 1973 г. Питер Догерти и Ролф Цинкернагель, также работавшие в Центре медицинских исследований имени Джона Кертина, показали, что в процессе распознавания Т-лимфоцитами инфицированных вирусами клеток участвуют не только вирусные антигены (что ожидалось), но и основные антигены гистосовместимости, или тканевой совместимости, самой клетки (что было неожиданным). Антигены гистосовместимости — это молекулы, ответственные за отторжение чужих тканей. Они различны у разных людей и вызывают сильный ответ Т-лимфо-цитов. Однако пересадка чужих тканей — не естественное явление, так что истинная биологическая функция этих антигенов была неизвестна до открытия Догерти и Цинкернагеля. Это открытие произвело коренные перемены в клеточной иммунологии, а Догерти и Цинкернагель получили Нобелевскую премию по физиологии и медицине в 1996 г.
Антигенспецифичные рецепторы Т-клеток (ТкР) распознают вирусные антигены, ассоциированные с главными антигенами гистосовместимости. Антител, связывающихся с такой ассоциацией, не образуется. Таким образом, Т-клетки и антитела никогда в норме не конкурируют за одни и те же сайты на поверхности клетки. Это можно продемонстрировать простым экспериментом. Если искусственно создать антитела к сайтам, узнаваемым Т-клетками, и добавить их к смеси инфицированных клеток и Т-клеток, то лизиса клеток не происходит, и вирусная инфекция успешно развивается. Этот эксперимент иллюстрирует селективные преимущества иммунной системы позвоночных, в которой Т-клетки и антитела не конкурируют за связывание с одними и теми же сайтами на поверхности инфицированной клетки.
Изучение описанных выше естественных иммунодефицитов у человека показало, что в отсутствие тимуса (и Т-лимфоцитов, которые развиваются в тимусе) могут образовываться антитела против бактериальных инфекций. Эти антитела относятся к классу иммуноглобулинов IgM. Секретируемая форма IgM, появляющаяся в ответ на бактериальную инфекцию без участия Т-лимфоцитов, представляет собой пентамер, то есть состоит из пяти молекул, структура которьк показана на рис. 3.2. Каждая из этих молекул имеет два антигенсвязывающих центра. Таким образом, пентамерный IgM имеет десять антигенсвязывающих центров (рис. 3.5).
Важная аксиома биологии гласит, что эффективность биохимической реакции зависит от степени связывания или сли-пания разных молекул. Взаимодействие между отдельным центром связывания антитела с комплементарным ему антигеном можно оценить количественно. Для этого в пробирке смешивают антиген и антитело в разных концентрациях и определяют, какая часть смеси находится в связанной форме (комплекс антиген—антитело), а какая — в несвязанной (рис. 3.6). Этот метод дает возможность оценить аффинность (сродство) антигенсвязывающего центра. Когда связывается больше одного центра, как у IgG или мономера IgM, имеющих по два центра, или у пентамера IgM с десятью центрами, в действие вступает новый фактор. Если чужеродный агент имеет на поверхности множество идентичных структур (как у бактериальных или вирусных частиц), то, как только происходит одно взаимодействие антиген—антитело, вероятность второго возрастает, и так далее (рис. 3.7). Таким образом, пентамер IgM может прилипать к поверхности бактерии, даже если аффинность отдельного антигенсвязывающего центра низка (из-за относительно плохого соответствия антигену). Сила такого множественного связывания антигена с антителом называется авидностью. Итак, высокая авидность IgM обеспечивает организму селективные преимущества, так как он образуется в первые часы и дни инфекции и способен связывать бактерии в крови и вызывать их элиминацию.
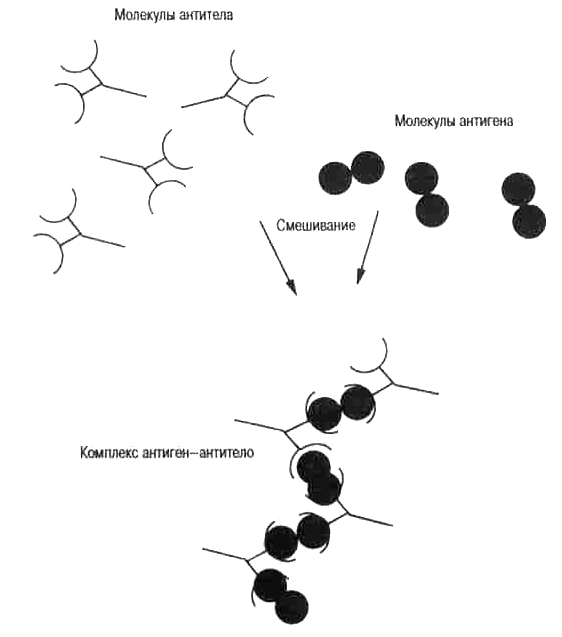
Рис. 3.6. Схема образования комплексов антиген-антитело. Комплексы антигенов и антител часто нерастворимы и осаждаются из раствора (рис. 3.3). Такие комплексы связываются с поверхностной мембраной клеток, например, фагоцитов, константной областью Н-це-пи антитела, давая клетке возможность поглотить их и переварить (рис. 3.1). В центрах размножения особые клетки, которые называются фолликулярными дендритными клетками (ФДК), представляют такие комплексы для отбора мутантных вариабельных областей с высокой аффинностью (рис. 5.4). Детали описаны в табл. 3.1.
Пентамерный IgM — крупная молекула, которая не может проникать через стенки кровеносных сосудов. Необходимы антитела помельче; это — иммунноглобулины класса IgG. Обычно IgM-ответ длится несколько дней, а затем происходит переключение на образование более мелких антител класса IgG , которые имеют только два антигенсвязывающих центра вместо десяти (рис. 3.8). Это переключение достигается в результате ряда сложных молекулярных событий, которые затрагивают определенные ДНК-последовательности генов IgG (молекулярные детали этого процесса мы не рассматриваем).
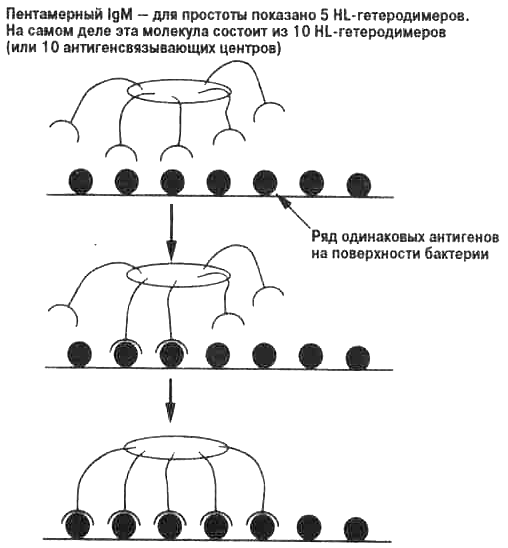
Рис. 3.7. Связывание пентамерного IgM с рядом одинаковых антигенов. Пентамерный IgM имеет много одинаковых антигенсвязывающих центров, у каждого из которых может быть низкая аффинность (рис. 3.5). Однако в результате множественного связывания с поверхностью антигена, например, с бактериальной клеткой (которая представляет собой ряд одинаковых антигенных эпитопов) пентамерный IgM связывается очень прочно (имеет высокую авидность). На рисунке показано множественное связывание высокой авидности. Если один центр связывается с антигеном, вероятность связывания соседнего центра возрастает. Когда сцеплены множественные антигенсвязывающие центры, общая сила связывания (авидность) оказывается много выше, чем у одного связывающего центра.
Переключение с синтеза IgM на синтез IgG иллюстрирует одну аксиому иммунологии, которая признается еще не всеми иммунологами. Эта аксиома утверждает, что единственное эволюционное селективное преимущество, которое дает специфичность в системе приобретенного иммунитета (антитела и ТкР), это возможность различения своего от не-своего. Так, IgM полезны, потому что, несмотря на низкую специфичность и низкую аффинность (плохое соответствие) отдельного связывающего центра, десять связывающих центров пентамерного IgM дают возможность одному и тому же антителу связывать множество родственных антигенов различных инфекционных агентов. Однако нужда в мелких, проникающих через стенки сосудов, антителах привела к появлению механизма переключения с производства IgM на производство IgG. Два антигенс-вязывающих центра IgG должны иметь большую аффинность, чем десять центров пентамерного IgM. В процесс переключения вовлекаются В-клетки с самой высокой аффинностью. Отбор таких клеток основан на конкуренции за связывание антигена в особых участках лимфоидной ткани (гл. 5). Еще одно селективное преимущество, которое дает механизм переключения, связано с эволюцией других классов антител (IgA, IgE), выполняющих свои специфические функции в различных тканях организма.

Рис. 3.8. Первичный и вторичный гуморальный ответ. Типичная зависимость от времени гуморального ответа у лабораторных мышей. На практике у человека вторичное введение антигена отделено от первичного месяцами или даже годами. Аффинность антител первичного ответа обычно ниже, чем антител вторичного ответа, «ответа памяти». Антитела, образованные во вторичном ответе, обычно оказываются соматически мутировавшими молекулами IgG или IgM , которые имеют более высокую аффинность, чем IgG- или lgM-антитела, образованные ранее (см. табл. 3.1 и гл. 5).
Наша иммунная система распознает большое число различных антигенов и реагирует на них. Чаще всего антигены — это белки и углеводы. (Углеводы — это полимеры, состоящие из разного числа молекул глюкозы или других Сахаров.) Следовательно, мир потенциальных биологических антигенов огромен. Иммунная система характеризуется способностью синтезировать почти безграничное число специфичных антител против чужеродных белков и углеводов. Каждое антитело способно отличить чужеродный антиген от собственных антигенов и участвует в элиминации чужеродных антигенов из организма.
В отличие от этого практически безграничного репертуара антител Т-лимфоциты узнают только короткий фрагмент (пептид) чужого белка, связанный специальной полостью в молекуле МНС антигена на поверхности клетки. Репертуар рецепторов Т-лимфоцитов (ТкР) ограничен вариациями МНС антигенов, которые создаются при связывании их с коротким чужеродным пептидом. Сложный многоэтапный процесс отбора развивающихся в тимусе Т-лимфоцитов обеспечивает создание этого ограниченного репертуара рецепторов в популяции функционирующих Т-клеток. Другой ряд сложных процессов, вовлеченных в образование антител в В-лимфо-цитах, приводит к тому, что не образуется антител против измененных МНС антигенов. Таким образом, антитела и рецепторы узнают разные стороны мира чужих антигенов.
Как достигается эта удивительная способность распознавать целый мир различных чужеродных антигенов и в то же время избегать ответа против собственных антигенов? Ответ на этот вопрос удалось получить в результате 40 лет иммунологических исследований. Мы рассмотрим его в следующей главе при обсуждении «клональной селекции».
Теперь оставим в стороне проблемы, связанные с разнообразием молекул иммунной системы, и рассмотрим другое фундаментальное свойство системы — невосприимчивость (толерантность) к собственным антигенам.
Реакция на чужеродные антигены («не-свое») — это только одна сторона медали, другая состоит в том, что у здоровых индивидов иммунная система почти никогда не производит антител и киллерных Т-клеток против тканей и клеток собственного организма. В норме может наблюдаться только очень кратковременная реакция против самого себя. И это несмотря на то, что химический состав белков и углеводов собственного организма очень похож на молекулярные структуры чужеродных антигенов. Эта неспособность организма реагировать на самого себя названа аутотолерантностью. Она была обнаружена в начале двадцатого века немецким микробиологом Паулем Эрлихом, который в общих чертах описал ее значение и проанализировал глубокие последствия, наступающие при нарушении аутотолерантности. Он назвал механизм, заставляющий иммунную систему организма отличать свое от не-своего, «страхом самоотравления» (horror autotoxicus). Сейчас мы знаем, что имел в виду Пауль Эрлих, когда говорил о выходе иммунной системы из-под контроля и нарушении аутотолерантности. Обнаружены подтачивающие здоровье аутоиммунные заболевания, когда организм стремится отторгнуть самого себя. К этим заболеваниям относятся, например, ревматоидный артрит (вызванный иммунной реакцией против соединительной ткани) и рассеяный склероз (вызванный иммунной атакой против нервной ткани). Если речь идет о реакции против «не-своего», мы знаем, что иммунная система важна для выживания. Если она работает неэффективно (при синдромах врожденных и приобретенных иммунных дефицитов), человек и другие позвоночные погибают от таких инфекционных агентов, которые в норме уничтожаются иммунной реакцией.
Так как же достигается аутотолерантность? Как она поддерживается, однажды появившись? Определяется ли она нашими генами и, таким образом, предопределена антигенами и антителами, унаследованными от родителей? Или она приобретается в течение жизни каждого индивида? С научной и философской точек зрения это не тривиальные вопросы. Только сейчас исследования на молекулярном и клеточном уровнях начинают давать ответы на них. Эти вопросы важны для поиска способов, которыми мы можем заставить иммунную систему нарушить нормальные правила поведения и начать бороться с раком (со «своим») или стать толерантной к пересадкам чужих органов и тканей (к «не-своему»).
Способностью реагировать на неожиданное и памятью обладает еще только одна система — центральная нервная система. Основное отличительное свойство иммунной системы состоит в том, что ее клетки (лимфоциты, фагоциты и другие белые кровяные клетки) могут быть как подвижными, циркулирующими по всему организму (рис. 3.9), так и включаться в неподвижные (фиксированные) ткани печени, селезенки, лимфатических узлов, кожи и кишечного тракта. В центральной нервной системе, наоборот, все нейроны и нервные волокна образуются очень рано и занимают фиксированное положение на протяжении всей взрослой жизни. Подобно тому, как нервная система следит за состоянием тканей организма и подачей сигналов мышцам всего тела, так и иммунная система с помощью системы подвижных клеток, которые мигрируют через лимфатические и кровеносные сосуды, следит за антигенной целостностью организма (рис. 3.9). Во времени и пространстве осуществляется мощный поток клеток и молекул (антител и других белков).
У взрослых все белые кровяные клетки образуются в костном мозге. Ежедневно появляются миллионы таких клеток. Они необходимы, чтобы постоянно заменять клетки, погибшие в разных тканях. Лимфоциты, образовавшиеся в костном мозге, дифференцируются затем в В-клетки, производящие антитела, и в Т-клетки. Предшественники Т-клеток покидают костный мозг и попадают в тимус, где они проходят дальнейшее развитие (дифференцировку), и на их поверхностной мембране появляются рецепторы ТкР. После этого зрелые Т-клетки покидают тимус.
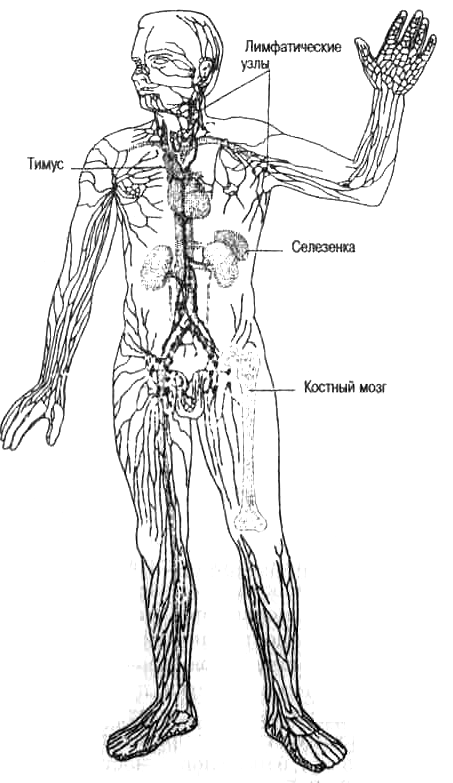
Рис. 3.9. Лимфоидная система человека. Лимфоидная система состоит из обширной сети лимфатических сосудов и лимфоидных органов (лимфатические узлы, селезенка, тимус). Лимфатические сосуды пронизывают большинство тканей и органов, соединяют лимфатические узлы и, наконец, впадают через грудной проток в кровь. Все В- и Т-лимфоциты (и другие белые кровяные клетки, и красные кровяные клетки) развиваются в костном мозге (стволовые клетки в костном мозге непрерывно делятся, образуя миллионы клеток в день). Те клетки, которые станут Т-лимфоцитами, мигрируют с кровью в тимус (вилочковую железу), где они созревают и экспортируются как зрелые Т-лимфоциты, способные к хелперным и киллерным функциям. В-лимфоциты, которые продуцируют антитела, сначала развиваются в костном мозге, затем мигрируют через кровь и лимфатический проток в лимфоидную систему и заселяют периферические лимфатические узлы, например, аденоиды, миндалины и селезенку. Лимфатические узлы в тонком кишечнике называются пейеровыми бляшками. Подвижные Т- и В-лимфоциты по кровеносным и лимфатическим сосудам могут мигрировать во все части тела, включая репродуктивные органы. Каждый лимфатический узел пронизан очень тонкими капиллярами, по которым идет движение молекул и клеток из крови в лимфу. ( По N.K. Jerne. Scientific American, vol.229: 52, 1973. Copyright ©Scientific American Inc. Мы признательны художнику Бунджи Тагава за разрешение перепечатать этот рисунок.)
Зрелые В- и Т-клетки (вместе с фагоцитами) заселяют периферические органы иммунной системы (селезенку и лимфатические узлы) и циркулируют по организму с кровью и лимфой. Лимфатические узлы расположены по всему телу, и те, которые находятся рядом с местом внедрения инфекционного агента, обычно реагируют первыми (рис. 3.9). Таким образом, иммунная система может быстро обнаружить попадание бактериальных или вирусных частиц в организм. Узлы увеличиваются (даже становятся болезненными), так как в них происходит быстрое деление и иммиграция из кровотока активированных антигеном лимфоцитов и других белых клеток. Каждый из нас знает по собственному опыту, что такое припухшие, болезненные лимфатические узлы (обычно в горле, паху, подмышке) после введения вакцины или во время болезни.
В 1930-х и 1940-х годах небольшая группа иммунологов и химиков (под руководством Фрэнка Макфарлейна Бернета, Лай-нуса Полинга (Pauling), Карла Ландштейнера, Фридриха Брени (Breini) и Феликса Горовица (Haurowitz) занялась выяснением механизма образования антител, обеспечивающего системе возможность реагировать на неожиданное. Это было задолго до того, как стали известны химический состав и структура генетического материала (ДНК) и законы, управляющие потоком генетической информации (т. е. ДНК<-^РНК->белок). В те годы общераспространенной была так называемая «инструктивная» модель Брени, Горовица и Полинга. Согласно этой модели, антиген как матрица просто воздействует на специфичное складывание гибкого Ig-белка в определенную форму и вызывает образование большого числа копий специфичного антитела, необходимого для борьбы с инфекцией (рис. 3.10).

Рис 3.10. Инструктивная модель образования антител Лайнуса Поллинга. Четыре стадии формирования молекулы нормального иммуноглобулина сыворотки крови и шесть стадий формирования антитела в результате взаимодействия белковой цепи иммуноглобулина с молекулой антигена. Внизу справа изображена молекула антигена, окруженная присоединенными к ней молекулами антител или их частями, что прекращает дальнейшее образование антител. (По рис. 1 из книги Linus Pauling. A Theory of the Structure and Process of Formation of Antibodies. Перепечатано с разрешения Химического общества Америки.)
Сейчас известно, что эта модель неверна. Белки антител не складываются под действием антигена в специфичную форму. Теперь мы знаем, что последовательность аминокислот диктует способ складывания белка, и осуществляется этот процесс с помощью недавно открытых белков — шаперонов. В свою очередь, последовательность аминокислот определяется линейной последовательностью оснований в ДНК и триплетным кодом при участии информационной РНК (см. гл. 2 и рис. 2.4). Инструктивной теорией нельзя объяснить и такие свойства иммунной системы, как экспоненциальный рост концентрации антител в ходе иммунного ответа и аутотолерантность. В конце концов, эти противоречия привели к кончине «инструкционизма» и появлению на свет альтернативных «селекционных» теорий, вершина которых — клонально-селекционная теория Бернета, впервые опубликованная в 1957 г.